
A、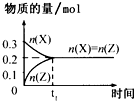 |
B、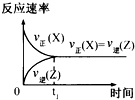 |
C、 |
D、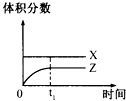 |


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:高中化学 来源: 题型:
 ②
② ③
③ ④HC≡CCH3 ⑤CH3CH2CH3 ⑥CH3CH=CHCH3( )
④HC≡CCH3 ⑤CH3CH2CH3 ⑥CH3CH=CHCH3( )| A、①和② | B、①和③ |
| C、①和④ | D、③和⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
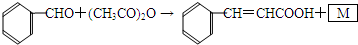

查看答案和解析>>
科目:高中化学 来源: 题型:

| A、氧化剂与还原剂必须直接接触,才能发生反应 |
| B、乙池中电极反应式为NO3-+4H++e-═NO2↑+2H2O |
| C、当铜棒质量减少6.4g时,甲池溶液质量增加6.4g |
| D、当铜棒质量减少6.4g时,向乙池密封管中通入标准状况下1.12L O2,将使气体全部溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
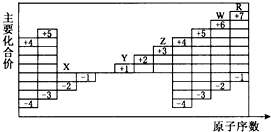 如图是部分短周期元素原子序数与主要化合价的关系图,X、Y、Z、W、R是其中的五种元素.下列说法不正确的是( )
如图是部分短周期元素原子序数与主要化合价的关系图,X、Y、Z、W、R是其中的五种元素.下列说法不正确的是( )| A、原子半径:Y>X |
| B、最高价氧化物的水化物的酸性:R>W |
| C、气态氢化物的稳定性:X>W |
| D、单质与水(或酸)反应的剧烈程度:Z>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加热可增强纯碱溶液去污力:CO32-+2H2O═H2CO3+2OH- |
| B、用稀硝酸洗涤做过银镜反应的试管:Ag+4H++NO3-═Ag++NO↑++2H2O |
| C、向煤中加入石灰石可减少煤燃烧时SO2的排放:2CaCO3+O2+2SO2═2CO2+2CaSO4 |
| D、碳酸氢钠溶液与少量澄清石灰水混合出现白色沉淀:HCO3-+Ca2++OH-═CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 实验内容 | 实验目的 |
| A. | 向盛有10滴0.1mol/L AgNO3溶液的试管中滴加0.1mol/L NaCl溶液,至不再有沉淀生成,再向其中滴加0.1mol/L Na2S溶液 | 证明AgCl沉淀能转化为溶解度更小的Ag2S沉淀 |
| B. | 向2 mL甲苯中加入3滴KMnO4酸性溶液,振荡;向2mL苯中加入3滴KMnO4酸性溶液,振荡 | 证明与苯环相连的甲基易被氧化 |
| C. | 向Na2SiO3溶液中通入CO2 | 证明碳酸的酸性比硅酸强 |
| D. | 在淀粉溶液中加入稀硫酸,水浴加热,一段时间后,再加入新制的氢氧化铜并加热 | 验证淀粉已水解 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验内容 | 实验目的 |
| A | 室温下,用pH试纸分别测定浓度为0.1mol?L-1 NaClO溶液和0.1mol?L-1 CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaC12固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 向10mL 0.2mol/L NaOH溶液中滴入2滴0.1mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/L FeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下的Ksp: Mg(OH)2>Fe(OH)3 |
| D | 分别测定室温下等物质的量浓度的Na2SO3与Na2CO3溶液的pH,后者较大 | 证明非金属性S>C |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
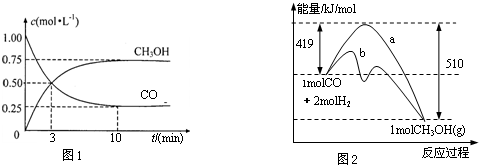
| n(CH3OH) |
| n(CO) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com