
2006年5月14日某新闻媒体报道齐齐哈尔第二制药有限公司生产的假药事件,“齐二药”违反规定,购入工业用“二甘醇”代替医用丙二醇(C3H8O2)作辅料,用于“亮菌甲素注射液”的生产,导致多名患者肾功能衰歇,造成多名患者死亡.二甘醇又称乙二醇醚,分子式为C4H10O3(HO﹣CH2﹣CH2﹣O﹣CH2﹣CH2﹣OH),二甘醇是一种重要的化工原料,可以制取酸、酯、胺等,其主要产品有吗啉及其衍生物1,4﹣二恶烷等被广泛应用于石油化工、橡胶、塑料、制药等行业,用途十分广泛.二甘醇一般的合成路线为:

请回答下列问题:
(1)下列关于“丙二醇”和“二甘醇”及“乙二醇”的有关说法正确的是
A.丙二醇是乙二醇的同系物
B.它们具有相同种类和数目的官能团,性质上完全相同
C.“丙二醇”和“二甘醇”在病人体内都能被氧化为草酸
D.分离“丙二醇”和“二甘醇”可采用分液的方法
(2)过程Ⅰ是石油加工中常用步骤,其名称为 .
(3)从物质B到物质C的过程如果条件控制不好会生成物质E,E可用于金属的切割,则为了能得到二甘醇D,物质B到物质C的反应条件是 ,该反应属于 取代反应 (添反应类型).写出B可能生成E的化学方程式: .
(4)物质D是二甘醇,则合成路线中的物质A、B、C的结构简式分别是:
A: B: C:
(5)反应Ⅲ的化学方程式为: .
(6)写出二甘醇制备1,4﹣二恶烷的化学方程式: H.
考点:
有机物的推断;结构简式;取代反应与加成反应.
专题:
压轴题;有机物的化学性质及推断.
分析:
(1)A、丙二醇与乙二醇含有相同的官能团﹣OH,且数目相同,其它为单键,组成通式相同;
B、二甘醇除含有2个﹣OH,还含有醚键,与丙二醇、乙二醇含有的官能团不同;
C、丙二醇可以氧化物为草酸,二甘醇氧化物HOOCHCH2﹣O﹣CH2CHO0H;
D、分液可以分离互不相溶的液体,丙二醇与二甘醇互溶;
(2)由石油裂解生成乙烯;
(3)BrCH2CH2Br在氢氧化钠水溶液、加热下发生取代反应生成HOCH2CH2OH,如果条件控制不好会发生消去反应生成乙炔,可用于金属的切割;
(4)由二甘醇的合成路线可知,A为C2H2,B为BrCH2CH2Br,C为HOCH2CH2OH,D为HOCH2CH2﹣O﹣CH2CH2OH,
(5)反应Ⅲ是乙二醇在浓硫酸、加热条件下发生分子间脱水生成HOCH2CH2﹣O﹣CH2CH2OH;
(6)二甘醇在浓硫酸、加热条件下发生脱水反应生成1,4﹣二恶烷( ).
).
解答:
解:(1)A、丙二醇与乙二醇含有相同的官能团﹣OH,且数目相同,其它为单键,组成通式相同,故A正确;
B、二甘醇除含有2个﹣OH,还含有醚键,与丙二醇、乙二醇含有的官能团不同,故B错误;
C、丙二醇可以氧化物为草酸,二甘醇氧化物HOOCHCH2﹣O﹣CH2CHO0H,故C错误;
D、丙二醇与二甘醇互溶,不能利用分液方法分离,故D错误;
故选A;
(2)由石油裂解生成乙烯,故答案为:裂解;
(3)BrCH2CH2Br在氢氧化钠水溶液、加热下发生取代反应生成HOCH2CH2OH,如果条件控制不好会发生消去反应生成乙炔,反应方程式为:CH2BrCH2Br+2NaOH HC≡CH↑+2 NaBr,
HC≡CH↑+2 NaBr,
故答案为:氢氧化钠水溶液、加热,取代反应,CH2BrCH2Br+2NaOH HC≡CH↑+2 NaBr;
HC≡CH↑+2 NaBr;
(4)由二甘醇的合成路线可知,A为C2H4,B为BrCH2CH2Br,C为HOCH2CH2OH,D为HOCH2CH2﹣O﹣CH2CH2OH,
故答案为:C2H4,BrCH2CH2Br,HOCH2CH2OH,;
(5)反应Ⅲ是乙二醇在浓硫酸、加热条件下发生分子间脱水生成HOCH2CH2﹣O﹣CH2CH2OH,反应方程式为:2HO﹣CH2﹣CH2﹣OH 2HO﹣CH2﹣CH2﹣O﹣CH2﹣CH2﹣OH+H2O,
2HO﹣CH2﹣CH2﹣O﹣CH2﹣CH2﹣OH+H2O,
故答案为:2HO﹣CH2﹣CH2﹣OH 2HO﹣CH2﹣CH2﹣O﹣CH2﹣CH2﹣OH+H2O;
2HO﹣CH2﹣CH2﹣O﹣CH2﹣CH2﹣OH+H2O;
(6)二甘醇在浓硫酸、加热条件下发生脱水反应生成1,4﹣二恶烷(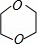 ),反应方程式为:HO﹣CH2﹣CH2﹣O﹣CH2﹣CH2﹣OH
),反应方程式为:HO﹣CH2﹣CH2﹣O﹣CH2﹣CH2﹣OH
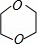 +H2O,
+H2O,
故答案为:HO﹣CH2﹣CH2﹣O﹣CH2﹣CH2﹣OH
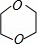 +H2O.
+H2O.
点评:
本题涉及到石油的裂解、有机反应类型、有机反应条件的选择以及烯与卤代烃、醇的性质与转化等,难度中等,注意基础知识的掌握.


科目:高中化学 来源: 题型:
向含有下列离子的溶液中分别加入烧碱固体(溶液体积变化可忽略),离子浓度保持不变的应该是下列选项中的( )
A、OH- B、Na+ C、 HCO3- D、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( )

|
| A. | 元素X与元素Z的最高正化合价之和的数值等于8 |
|
| B. | 原子半径的大小顺序为:rX>rY>rZ>rW>rQ |
|
| C. | 离子Y2﹣和Z3+的核外电子数和电子层数都不相同 |
|
| D. | 元素W的最高价氧化物对应的水化物的酸性比Q的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
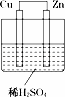
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
| 2011.3.18,实验后的记录: ①Cu为负极,Zn为正极 ②Cu极上有气泡产生,发生还原反应 ③SO42﹣向Cu极移动 ④若有0.5mol电子流经导线,则可产生0.25mol气体 ⑤电子的流向是:Cu﹣→Zn ⑥正极反应式:Cu+2e﹣═Cu2+,发生氧化反应 |
|
| A. | ①②③ | B. | ②④ | C. | ②③④ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中有丰富的资源,多种多样的海洋动物和植物,海底有丰富的矿藏、石油、天然气等,此外,海水中还含有大量的电解质,它们电离产生Cl﹣、Br﹣(溴离子)、SO42﹣、Na+、Mg2+、Ca2+等,都是重要资源.
(1)写出步骤①、②、④分离提纯的方法:
① ② ④
(2)步骤②分离提纯过程中需要选用主要玻璃仪器的名称 .
(3)欲除去初步提纯后的粗盐中的MgCl2、CaCl2和Na2SO4,应向该粗食盐水中依次加入NaOH溶液、 溶液、 溶液,然后过滤;为尽可能除去杂质,每次加入的试剂应 量.向所得溶液中滴加 至无气泡产生,再经蒸发结晶得到食盐晶体.
(4)检验淡水中是否含有Cl﹣ 的操作现象及结论 .
(5)写出加入试剂a后,发生反应的离子方程式 .
(6)工业上用电解饱和食盐水的方法生产氯气、氢气和烧碱,请写出利用氯气和消石灰制取漂白粉的化学方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
对下列实验过程的评价,正确的是()
A. 某固体中加入稀盐酸,产生了无色气体,证明该固体中一定含有碳酸盐
B. 某溶液中先滴加稀盐酸酸化,再滴加几滴BaCl2溶液,生成白色沉淀,证明一定含有SO42﹣
C. 某无色溶液滴入紫色石蕊试液显红色,该溶液一定显碱性
D. 验证烧碱溶液中是否含有Cl﹣,先加稀硝酸除去OH﹣,再加入AgNO3溶液,有白色沉淀,证明含有Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A. 阿伏加德罗常数为6.02×1023
B. 摩尔质量等于该粒子的相对原子质量或相对分子质量
C. 1molH2的体积为22.4L
D. Na+的摩尔质量为23g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的分类不正确的是( )
|
| A. | 水、过氧化氢和干冰都属于氧化物 |
|
| B. | 烧碱、纯碱、熟石灰都属于碱 |
|
| C. | H2SO4、HNO3、H2CO3都属于酸 |
|
| D. | NaHSO4、CuSO4和KMnO4都属于盐 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com