
下列混合溶液中,各离子浓度的大小顺序正确的是 ( )
A.10 mL0.1mol·L-1氨水与10 mL0.1mol·L-1盐酸混合:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
B.10 mL0.1mol·L-1 NH4Cl与5 mL0.2mol·L-1NaOH溶液混合:c(Na+)=c(Cl-)>c(OH-)>c(H+)
C.10 mL0.1mol·L-1醋酸与5 mL0.2mol·L-1 NaOH混合:c(Na+)=c(CH3COO-)>c(OH-)>c(H+)
D.10 mL0.5mol·L-1CH3COONa溶液与6mL0.1mol·L-1盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+)
科目:高中化学 来源: 题型:
 常温下有浓度均为0.1mol?L-1的四种溶液:①碳酸钠溶液;②碳酸氢钠溶液;③盐酸;④氨水.请根据题目要求回答下列问题.
常温下有浓度均为0.1mol?L-1的四种溶液:①碳酸钠溶液;②碳酸氢钠溶液;③盐酸;④氨水.请根据题目要求回答下列问题.| c(OH-) | c(NH3?H2O) |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年河南省原名校高三上学期期联考化学试卷(解析版) 题型:填空题
Ⅰ.某溶液中仅含下表离予中的5种离子(不考虑水的电离及离子的水解),且各离子的物质的量均相等都为0.0lmol。
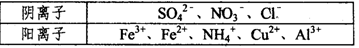
①若向原溶液中加入KSCN溶液,无明显变化。
②若向原溶液中加入过量的盐酸,有气体生成.溶液中阴离子种类不变。
③若向原溶液中加入BaCl2溶液,有白色沉淀生成。
试回答下列问题
(1)若先向原溶液中先加入过量的盐酸,再加入KSCN溶液,现象是__________________。该过程中涉及的离子方程式有________________、__________________。
(2)向原溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体为____________________(写化学式)。
(3)向原溶液中加入足量盐酸后,用排水法收集所产生的气体并使气体恰好充满容器,将容器倒置于水槽中,再向容器中通入___________mLO2(气体体积均指标准状况),能使溶液充满该容器。
Ⅱ.amolCu2S和bmol FeS投入到v L c mol/L的稀硝酸中;充分反应,生成NO气体,所得澄清溶液可以看作Cu(NO3)2、Fe(NO3)3和H2SO4的混合溶液,则反应中未被还原的硝酸的物质的量为 ___________mol(用同时含有a、b、v、c的表达式表示)。
Ⅲ.已知CH4(g)+2O2(g)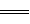 CO2(g)+2H2O(l) △H1=a kJ/mol欲计算反应CH4(g)+4NO(g)
CO2(g)+2H2O(l) △H1=a kJ/mol欲计算反应CH4(g)+4NO(g)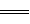 2N2(g)+CO2(g)+2H2O(l)的焓变△H2,则还需要查找某反应的焓变△H3,当反应中各物质化学计量数之比为最简整数比时△H3=b kJ/mol,则该反应的热化学方程式为______________________________________。
2N2(g)+CO2(g)+2H2O(l)的焓变△H2,则还需要查找某反应的焓变△H3,当反应中各物质化学计量数之比为最简整数比时△H3=b kJ/mol,则该反应的热化学方程式为______________________________________。
据此计算出△H2=_____________kJ/mol(用含a和b的式子表示)。
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高一第二次月考化学试卷(解析版) 题型:实验题
(共18分)某次实验需用0.4 mol·L-1 NaOH溶液480 mL。配制方法如下:
(1)配制该溶液应选用_____________mL容量瓶;
(2)用托盘天平准确称量__________ g 固体NaOH;
(3)将称量好的NaOH固体放在500 mL大烧杯中,倒入约300 mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待___________后,将烧杯中的溶液注入容量瓶中;
(4)用少量蒸馏水洗涤烧杯 次,洗涤后的溶液也转移到容量瓶中,轻轻晃动容量瓶,使溶液混合均匀;
(5)向容量瓶中加入蒸馏水,到液面离刻度线_______________ 时,改用___________加蒸馏水至液面最低点与刻度线相切。盖好瓶塞,上下颠倒摇匀。
(6)若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是_________,偏低的是_________,对实验结果没有影响的是_________(填各选项的序号)。
A.所用的NaOH中混有少量NaCl
B.用托盘天平称量一定质量固体NaOH时,砝码上有油污
C.配制溶液所用的容量瓶洗净后没有烘干
D.固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.最后确定NaOH溶液体积(定容)时,俯视观察液面与容量瓶刻度线
G.定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下有浓度均为0.1mol·L-1的四种溶液:①碳酸钠溶液;②碳酸氢钠溶液;③盐酸;④氨水。请根据题目要求回答下列问题。
(1) 上述溶液中,既能与氢氧化钠溶液反应,又能与硫酸溶液反应的是__________。
(2) 取适量溶液④,加入少量氯化铵固体,此时溶液中 ![]() 的值_____(填“增大” 或“减小”或“不变”)。
的值_____(填“增大” 或“减小”或“不变”)。
(3) 将等体积的③和④的溶液混合后,所得溶液中离子浓度由大到小的顺序是:__________。 所得溶液的pH<7,用离子方程式表示其原因________________;混合后的溶液中由水电 离
出的c(OH-)____0.1 mol/L NaOH溶液中由水电离出的c(OH-) (填“>”、“<”或“=”)。
(4) 取10mL溶液③,加水稀释到500mL,则该溶液中由水电离出c(H+)=________________。
(5) 若向氨水中加入pH=1的硫酸,且氨水与硫酸的体积比为1:1,则所得溶液中各离子物质的量浓度由大到小的关系是__________。
(6) 有相同温度下相同浓度的四种盐溶液:A.NH4HCO3;B.CH3COONH4;C.(NH4)2SO4; D.NH4Cl, 按pH由大到小的顺序排列_______ _(填序号)
查看答案和解析>>
科目:高中化学 来源:2012-2013学年辽宁省沈阳二中高二(上)期中化学试卷(解析版) 题型:解答题
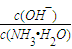 的值______(填“增大”或“减小”或“不变”).
的值______(填“增大”或“减小”或“不变”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com