
使用新型电极材料,以N2、H2为电极反应物,以HC1-NH4C1为电解质溶液,可制造出一种既能提供电能,又能实现氮固定的新型燃料电池,原理如下图所示。下列有关分析正确的是( )
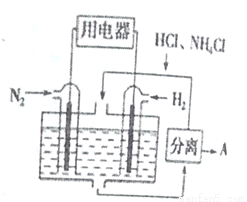
A. 通入H2—极为正极 B. 分离出的物质X为HC1
C. 电池工作一段时间后,溶液pH减小 D. 通入N2一极的电极反应式为:N2+6e-+8H+=2NH4+
科目:高中化学 来源:2017届浙江省高三3月高考模拟化学试卷(解析版) 题型:选择题
在下列分子结构中,原子的最外层电子不能满足8电子稳定结构的是( )
A. CO2 B. PCl3 C. CCl4 D. H2O
查看答案和解析>>
科目:高中化学 来源:2017届山东省泰安市高三第一轮复习质量检测(一模)理科综合化学试卷(解析版) 题型:填空题
常见的太阳能电池有单晶硅太阳能电池、多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。
(1)铜原子在基态时的价电子排布式为__________。金属铜的结构形式为面心立方最密堆积,晶胞中每个铜原子周围最近的铜原子有________个。
(2)砷、硒是第四周期的相邻元素,已知砷的第一电离能大于硒。请从原子结构的角度 加以解释_______________________。
(3)GaC13和AsF3的空间构型分别是:_________,_______。
(4)硼酸(H3BO3)本身不能电离出H+,在水中易结合一个OH-生成[B(OH)4]-,而体现弱酸性。
①[B(OH)4]-中B原子的杂化类型为____________;
②[B(OH)4]-的结构式为_________________。
(5)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅;若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)。

①金刚石、晶体硅、碳化硅的熔点由高到低的排列顺序是______________(用化学式表示);
②立方氮化硼晶体的结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5pm (1pm=10-12m)。立方氮化硼的密度是______g·cm-3(只要求列算式,不必计算出数值,阿伏加德罗常数为NA)。
查看答案和解析>>
科目:高中化学 来源:2017届湖南省邵阳市高三第二次大联考理综化学试卷(解析版) 题型:选择题
0.1mol·L-1NH4Al(SO4)2溶液的pH随温度变化的关系如曲线1所示,下列说法中正确的是
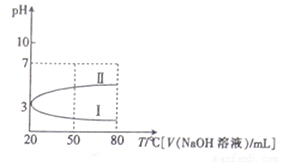
A. 0.1mol·L-1NH4Al(SO4)2溶液c(NH4+)大于等浓度的NH4HSO4溶液中c(NH4+)
B. 向100mL0.1mol·L-1NH4Al(SO4)2溶液中逐滴滴加80mL0.05 mol·L-1NaOH 溶液时,溶液pH的变化如曲线II
C. 升高温度,NH4Al(SO4)2溶液的pH减小,是因为促进了NH4Al(SO4)2的电离
D. 20℃时,0.1mol·L-1NH4Al(SO4)2溶液中:2c(SO42-)-c(NH4+)-3c(Al3+)=10-3mol·L-1
查看答案和解析>>
科目:高中化学 来源:2017届吉林省长春市高三下学期第二次质量监测理综化学试卷(解析版) 题型:简答题
人类文明的发展历程,也是化学物质的认识和发现的历程,其中铁、二氧化碳、青霉素、硝酸钾、乙醇、氨等“分子”改变过人类的世界。
(1)铁原子在基态时,外围电子排布式为____________。
(2)CO2的电子式为____________,1 mol CO2分子中含有σ键的物质的量为____________。
(3)6-氨基青霉烷酸的结构如图所示:
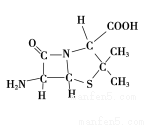
①其中C、N、O原子半径的大小关系为____________,电负性的大小关系为____________;
②其中采用sp3杂化的原子有C、____________。
(4)硝酸钾中NO3-的空间构型为____________,写出与NO3-互为等电子体的一种由前二周期元素原子构成的非极性分子化学式____________。
(5)乙醇的相对分子质量比氯乙烷小,但其沸点比氯乙烷高,其原因是____________。
(6)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,若两个最近的Fe原子间的距离为a cm,则该晶体的密度计算式为____________g/cm3(用NA表示阿伏加德罗常数)。
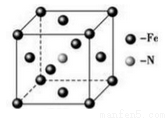
查看答案和解析>>
科目:高中化学 来源:2017届吉林省长春市高三下学期第二次质量监测理综化学试卷(解析版) 题型:选择题
化学与生产、生活、社会等密切相关,下列说法正确的是
A. 绿色化学的核心是应用化学原理对环境污染进行治理
B. 用CO2合成可降解的聚碳酸酯塑料,能减少白色污染及其危害
C. 推广使用煤的液化技术,从根本上减少二氧化碳等温室气体的排放
D. 明矾常用于水体杀菌消毒
查看答案和解析>>
科目:高中化学 来源:2017届湖南省、衡阳八中等十三校重点中学高三第一次联考化学试卷(解析版) 题型:选择题
常温下,Ksp(AgCl)=1.8×10-10, Ksp(AgI)=1.0×10-14,将等体积的AgCl和AgI的饱和溶液的清混合,再向其中加入一定量的AgNO3固体,下列说法正确的是
A. 向AgI清液中加入AgNO3,c(Ag+)增大,Ksp(AgI)也增大
B. 两清液混合,AgCl和AgI都沉淀
C. 若取0.1435gAgCl固体加入100mL水(忽略体积变化),c(Cl-)为0.01mol/L
D. 若AgNO3足量,AgCl和AgI都可沉淀,但以AgCl为主
查看答案和解析>>
科目:高中化学 来源:2017届湖南省、衡阳八中等十三校重点中学高三第一次联考化学试卷(解析版) 题型:选择题
下列化学用语表示正确的是
A. CH4分子的球棍模型:
B. 乙烯的结构简式:CH2CH2
C. N2分子的电子式: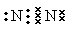
D. HOCH2COOH缩聚物的结构简式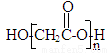
查看答案和解析>>
科目:高中化学 来源:2017届河南省安阳市高三第二次模拟考试理综化学试卷(解析版) 题型:推断题
4-氨基-3硝基苯甲醚是合成类风湿关节炎治疗药物艾拉莫德的主要原料。4-氨基-3-硝基苯甲醚的合成路线如下:
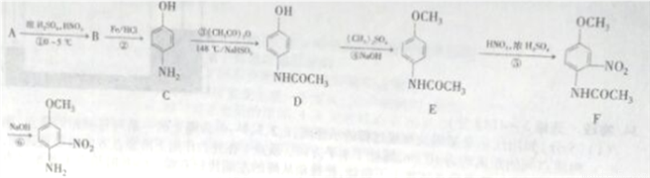
已知: NH2(有弱碱性,易被氧化)
NH2(有弱碱性,易被氧化)
回答下列问题:
(1)A的结构简式为_______________,B的名称是_______________。
(2)反应②的反应类型是____________。
(3)C中官能团的名称是_________________。
(4)写出反应③的化学方程式:________________,反应③温度较高,若不加NaHSO3会导致反应混合体系的颜色明显不同,可能的原因是________________。
(5)写出反应⑥的化学方程式:______________________。
(6)H是E的同分异构体,则满足下列条件的结构有____种(不考虑立体异构),其中核磁共振氢谱中有4组峰,且峰面积比为1:2:2:6的结构简式为_____________。
①含有 结构且能发生银镜反应
结构且能发生银镜反应
②N原子直接与苯环相连,且结构中不存在N—O键;
③苯环上有两个取代基。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com