
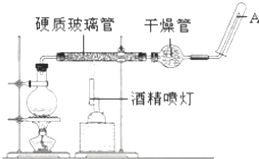
 在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.
在常温下,Fe与水并不起反应,但在高温下,Fe与水蒸气可发生反应. 应用下列装置,在硬质玻璃管中放入还原铁粉和石棉绒的混合物,加热,并通入水蒸气,就可以完成高温下“Fe与水蒸气的反应实验”.
| ||
| ||
| ||
| v |
| vm |
| 11.2L |
| 22.4L/mol |
| 8 |
| 4 |
| ||


科目:高中化学 来源: 题型:
 一带有活塞的绝热密闭容器中盛有A、B组成的混合气体,并发生如下反应:A(g)+B(g)?2C(g),在通常条件下,反应从状态Ⅰ变化到状态Ⅱ时,气体体积(V)与气体压强(p)的变化曲线如图所示.则下列说法正确的是( )
一带有活塞的绝热密闭容器中盛有A、B组成的混合气体,并发生如下反应:A(g)+B(g)?2C(g),在通常条件下,反应从状态Ⅰ变化到状态Ⅱ时,气体体积(V)与气体压强(p)的变化曲线如图所示.则下列说法正确的是( )| A、反应物具有的总能量等于生成物具有的总能量 |
| B、反应从状态Ⅰ变化到状态Ⅱ时,混合气体的平均相对分子质量减小 |
| C、反应从状态Ⅰ变化到状态Ⅱ时,反应速率一定减小 |
| D、该反应是放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、13C与C60互为同素异形体 |
| B、15N与14N互为同位素 |
| C、13C与15N有相同的中子数 |
| D、15N的核外电子数与中子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
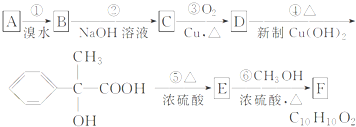
 ,满足上述条件的除A外还有
,满足上述条件的除A外还有查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

 耗NaOH溶液的体积,分别计算乙酰水杨酸的质量分数.在上述测定过程中,为防止乙酰水杨酸在滴定过程中水解,应如何正确操作?并说明理由.
耗NaOH溶液的体积,分别计算乙酰水杨酸的质量分数.在上述测定过程中,为防止乙酰水杨酸在滴定过程中水解,应如何正确操作?并说明理由.
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用10mL量筒准确量取稀硫酸溶液8.0mL |
| B、用湿润的pH试纸测定氨水的pH |
| C、实验室制备乙烯气体时,将温度计水银球置于混合溶液的液面上方 |
| D、将饱和FeCl3溶液滴入蒸馏水中即得Fe(OH)3胶体 |
| E、圆底烧瓶、锥形瓶、蒸发皿加热时都应垫石棉网. |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com