
【题目】现有一份澄清溶液, 可能含有 Na+、 K+、 NH4+、 Ca2+、 Fe3+、 SO42-、 CO32-、 SO32-、 Cl-、I-中的若干种, 且离子的物质的量浓度均为 0.1 mol·L-1(不考虑水解和水的电离)。 往该溶液中加入过量的盐酸酸化的 BaCl2 溶液, 无沉淀生成。 另取少量原溶液, 设计并完成如下实验:
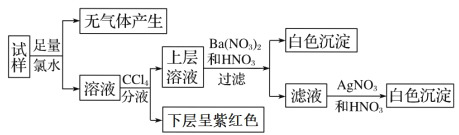
则关于原溶液的判断中不正确的是
A. 是否存在 Na+、K+需要通过焰色反应来确定
B. 通过CCl4 层的颜色变化,也能判断出原溶液中是否存在Fe3+
C. 虽然实验过程引入了氯元素, 但不影响原溶液是否存在Cl-的判断
D. 肯定不存在的离子是 Ca2+、Fe3+、SO42-、CO32-、Cl-
【答案】A
【解析】试样加足量的Cl2水,没有气体产生,说明无CO32-,溶液加四氯化碳分层,下层为紫红色,说明有I-无Fe3+,因为两者不能共存。上层加硝酸钡和稀硝酸,有白色沉淀产生,说明可能是SO42-、 SO32-或单一一个。根据往该溶液中加入过量的盐酸酸化的 BaCl2 溶液, 无沉淀生成,说明原溶液无SO42-,一定有SO32-,根据离子共存,溶液中无Ca2+存在,滤液加硝酸银和硝酸,不能确定是否含有Cl-。A. 是否存在 Na+、K+需要通过焰色反应来确定正确,故A对,B. 通过CCl4 层的颜色变化,也能判断出原溶液中是否存在Fe3+正确,故B对;C. 虽然实验过程引入了氯元素, 但不影响原溶液是否存在Cl-的判断,错误,故C错;D. 肯定不存在的离子是 Ca2+、Fe3+、SO42-、CO32-、Cl-错误,因为不能确定是否存在Cl-,故D错。答案;C D。


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:
【题目】实验室制备无水乙醇常用蒸馏法,实验步骤如下:
I.回流:在l00mL圆底烧瓶中加入l0g小颗粒状的生石灰和几颗氢氧化钠,慢慢注入50mL工业乙醇,回流1h。
Ⅱ.蒸馏:回流毕,待烧瓶冷却后在烧瓶中加入几粒沸石,改为蒸馏装置,收集78C时的馏分,即为无水乙醇。回流和蒸馏装置如下图(用△表示酒精灯):

回答下面问题:
(1)装置b的名称是________ 。
(2)简述向烧瓶中加入生石灰的方法_____________
(3)加入NaOH固体是为了除去工业乙醇中少量的醛,发生的关键反应为CH3CHO+CH3CHO![]() CH3CH(OH)CH2CHO,该反应的反应类型为____,回流1h的目的是___ 。
CH3CH(OH)CH2CHO,该反应的反应类型为____,回流1h的目的是___ 。
(4)蒸馏时,先____,后____(①点燃酒精灯②接通冷凝水,填代号),待温度计指示为78℃左右时,尾接管中出现液滴,弃去开始流出的液体,原因是____。
(5)有同学建议改蒸馏为过滤,请回答过滤法不妥的原因 ___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究金属单质M与盐溶液的反应,某同学进行了下列实验,实验过程及现象如图所示,结合实验现象判断该同学得出的下列结论中正确的是
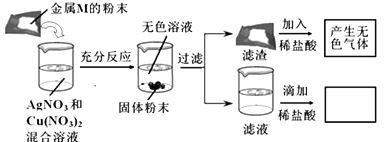
A. 向滤液中滴加盐酸的实验现象是产生白色沉淀
B. 滤渣可能是两种单质的混合物
C. 滤渣在足量的稀硝酸中能完全溶解
D. 加入的金属M可能是镁或钠
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向下列各溶液中通入足量CO2气体,最终有浑浊现象产生的是
①饱和Na2CO3溶液 ②澄清石灰水 ③NaAlO2溶液
④CaCl2溶液 ⑤Na2SiO3溶液
A. 全部 B. 除①④⑤外
C. 除①②④外 D. 除②④外
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl- 六种粒子。其中N2的物质的量随时间变化的曲线如图所示。下列判断正确的是
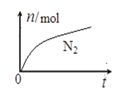
A. 该反应的还原剂是Cl-
B. 消耗1 mol还原剂,转移6 mol电子
C. 氧化剂与还原剂的物质的量之比为2:3
D. 反应后溶液的酸性明显增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某燃煤发电厂处理废气的装置示意图.下列说法正确的是( )

A. 此过程中没有分解反应
B. 整个过程的反应可表示为: 2SO2+2CaCO3+O2═2CaSO4+2CO2
C. 使用此废气处理装置可减少CO2的排放
D. 此过程中S元素的化合价未发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于NO的下列叙述中不正确的是
A.在放电条件下,N2和O2可直接化合生成NOB.NO气体难溶于水
C.打开盛NO气体的瓶盖,立即看到瓶口有红棕色气体生成D.NO是红棕色气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同周期的X、Y、Z三种元素的最高价氧化物对应水化物分别是:H3XO4、H2YO4、HZO4,下列判断正确的是( )
①阴离子的还原性按X、Y、Z顺序减弱 ②单质的氧化性按X、Y、Z顺序增强
③元素的原子半径按X、Y、Z顺序减小 ④气态氢化物的稳定性按X、Y、Z顺序减弱
⑤酸性由强到弱的顺序是:HZO4![]() H2YO4
H2YO4![]() H3XO4
H3XO4
A. ①②B. ②③⑤C. ①②③⑤D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁铝合金溶于适量盐酸后,再加入过量的氢氧化钠溶液,过滤,滤液中可能大量共存的离子是( )
A.Na+ Mg2+ Al3+ Cl-B.Na+ AlO2- Cl- OH-
C.Na+ Mg2+ AlO2- Cl-D.Na+ Al3+ AlO2- Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com