
(1)X元素位于周期表中第__________族(用字母表示)。
(2)X、Y、Z三种元素形成的单质中,氧化性最弱的是_____________(填化学式)。
(3)Y与Z可形成共价化合物Y2Z2,分子中Y与Z均满足8电子稳定结构,则Y2Z2的电子式为_____________。
(4)a溶液的pH_____________7(填“>”“<”或“=”),用离子方程式解释为_____________,若在a溶液中加入少量镁粉,可观察到的现象是_____________。
(5)取pH=0的W的最高价氧化物对应水化物的溶液100.0 mL于某容器中,加入
若设Cu、Ag的物质的量分别为x、y。欲求算x、y的值,可列出下列计算式:
Ⅰ.64x+108y=0.90,该计算式是依据________________________关系列出的;
Ⅱ.2x+y=1 mol·L -1×
解析:W元素的氢化物与Z元素的氢化物反应只生成一种盐a,可考虑氨气与氯化氢反应生成氯化铵,W元素为N,Z元素为Cl,前者在ⅤA族,后者在ⅦA族,X、Y位于同一族,可考虑ⅥA族,即可推断出W、X、Y、Z四种短周期元素分别为N、O、S、Cl。
(1)O元素位于周期表中第ⅥA族。
(2)O、S、Cl三种元素形成的单质中,氧化性最弱的是S。
(3)S与Cl可形成共价化合物S2Cl2,分子中S与Cl均满足8电子稳定结构,结构式必为Cl—S—S—Cl,电子式略。
(4)a溶液为氯化铵溶液,水解显酸性,pH<7,原因是:![]() +H2O
+H2O![]() NH3·H2O+H+;若在氯化铵溶液中加入少量镁粉,镁粉与氢离子反应现象为镁粉逐渐溶解,并放出无色气泡。
NH3·H2O+H+;若在氯化铵溶液中加入少量镁粉,镁粉与氢离子反应现象为镁粉逐渐溶解,并放出无色气泡。
(5)由题意知:合金总质量为
答案:(1)ⅥA
(2)S
(3)![]()
(4)< ![]() +H2O
+H2O![]() NH3·H2O+H+ 镁粉逐渐溶解,且有气泡产生
NH3·H2O+H+ 镁粉逐渐溶解,且有气泡产生
(5)金属质量(或质量) W元素(或N元素或原子)


科目:高中化学 来源: 题型:
| 1 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
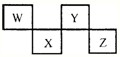 W、X、Y、Z四种短周期元素在元素周期表中的位置如图所示,其中Z位于ⅦA族.请回答下列问题.
W、X、Y、Z四种短周期元素在元素周期表中的位置如图所示,其中Z位于ⅦA族.请回答下列问题.
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| W | X | |
| Y | Z |
| A、原子半径大小:W>X |
| B、元素最高正价:W>Z |
| C、简单阴离子的还原性:Y>Z |
| D、气态氢化物的稳定性:X>Y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com