
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源: 题型:
| 放电 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 放电 | 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| Y | |||
| R | Q |
| ||
| ||

查看答案和解析>>
科目:高中化学 来源: 题型:
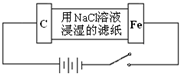 某同学设计一个如图所示(用铅蓄电池做电源)的电化学实验.下列说法正确的是( )
某同学设计一个如图所示(用铅蓄电池做电源)的电化学实验.下列说法正确的是( )| A、电解池的阳极电极反应式:Fe-2e-?Fe2+ | B、电解池的阴极电极反应式:2H++2e-?H2↑ | C、铅蓄电池的负极的电极反应式:PbO2+4H++SO42-+2e-?PbSO4+2H2O | D、铅蓄电池的负极的电极反应式:Pb-2e-?Pb2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com