
【题目】下列变化不需要破坏化学键的是( )
A.加热氯化铵B.冰融化成水
C.水通电分解D.氯化氢溶于水
科目:高中化学 来源: 题型:
【题目】烃A在一定条件下可以转化为有机物E,其转化关系如下图。已知烃A在标准状况下的密度为116g/L,加热时B与新制氢氧化铜产生砖红色沉淀,E为有浓郁香味、不易溶于水的油状液体。
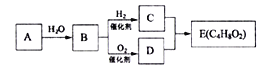
请回答:
(1)B中官能团的结构简式为_________________________。
(2)C+D→E的化学方程式为___________________________________。
(3)下列说法正确的是______
a.C物质与金属钠反应比水与金属钠反应更剧烈
b.有机物C、D、E可用饱和Na2CO3溶液鉴别
c.实验室制备E时,加入浓盐酸做催化剂
d.B能被酸性KMnO4溶液氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】盐酸埃克替尼片又名凯美纳是我国自主研发的治疗肺癌良药,以下是制备盐酸埃克替尼的其中一条合成路线:
(已知: 结构片段可以简写为
结构片段可以简写为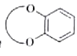 )
)
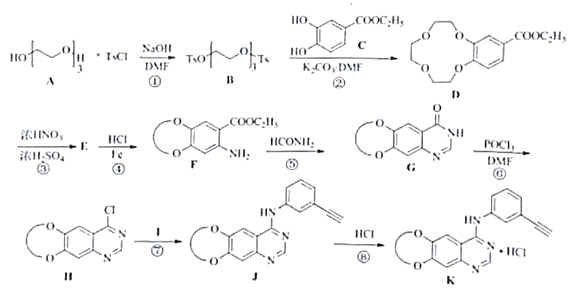
(1)化众物F中含氧官能团名称是_______,________。
(2)反应①⑦的反应类型分别是_________,_________。
(3)化合物Ⅰ的结构简式为_________。
(4)反应③的化学方程式为_________
(5)化介物M是化合物C的同系物,分子式为C8H5O4,其同分异构体有多种,其中同时满足下列三个条件的同分异构体有____种。
①能发生银镜反应
②不含醇羟基
③含有的官能团数目、种类及苯环上取代基数目与化合物C都完全相同。
其中核磁共振氢谱上显示苯环上只有2组峰,峰面积比例为1:2的同分异构体的结构简式为__________。
(6)三缩乙二醇(A)可以由三分子乙二醇在浓硫酸加热条件下缩合得到。请从最简单的烯烃出发,经三步合成三缩乙二醇,请完成合成路线。______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“一带一路”为中国化工企业开辟了新的国际市场,而能源、资源整合及环境治理是保驾护航的基础。
Ⅰ.在能源领域,科学家提出“绿色自由“”构想: 把含有大量CO2的空气吹入K2CO3溶液中,再把CO2从溶液中提取出来,并使之与H2反应生成可再生能源甲醇。其工艺流程如下图所示:
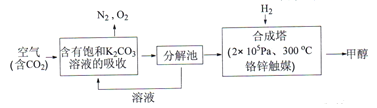
(1)在合成塔中,若有4400gCO2与足量H2完企反应,生成气态的H2O和气态甲醇,可放出5370kJ的热量,写出该反应的热化学方程式__________。
(2)一定条件下,向2L恒容密闭容器中充入1molCO2和3molH2,在不同催化剂作用下发生反应Ⅰ、反应Ⅱ与反应Ⅲ,相同时间内CO2的转化率随温度变化如下图所示:
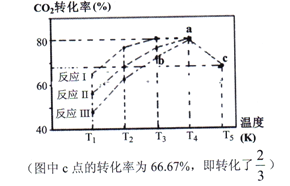
①催化剂效果最佳的反应是__________(填“反应I”,“反应II”,“反应III”)。
②b点v (正)______ v (逆)(填 “>”, “<”, “=”)。
③c点时该反应的平衡常数K =_________。(写单位)
Ⅱ.环境治理中,安装汽车尾气催化转化器的反应是:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g)ΔH<0
2CO2(g)+N2(g)ΔH<0
(3)温度升高K值_______(填“增大”或“减小”)
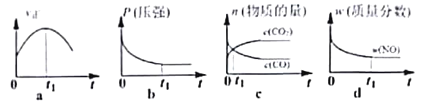
(4)若反应在恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是____________。
(5)下列所示装置可以在吸收SO2的同时,用阴极排出的溶液吸收NO2,(电极均为惰性电极)
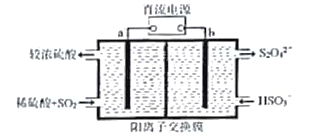
a极为______极(填“阴”、“阳”),b极的电极反应式为_________,结合电极反应式简述该装置能吸收SO2的原理:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质在一定条件下反应,可以制得较纯净的 1,2-二氯乙烷的是( )
A.乙烷与氯气在光照条件下反应B.乙烯与氯化氢气体混合
C.乙烯与氯气混合D.乙烯通入浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行实验,正确的是
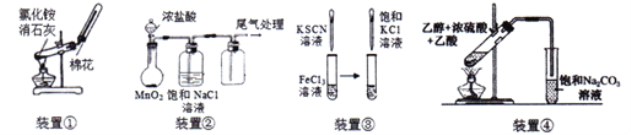
A. 用图①装置制取并收集氨气
B. 用图②装置制取和收集纯净的Cl2
C. 用图③装置可以看到试管内液体变为红色,滴加KCl溶液后颜色加深
D. 用图④装置制取乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为________________;
(2)从开始至2min,B的平均反应速率为_______________;平衡时,C的浓度为_____________ ,A的转化率为________________;
(3)反应达平衡时体系的压强是开始时的________________倍;
(4)下列叙述能说明该反应已达到化学平衡状态的是(填标号)________________;
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.相同时间内消耗3n molA,同时消耗n mol的B
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
(5)在某一时刻采取下列措施能使该反应速率减小的是______________。
A.加催化剂 B.降低温度
C.体积不变,充入A D.体积不变,从容器中分离出A
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常工业上监测SO2含量是否达到排放标准的化学反应原理是SO2+H2O2+BaCl2=BaSO4↓+2HCl,用NA表示阿伏伽德罗常数的值,下列说法不正确的是
A. 0.1 mol BaCl2中所含离子总数为0.3 NA
B. 25℃时,0.1mol/L的HCl溶液中含有H+的数目为0.1 NA
C. 标准状况下,17 g H2O2中所含分子总数为0.5 NA
D. 生成2.33 g BaSO4沉淀时,吸收SO2的体积在标准状况下约为0.224 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酒精和醋酸是生活里的常用品,下列方法不能将二者鉴别开的是( )
A.闻气味
B.分别用来浸泡水壶中的水垢看是否溶解
C.分别滴加NaOH溶液
D.分别滴加石蕊试液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com