
【题目】一种比黄金贵百倍的18O2气体,不久前在兰州近代物理研究所研究成功。1mol这种18O2气体中含中子的物质的量为( )
A. 10mol B. 16mol C. 20mol D. 36mol
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】W是由A、B两种元素组成的AB2型化合物。
(1)若W和焦炭在高温下发生反应,所制得的半导体材料应用广泛。则W为________(填化学式)。
(2)若取两支试管分别加入少量W溶液,往一支试管中滴入KSCN溶液,无明显现象。往另一支试管中加入足量氯水,再加入适量CCl4,振荡,静置,下层溶液呈紫红色;往上层溶液中滴入KSCN溶液,溶液呈红色。
①W溶液中所含金属阳离子为________。
②上述实验中,W与足量氯水反应的离子方程式为_____________________。
(3)若W是离子化合物,其阴、阳离子均含18个电子,且阴、阳离子个数比为1∶1。
①阴离子的电子式为________。
②1 mol W与足量水充分反应,转移电子的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中p表示压强,t表示温度,n表示物质的量):
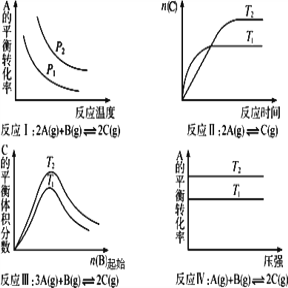
根据图像判断,下列结论正确的是( )
A. 反应Ⅰ△H> 0,P2>P1 B. 反应Ⅱ△H<0,T1>T2
C. 反应Ⅲ一定是△H> 0,T2>T1 D. 反应Ⅳ△H<0,T2>T1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合图判断,下列叙述正确的是

A. I和II中正极均被保护
B. I和II中负极反应均是Fe-2e-=Fe2+
C. I和II中正极反应均是O2+2H2O+4e-=4OH-
D. I和II中分别加入少量氯水和KSCN溶液均变红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一容积不变的密闭容器中充入一定量A和B,发生如下反应:xA(g)+yB(s) ![]() zC(g) ΔH<0。反应中A和B消耗的物质的量相同,在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答下列问题:
zC(g) ΔH<0。反应中A和B消耗的物质的量相同,在一定条件下,容器中A、C的物质的量浓度随时间变化的曲线如图所示。请回答下列问题:

(1)根据图示可确定x∶y∶z=__________________________。(用最简整数比表示)
(2)0~10 min容器内压强______________(填“变大”、“不变”或“变小”)。
(3)推测第10 min引起曲线变化的反应条件可能是________;第16 min引起曲线变化的反应条件可能是________。(选填数字编号)
①减压 ②增大A的浓度 ③增大C的量 ④升温 ⑤降温 ⑥加催化剂
(4)平衡Ⅰ的平衡常数为K1=___________,平衡Ⅱ平衡常数为K2,则K1________K2(填“>”、“=”或“<”)。
(5)在平衡I的温度下,假设容积恒定为1L,下列措施中能使平衡时 n(A)/n(C)增大的有___________(选填字母编号)
A.升高温度 B.充入氦气 C.再充入0.2molA和0.5molC D.使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,浓度均为1.0mol/L的HX溶液、HY溶液,分别加水稀释.稀释后溶液的pH随浓度的变化如图所示,下列叙述正确的是
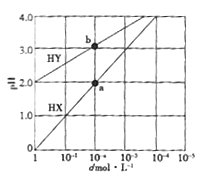
A. HX是强酸,溶液每稀释10倍.pH始终增大l
B. 常温下HY的电离常数为1.0×10-4
C. 溶液中水的电离程度:a 点大于b 点
D. 消耗同浓度的NaOH溶液体积:a 点大于b 点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳的回收利用是环保领域研究热点。
(l)在太阳能的作用下,以CO2为原料制取炭黑的流程如图所示,总反应的化学方程式为_________。
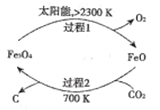
(2)工业上可用CO2和H2反应制得甲醇。在2×105Pa、300℃的条件下,CO2和H2反应生成甲醇和液态水,当消耗2molCO2时放出98kJ的热量,该反应的热化学方程式为___________。
(3)如利用CO2和CH4重整可制合成气(主要成分为CO、H2), 其原理为:CO2(g)+CH4(g)![]() 2CO(g)+2H2(g)。在密闭容器中通入物质的量均为1mol的CH4和CO2,在一定条件下发生反应。CH4的平衡转化率与温度及压强(单位Pa)的关系如图所示:
2CO(g)+2H2(g)。在密闭容器中通入物质的量均为1mol的CH4和CO2,在一定条件下发生反应。CH4的平衡转化率与温度及压强(单位Pa)的关系如图所示:
①压强:P1_____P2(填“>”、“=”或“<”,下同) , y点:V正_______V逆。
②已知气体分压(P分)=气体总压(P总)×气体的体积分数。用气体分压代替平衡浓度可以得到平衡常数KP,求X点对应温度下反应的平衡常数KP=________。

(4)Na2CO3溶液也通常用来捕获CO2,发生如下反应:CO32-+CO2+H2O![]() 2HCO3-,用0.12mol/LNa2CO3溶液若吸收CO2一段时间后,溶液的pH=7,溶液中c(HCO3-)/c(CO32-)=10,则溶液中的c(CO32-) =__________。
2HCO3-,用0.12mol/LNa2CO3溶液若吸收CO2一段时间后,溶液的pH=7,溶液中c(HCO3-)/c(CO32-)=10,则溶液中的c(CO32-) =__________。
(5)甲醇燃料电池(简称DMFC)可作为常规能源的替代品而备受关注。DMFC的工作原理如图所示:
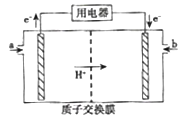
①加入a物质的电极是电池的______(填“正”或“负”)极,其电极反应式为_______。
②常温下以该装置作电源,用情性电极电解NaCl和CuSO4的混合溶液,当电路中通过0.4 mol 电子的电量时,两电极均得到0.14mol的气体。若电解后溶液体积为40L,则电解后溶液的pH=_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种金属A与B和稀硫酸组成原电池时,A是正极。下列有关推断正确的是( )
A. A的金属性强于B
B. 电子不断由A电极经外电路流向B电极
C. A电极上发生的电极反应是还原反应
D. A的金属活动性一定排在氢前面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com