
下列说法正确的是( )
A. 手机外壳上贴的碳纤维外膜是一种新型的有机高分子材料
B. 绿色化学的核心是对环境产生的污染进行治理
C. 氯化铵、二氧化硫溶于水都能导电,所以它们都属于电解质
D. 云、烟、雾等均能产生丁达尔现象
科目:高中化学 来源:2016-2017学年河北省石家庄市高一上学期期末考试化学试卷(解析版) 题型:选择题
取3.38g K2CO3和KHCO3的混合物溶于水配成25 mL溶液,往溶液中加入25 mL Ba(OH)2溶液恰好使生成白色沉淀的量最多。反应后溶液的c(OH-)=0.8mol/L(忽略混合后溶液体积变化)。则原混合物中K2CO3和KHCO3物质的量之比为
A. 1:2 B. 1:1 C. 2:1 D. 2:3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高一上学期期末考试化学试卷(解析版) 题型:选择题
KClO3与浓盐酸发生如下反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,有关该反应,说法不正确的是
A. 被氧化的元素和被还原的元素的质量之比5:1
B. Cl2既是氧化产物,又是还原产物
C. 盐酸既体现酸性,又体现还原性
D. 转移5mol电子时,产生67.2L的Cl2
查看答案和解析>>
科目:高中化学 来源:2017届福建省漳州市八校高三上学期期末联考化学试卷(解析版) 题型:选择题
25℃时,部分弱酸的电离平衡常数如表:
弱酸 | CH3COOH | HCN | H2CO3 |
电离平衡常数 | 1.8×10﹣5 | 4.9×10﹣10 | K1=4.3×10﹣7 K2=5.6×10﹣11 |
下列有关说法正确的是( )
A. 等物质的量浓度溶液的pH关系为pH(NaCN)>pH(Na2CO3)>pH(CH3COONa)
B. a mol•L﹣1HCN溶液与b mol•L﹣1NaOH溶液等体积混合后,所得溶液中:c(Na+)>c(CN﹣),则a一定小于b
C. 往冰醋酸中逐滴加水,溶液的导电性逐渐增大
D. 将0.2 mol•L﹣1 KHCO3溶液与0.1 mol•L﹣1 KOH溶液等体积混合:c(K+)+c(H+)=c(OH﹣)+c(HCO3-)+2c(CO32-)
查看答案和解析>>
科目:高中化学 来源:2017届福建省漳州市八校高三上学期期末联考化学试卷(解析版) 题型:选择题
俗称“一滴香”的有毒物质被人食用后会损伤肝脏,还能致癌.“一滴香”的分子结构如图所示,下列说法正确的是( )

A. 该有机物的分子式为C7H7O3
B. 该有机物能发生取代、加成和氧化反应
C. 1mol该有机物最多能与2mol H2发生加成反应
D. 该有机物的一种含苯环的同分异构体能发生银镜反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二下学期开学考试化学试卷(解析版) 题型:填空题
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂,目前已开发出用电解法制取ClO2的新工艺.
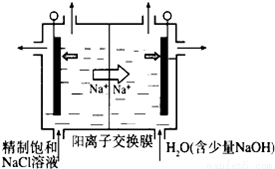
(1)①如图示意用石墨做电极,在一定条件下电解饱和食盐水制取ClO2。写出阳极产生ClO2的电极反应式:__________________.
②电解一段时间,当阴极产生的气体体积为112mL(标准状况)时,停止电解.通过阳离子交换膜的阳离子的物质的量为____mol;用平衡移动原理解释阴极区pH增大的原因___________。
(2)ClO2对污水中Fe2+、Mn2+、S2-和CN-等有明显的去除效果.某工厂污水中含CN-amg/L,现用ClO2将CN-氧化,只生成两种气体,其离子反应方程式为______;处理100m3这种污水,至少需要ClO2______mol.
(3)为提高甲醇燃料的利用率,科学家发明了一种燃料电池,电池的一个电极通入空气,另一个电极通入甲醇气体,电解质是掺入了Y2O3的ZrO2晶体,在高温下它能传导O2-。电池工作时正极反应式为_________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二下学期开学考试化学试卷(解析版) 题型:选择题
分别在等体积等pH或等物质的量浓度的盐酸和醋酸溶液中,加入足量锌粉,氢离子浓度c(H+)及氢气的体积V(H2)(同温同压下测定)的变化图示如下,其中正确的是 ( )
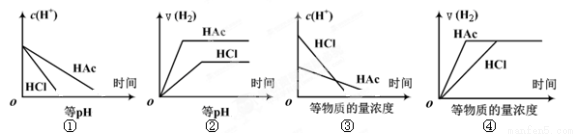
A. ①②③ B. ②④ C. ①③ D. ①②③④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高二上学期期末考试化学试卷(解析版) 题型:选择题
固体氧化物燃料电池(SOFC)以固体氧化物作为电解质,其工作原理如下图所示。下列关于固体
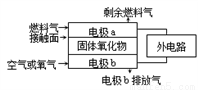
燃料电池的有关说法中正确的是
A. 固体氧化物的作用是让电子在电池内通过
B. 固体氧化物中O2-从a极向b极移动
C. 电极b为电池的负极,电极反应式为:O2 + 4e- = 2O2-
D. 若以C3H8为燃料气,则接触面上发生的反应为C3H8 – 20e- + 10O2- =3CO2 +4H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省天水市高二下学期开学考试(寒假作业检测)化学试卷(解析版) 题型:简答题
实现 “节能减排” 和“低碳经济”的一项重要课题就是如何将CO2转化为可利用的资源。目前工业上有一种方法是用CO2来生产燃料甲醇。一定条件下发生反应:
CO2(g)+3H2(g)  CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:
CH3OH(g)+H2O(g),下图1表示该反应过程中能量(单位为kJ·mol-1)的变化:

(1)关于该反应的下列说法中,正确的是____________(填字母)。
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)为探究反应原理,现进行如下实验,在体积为l L的密闭容器中,充入l mol CO2和4mol H2,一定条件下发生反应:CO2(g)+3H2(g)  CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
CH3OH(g)+H2O(g),测得CO2和CH3OH(g)的浓度随时间变化如上图2所示。
①从反应开始到平衡,CO2的平均反应速率v(CO2)=_________;
②下列措施中能使化学平衡向正反应方向移动的是___________(填字母)。
A.升高温度B.将CH3OH(g)及时液化抽出C.选择高效催化剂D.再充入l molCO2和4 molH2
(3)25℃,1.01×105Pa时,16g 液态甲醇完全燃烧,当恢复到原状态时,放出363.3kJ的热量,写出该反应的热化学方程式:_____________。
(4)选用合适的合金为电极,以氢氧化钠、甲醇、水、氧气为原料,可以制成一种以甲醇为原料的燃料电池,此电池的负极的电极反应式是:______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com