
汽车尾气的主要成分有CO、SO2、氮氧化物等,科研工作者目前正在尝试以二氧化钛(TiO2)催化分解汽车尾气的研究。
(1)已知:2NO(g)+O2(g)=2NO2(g) ΔH1=-113.0KJ/mol
2SO2(g)+O2(g)=2SO3(1) ΔH2=-288.4KJ/mol
请判断反应NO2(g)+SO2(g)=NO(g)+SO3(1) ΔH3,在低温下能否自发进行,并说明理由_________。
(2)已知TiO2催化尾气降解原理为:
2CO(g)+O2(g)  2CO2(g);
2CO2(g);
2H2O(g)+4NO(g)+O2(g)  4HNO3(g)。
4HNO3(g)。
Ⅰ.在O2浓度几乎不变的条件下,模拟CO、NO的降解,得到降解率随时间变化如图1所示( ),反应40秒后检测气体浓度有所降低,请用化学方程式结合化学反应原理知识解释出现该现象可能的原因______________。
),反应40秒后检测气体浓度有所降低,请用化学方程式结合化学反应原理知识解释出现该现象可能的原因______________。

Ⅱ.图2为在不同颗粒间隙的沥青混凝土(α、β型)和不同温度下,实验进行相同一段时间(t秒)后测得的CO降解率变化,回答谢列问题:
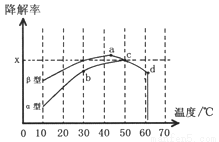
①已知50℃、t秒时容器中O2浓度为0.01mol/L,求此温度下CO降解反应的平衡常数_______。
②下列关于图2的叙述不正确的是_______
A.根据降解率由b点到c点随温度的升高而增大,可知CO降解反应的平衡常数Kb<Kc
B.相同温度下β型沥青混凝土中CO降解速率比α型要大
C.a点的数据反映出CO与O2之间所发生的有效碰撞频率是整个实验过程中最高的
D.d点降解率出现突变的原因可能是温度升高后催化剂失效
③科研团队以β型沥青混凝土颗粒为载体,将TiO2改为催化效果更好的TiO2纳米管,在10-60℃范围内进行实验,请在图2中用线段与阴影仿照“示例”描绘出CO降解率随温度变化的曲线可能出现的最大区域范围(示例: )。_______
)。_______
(3)TiO2纳米管的制备是在弱酸性水溶液中以金属钛为阳极进行电解,写出阳极的电极反应式________。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2016-2017学年河北省张家口市高二上学期期末考试化学试卷(解析版) 题型:选择题
已知:
化学键 | C—H | C—F | H—F | F—F |
键能 | 414 | 489 | 565 | 158 |
CH4(g)+4F2(g)=CF4(g)+4HF(g) ΔH=akJ·mol-1。则a等于
A. -1928 B. +1928 C. +1838 D. -1838
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省大连市高二上学期期末考试(文)化学试卷(解析版) 题型:选择题
下列四支试管中,过氧化氢分解的化学反应速率最大的是
试管 | 温度 | 过氧化氢溶液的浓度 | 催化剂 |
A | 室温(25℃) | 12% | 有 |
B | 水浴加热(50℃) | 8% | 有 |
C | 水浴加热(50℃) | 12% | 有 |
D | 室温(25℃) | 8% | 无 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届山西省名校高三下学期联考理综化学试卷(解析版) 题型:简答题
人口资源环境委员会副主任、中国科学院院士秦大河表示,当前情况下散烧煤和没有清洁的煤是造成中国城市雾霾或者东部雾霾的主要原因。煤的气化是解决雾霾,清洁地利用煤炭的重要途径之一。
⑴已知:H2O(g)=H2O(I) △H=-44kJ/mol
物质 | H2(g) | C(s) | CO(g) |
燃烧热kJ/mol | -285.8 | -393.5 | -283.0 |
①请写出煤的气化反应生成合成气(CO和H2)的热化学方程式___________。
②在恒温、恒容的反应器中,能表明上述反应达到平衡状态的是_______。
a.混合气体平均相对分子质量不再改变
b.气体压强不再改变
c.各气体浓度相等
d.反应体系中温度保持不变
e.断裂氢氧键速率是断裂氢氢键速率的2倍
f.混合气体密度不变
g.单位时间内,消耗水的质量与生成氢气的质量比为9:1
⑵在催化剂作用下合成气合成甲烷过程中会发生如下反应:
I CO(g)+3H2(g) = CH4(g)+H2O(g) △H1= -206 kJ/mol
II CO(g)+H2O(g) = CO2(g)+H2(g) △H2= -41 kJ/mol
Ⅲ 2CO(g)+2H2(g)= CH4(g)+CO2(g) △H 3= -247.4 kJ/mol
①图1是太原理工大学煤化工研究所利用热力学数据分析得到温度对反应ⅠInK(化学平衡常数K的自然对数)的曲线图,请分析出现这样趋势的原因是____________。
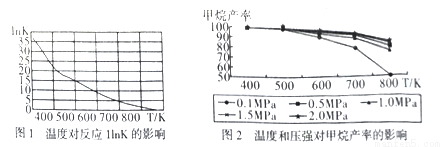
②提高甲烷反应选择性的关键因素是_______,根据相关知识和图2分析合成甲烷适宜的反应条件是
在550~630K,1MPa的原因是__________________。
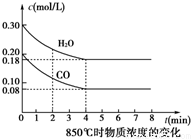
③850℃时在体积为5L反应器中发生反应Ⅱ,CO和H2O(g)浓度变化如图所示,请列式计算此条件下的平衡常数_____________ 。
(3)CH4燃料电池利用率很高,装置中添加1L2mol/L的KOH溶液为电解质,持续缓慢通入标准状况下甲烷22.4L~33.6 L时负极电极反应为___________。
查看答案和解析>>
科目:高中化学 来源:2017届山西省名校高三下学期联考理综化学试卷(解析版) 题型:选择题
下列选项中陈述Ⅰ和陈述Ⅱ均正确,且陈述Ⅰ和陈述Ⅱ有因果关系的是
选项 | 陈述Ⅰ | 陈述Ⅱ |
A | 浓硫酸具有脱水性 | 少量胆矾放入适量浓硫酸中,固体变为白色 |
B | 氮元素的非金属性强于碳元素 | 酸性:HNO3>H2CO3 |
C | NaHCO3溶液呈碱性 | NaHCO3可用作发酵粉 |
D | 通过煤的干馏和分馏可分离获得苯和甲苯 | 煤中含有苯和甲苯 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:浙江省台州市2017届高三2月选考科目教学质量评估测试化学试卷 题型:选择题
已知还原性:SO32->I-。某溶液X可能含有NH4+、Na+、Ba2+、Fe3+、I-、SO32-、SO42-中的几种,为确定其组成,某同学进行如下实验:
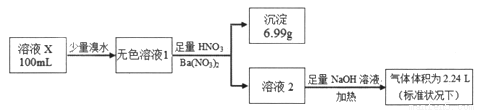
下列说法正确的是
A. 溶液X肯定只存在NH4+、SO42-
B. 溶液X一定不含有Ba2+、Fe3+,可能含有I-
C. 为确定可能存在的阴离子,可另取试液滴加足量盐酸、BaCl2溶液
D. 为确定可能存在的阳离子,可用经过稀硫酸洗过的铂丝蘸取溶液X在酒精灯火焰上灼烧
查看答案和解析>>
科目:高中化学 来源:浙江省台州市2017届高三2月选考科目教学质量评估测试化学试卷 题型:选择题
下列说法不正确的是
A. NH4Cl溶液呈酸性说明NH3·H2O是弱电解质
B. 醋酸钠溶液中c(Na+)>c(CH3COO-)
C. 常温下相同pH的NaOH溶液和CH3COONa溶液中水电离出的OH-浓度相同
D. 常温下,在1mol·L-1的盐酸中加入等体积等浓度的氨水,溶液导电能力减弱
查看答案和解析>>
科目:高中化学 来源:浙江省台州市2017届高三2月选考科目教学质量评估测试化学试卷 题型:选择题
下列物质属于碱性氧化物的是
A. SiO2 B. CaO C. CO D. NaOH
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二下学期基础训练(15)化学试卷(解析版) 题型:选择题
某溶液可能含Cl-、CO32-、SO42-、Na+,现取少量溶液滴入硝酸酸化,无明显现象,再滴入氯化钡溶液,有白色沉淀生成,取上层清液滴加硝酸银溶液,产生白色沉淀。下列判断不合理的是
A. 一定有Cl- B. 一定有Na+
C. 一定无CO32- D. 一定有SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com