
从100 mL 0.1 mol / L的AlCl3溶液中取出50 mL,其中Cl-的物质的量浓度是高考资源网
A.0.3 mol / L B.0. 5 mol / L 高考资源网
C.0.1 mol / L D.0.15 mol / L高考资源网
科目:高中化学 来源: 题型:阅读理解
一般测定样品中成分含量的实验应重复2—3次。为了测定某氢氧化钠固体中混有的碳酸钠的质量分数,甲、乙、丙三位同学分别设计了如下实验方案:
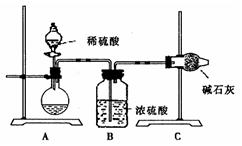
Ⅰ.甲同学的方案如上图所示:
(1)根据甲同学的实验装置图分析,在每次实验过程中所进行的称量操作至少要进行 次;如何来检验A装置的气密性?
。
(2)甲同学重复进行了三次实验,得到碳酸钠的质量分数的数据存在较大的偏差,你认为可能引起测量结果偏低的原因是 (填序号)。
A.装置内原有空气中的二氧化碳气体也被碱石灰吸收;
B.装置外空气中的水蒸气和二氧化碳被碱石灰吸收;
C.反应完成后,装置中的二氧化碳没有全部被碱石灰吸收;
D.加入稀硫酸的量不足反应不充分
(3)为了让甲的实验测量结果更准确,在其他实验步骤都正确下,你认为图中的实验装置应该如何改进实验装置:
Ⅱ.乙同学的方案是:从下图所提供的装置中选择实验装置,代替甲同学实验的B、C,通过测定放出的二氧化碳的体积(不考虑二氧化碳溶于水)来计算。
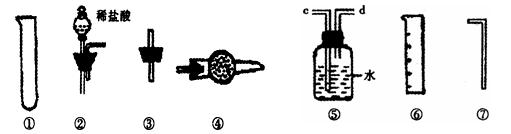
选择最简装置的连接顺序为 ;
Ⅲ.丙同学的方案是:称取样品m g,并溶解,加入过量氯化钡溶液,过滤、洗涤、烘干、称量,得固体n g。
(1)配制100 mL 0.10 mol·L-1 BaCl2溶液及过滤实验中所需的玻璃仪器除烧杯、玻璃棒、胶头滴管、量筒外还有_______________________________(填仪器名称);
(2)混合物中碳酸钠的质量分数为(用m、n表示) 。
(3)Ca2+、Ba2+都可以使CO32-沉淀完全。能否使用氯化钙溶液代替氯化钡溶液?为什么?
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)(2011·济南一模)海水中蕴藏着丰富的资源,人类需要的很多材料都来源于海水的综合利用。
(1)工业上用NaCl制备金属钠的化学方程式是____________________________________
________________________________________________________________________。
(2)实验室用惰性电极电解100 mL 0.1 mol·L-1NaCl溶液,若阴阳两极均得到112 mL气体(标准状况),则所得溶液的pH为________(忽略反应前后溶液的体积变化)。
(3)电解氯化钠溶液可制备“84消毒液”(主要成分是次氯酸钠),通电时氯气被溶液完全吸收。假设所得的消毒液仅含一种溶质,请写出相应的总化学方程式________________________________________________________________________。
(4)该小组同学认为,如果模拟工业上离子交换膜法制烧碱的方法,可以设想用如图装置电解硫酸钾溶液来制取氢气、氧气、硫酸和氢氧化钾。
①该电解槽的阳极反应式为:_______________________________________________;
通过阴离子交换膜的离子数________(填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数。
②制得的氢氧化钾溶液从出口(填写“A”、“B”、“C”或“D”)________导出。
③请简述通电开始后,阴极附近溶液pH变化的原因:____________________。
④若将制得的氢气、氧气和氢氧化钾溶液组合为氢氧燃烧电池,则电池正极的电极反应式为_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014学年河南省开封市高三第二次模拟考试理综化学试卷(解析版) 题型:实验题
乙二酸(H2C2O4)俗称草酸,是一种重要的化工原料。查阅资料,了解到以下有关信息:
①乙二酸易溶于水,加热至100℃开始升华,125℃时迅速升华,157℃时大量升华并开始分解。乙二酸受热分解生成水、二氧化碳和一种常见的还原性气体。
②乙二酸的钙盐——乙二酸钙为不溶于水的白色晶体。某校化学研究性学习小组为探究草酸的部分性质,进行了如下实验:
(1)为比较相同浓度的草酸和硫酸的导电性,实验室需配制100 mL 0.1mol/L的草酸溶液,配制过程中用到的玻璃仪器有量筒、烧杯、玻璃棒、_____ 、____。
(2)化学兴趣小组的同学用实验证明乙二酸晶体受热分解生成的气体成分。他们利用下图提供的装置,自选试剂,提出了下列实验方案:按A→B→C→C→C→D→E顺序从左至右连接装置,检验乙二酸晶体受热分解生成的气体成分。请你按整套装置从左至右的顺序填写下表中的空格:
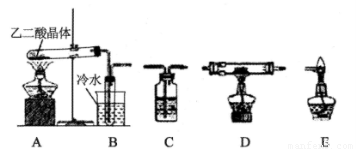
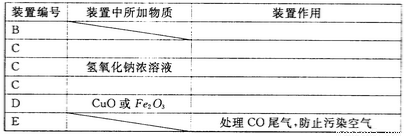
①请写出乙二酸受热分解的化学方程式 _______。
②上述实验中能说明乙二酸热分解生成了还原性气体的实验现象是____。
③检验乙二酸具有较强的还原性,通常选用的试剂是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
从100 mL 0.1 mol / L的AlCl3溶液中取出50 mL,其中Cl-的物质的量浓度是
A.0.3 mol / L B.0. 5 mol / L
C.0.1 mol / L D.0.15 mol / L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com