
【题目】分别以下列各组物质作为单体在一定条件下,通过缩聚反应能合成高分子化合物的是( )
①乙烯、丙烯、苯乙烯
②乙酸、乙二醇
③1,![]() 己二酸、1,
己二酸、1,![]() 己二胺
己二胺
④对苯二甲酸、乙二醇
⑤α-氨基乙酸、α-氨基丙酸
⑥α-羟基丙酸
A.①③⑤⑥B.①②③④C.③④⑤⑥D.①②③④⑤⑥
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】有机物M的合成路线(反应条件略去)如图所示:

下列叙述错误的是( )
A.步骤(1)产物中残留的苯酚可用FeCl3溶液检验
B.苯酚和M均可与酸性KMnO4溶液发生反应
C.苯氧乙酸和M均可与NaOH溶液发生反应
D.步骤(2)产物中残留的烯丙醇可用溴水检验
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列结构示意图,判断下列说法中正确的是
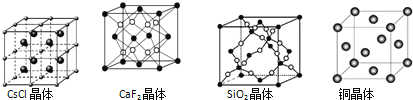
A.在CsCl晶体中,距Cs+最近的Cl-有6个
B.在CaF2晶体中,Ca2+周围距离最近的F-有4个
C.在SiO2晶体中,每个晶胞中含有4个Si原子和8个O原子
D.在铜晶体中,每个铜原子周围距离最近的铜原子有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G都是有机化合物,它们的转化关系如图所示:
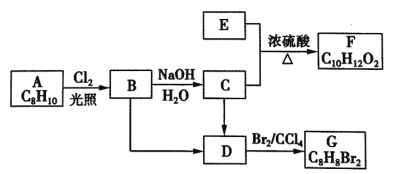
(1)已知6.0g化合物E完全燃烧生成8.8gCO2和3.6gH2O,同温同压下E的蒸气与氢气的密度比为30:1,则E的分子式为__________。
(2)A为一取代芳香烃,B中含有一个甲基。由B生成C的化学方程式为_________。
(3)由B生成D、由C生成D的反应条件分别是______________、________________。
(4)由A生成B、由D生成G的反应类型分别是______________、________________。
(5)F的结构简式为______________。
(6)在G的同分异构体中,苯环上的一硝基取代物只有一种的共有_______种,其中分子中含有两种不同化学环境的氢原子且个数比为1:1的是_____________(填结构简式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.聚丙烯能使酸性高锰酸钾溶液褪色
B.聚乙烯是由分子组成的化合物,有固定的熔点
C.同质量的乙烯和聚乙烯燃烧后生成的![]() 的质量相等
的质量相等
D.高分子化合物的特点之一是组成元素简单、结构复杂、相对分子质量大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物由碳、氢氧三种元素组成,该有机物中碳元素的质量分数为54.5%,所含氢原子数是碳原子数的2倍,又知其最简式即为其分子式。则该有机物的分子式为( )
A.CH2OB.CH2O2C.C2H4O2D.C2H4O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某药物C能治疗血管疾病,它在人体内能释放出一种“信使分子”D。已知C的相对分子质量为227,由C、H、O、N四种元素组成,C、H、N的质量分数依次为15.86%、2.20%和18.50%。
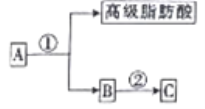
(1)C的分子式为________。D是双原子分子,相对分子质量为30,则D的分子式为______。
(2)药物C可由油脂A经如图途径得到。反应②的化学方程式为_____________________。
(3)0.1molB与足量的金属钠反应,消耗____g金属钠。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A经李比希法和质谱法分析得知其分子式为C8H8O2,相对分子质量为 136,A的核磁共振氢谱有4个峰且面积之比为1:2:2:3,A分子中只含一个苯环,且苯环上只有一个取代基,其核磁共振氢谱与红外光谱如图。关于A的下列说法中不正确的是( )
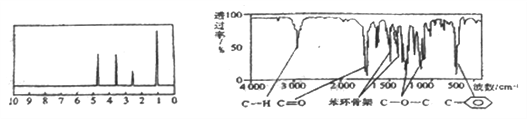
A. A分子属于酯类化合物,在一定条件下能发生水解反应
B. A在一定条件下可与3 mol H2发生加成反应
C. 符合题中A分子结构特征的有机物只有一种
D. 与A属于同类化合物的同分异构体只有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据环保要求,在处理有氰电镀废水时,剧毒的CN-离子在催化剂TiO2颗粒作用下,先用NaClO将CN-离子氧化成CNO-(CN-和CNO-中N元素均为-3价),再在酸性条件下继续与NaClO反应生成N2、CO2和Cl2。环保工作人员在密闭系统中用如图装置进行实验,测定CN-被处理的百分率。
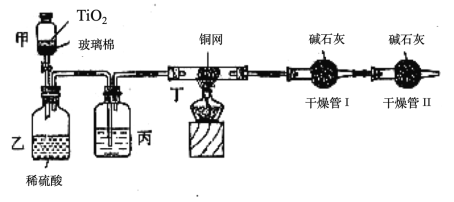
现将浓缩后含CN-离子的污水与过量NaClO溶液的混合液倒入甲中,塞上橡皮塞,一段时间后,打开橡皮塞和活塞,使溶液全部放入乙中,关闭活塞。回答下列问题:
(1)根据题意,写出相关主要反应的离子方程式:甲中的反应_________________,乙中的反应:_____________________。
(2)上述实验是通过测定CO2的量来确定对CN-的处理效果。丙装置中的试剂是______________,丁装置的目的是________________________;干燥管Ⅱ的作用是______________________。
(3)假定上述每一个装置都充分吸收,则利用该装置测得的CN-被处理的百分率与实际值相比_____(填“偏高”或“偏低”),简述可能的原因:______________________。
(4)含氰废水也可采用电化学方法进行处理。在碱性条件下,使用惰性电极电解含氰废水,氰离子被氧化为无毒的物质,其中阳极电极反应式是___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com