
汽车尾气里含有有毒的NO和CO,NO和CO能缓慢地反应生成N2和CO2.对此反应的下列叙述不正确的是( )
A. 使用催化剂能加快反应速率
B. 升高温度能加快反应速率
C. 改变压强对反应速率无影响
D. 此反应能减轻尾气对环境的污染
考点: 氮的氧化物的性质及其对环境的影响.
专题: 氮族元素.
分析: NO和CO能缓慢地反应生成N2和CO2,把有毒气体变为无毒气体减轻了对环境的污染;影响反应速率的因素主要有温度、压强、浓度、催化剂、表面积等,升高温度会加快反应速率;对有气体参加的反应,增大压强会增大反应速率;增大浓度会增大反应速率;使用催化剂可以加快反应速率.
解答: 解:A、使用催化剂能加快反应速率,故A正确;
B、升温能加快化学反应速率,故B正确;
C、NO和CO反应为2NO+2CO=N2+2CO2,反应前后都有气体,改变压强一定改变化学反应速率,故C错误;
D、有毒气体NO和CO反应生成了无毒的气体N2和CO2,减少了对大气的污染,故D正确;
故选C.
点评: 本题主要考查了外界条件对化学反应速率的影响,如何对污染气体处理成无污染的气体,减少对大气的污染.


科目:高中化学 来源: 题型:
工业上制备纯硅反应的热化学方程式如下:
SiCl4(g)+2H2(g)===Si(s)+4HCl(g)ΔH=+Q kJ·mol-1(Q>0)某温度、压强下,将一定量的反应物通入密闭容器中进行以上反应(此条件下为可逆反应),下列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl4的转化率
B.若反应开始时SiCl4为1mol,则达到平衡时,吸收热量为QkJ
C.反应至4min时,若HCl浓度为0.12mol·L-1,则H2的反应速率为
0.03mol·L-1·min-1
D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL1mol·L-1的NaOH溶液中恰好反应
查看答案和解析>>
科目:高中化学 来源: 题型:
在298 K、100 kPa时,已知:2H2O(g)===O2(g)+2H2(g) ΔH1
Cl2(g)+H2(g)===2HCl(g) ΔH2
2Cl2(g)+2H2O(g)===4HCl(g)+O2(g) ΔH3
则ΔH3与ΔH1和ΔH2间的关系正确的是( )
A.ΔH3=ΔH1+2ΔH2 B.ΔH3=ΔH1+ΔH2
C.ΔH3=ΔH1-2ΔH2 D.ΔH3=ΔH1-ΔH2
查看答案和解析>>
科目:高中化学 来源: 题型:
在2 L密闭容器内,800℃时反应:2NO(g)+O2(g)2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.01 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)800℃,反应达到平衡时,NO的物质的量浓度是________;升高温度,NO的浓度增大,则该反应是________(填“放热”或“吸热”)反应。
(2)如图中表示NO2的变化的曲线是________。用O2表示从0~2 s内该反应的平均速率v=________。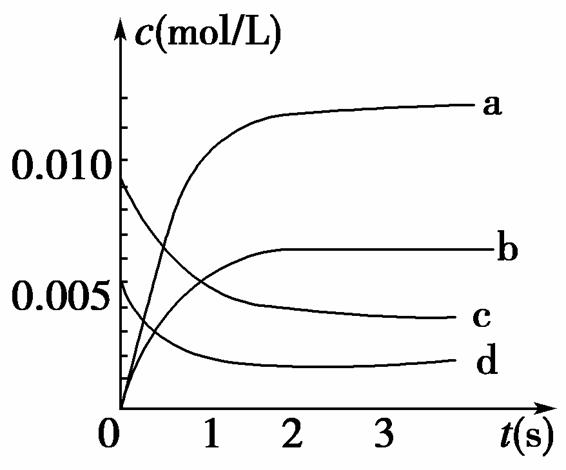
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2) b.容器内压强保持不变
c.v逆(NO)=2v正(O2) d.容器内密度保持不变
(4)能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
意大利科学家合成了一种新型氧分子,它是由四个氧原子构成的(O4),下列微粒互为同素异形体的是( )
①168O ②O2③188O ④O3 ⑤O4 ⑥O2﹣ ⑦O22﹣.
A. ①③⑥ B. ②④⑤ C. ①②⑦ D. ④⑤⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
少量铁粉与100mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率可以使用如下方法( )
A. 加H2O B. 加入饱和食盐水
C. 增大压强 D. 升高温度(不考虑盐酸挥发)
查看答案和解析>>
科目:高中化学 来源: 题型:
NA代表阿伏伽德罗常数的值,下列说法正确的是( )
A. 7.8g苯中碳碳双键的数目为0.3NA
B. 常温常压,11.2L CO和O2混合气体的原子数为NA
C. 1molNO2溶于足量水中,转移电子的数目为NA
D. 1.5g甲基所含有的电子数目为0.9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
氨气是重要的化工原料.实验室可用浓氨水和 来制取氨气.
a.烧碱 b.生石灰 c.氯化铵
(2)某实验小组设计了下列装置进行氨的催化氧化实验.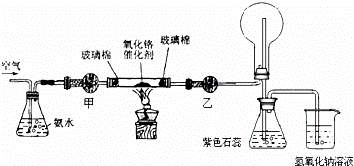
①盛放氨水的实验仪器的名称为 ;在加热条件下,硬质玻璃管中发生反应的化学方程式为 .
②实验时发现:如果缺少乙处的干燥管,将反应后的气体直接通入烧瓶,则烧瓶中先产生白雾,随即产生白烟,其原因是 .
③烧杯中盛有NaOH溶液的作用是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com