
| A. | 向CuSO4溶液中加入Na2O2:2Na2O2+Cu2++H2O═4 Na++Cu(OH)2↓+O2↑ | |
| B. | 工业上用石灰乳制备漂白粉:Ca+2OH-+Cl2=Ca2++ClO-+Cl-+H2O | |
| C. | 向Na2SiO3溶液中通入过量SO2:SiO32-+2SO2+2H2O═H2SiO3↓+2HSO3- | |
| D. | 制备Fe(OH)3胶体:Fe3++3H2O═Fe(OH)3(胶体)+3H+ |
分析 A.反应生成硫酸钠、氢氧化铜和氧气;
B.石灰乳在离子反应中保留化学式;
C.反应生成硅酸和亚硫酸氢钠;
D.加热至沸水,水解生成胶体.
解答 解:A.向CuSO4溶液中加入Na2O2的离子反应为2Na2O2+Cu2++H2O═4 Na++Cu(OH)2↓+O2↑,故A正确;
B.工业上用石灰乳制备漂白粉的离子反应为Ca(OH)2+Cl2=Ca2++ClO-+Cl-+H2O,故B错误;
C.向Na2SiO3溶液中通入过量SO2的离子反应为SiO32-+2SO2+2H2O═H2SiO3↓+2HSO3-,故C正确;
D.制备Fe(OH)3胶体的离子反应为Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3(胶体)+3H+,故D错误;
故选AC.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.


 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3→Na2SiO3 | B. | SiO2→H2SiO3 | C. | Cu→CuSO4 | D. | SiO2→Si |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金刚石的网状结构中,由共价键形成的碳原子环,其中最小的环上有6个碳原子 | |
| B. | 在氯化钠晶体中,每个Na+或Cl-的周围紧邻6个Cl-或6个Na+ | |
| C. | 干冰晶体熔化时,1mol干冰要断裂2mol碳氧双键 | |
| D. | 在氯化铯晶体中,每个Cs+周围紧邻8个Cl-,每个Cl-周围也紧邻8个Cs+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
| CO | H2O | CO | H2 | |||
| 1 | 650 | 2 | 4 | 0.5 | 1.5 | 5 |
| 2 | 900 | 1 | 2 | 0.5 | 0.5 | - |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
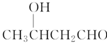
| A. | ①③④ | B. | ②④⑤ | C. | ①③⑤ | D. | ①②⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com