
| A. | 小苏打溶液与过量的澄清石灰水反应:Ca2++OH-+HCO${\;}_{3}^{-}$=CaCO3↓+H2O | |
| B. | 少量SO2通入氢氧化钠溶液中:OH-+SO2=HSO${\;}_{3}^{-}$ | |
| C. | 双氧水作脱氯剂,用于消除水中的氯气:Cl2+H2O2=2HCl+O2 | |
| D. | Fe3O4溶于氢碘酸的离子方程式:Fe3O4+8H+=2Fe3++Fe2++4H2O |
分析 A.苏打溶液与过量的澄清石灰水反应可生成碳酸钙沉淀和水;
B.少量SO2通入氢氧化钠溶液生成亚硫酸根离子;
C.氯气与过氧化氢发生氧化还原反应生成氧气;
D.铁离子与碘离子发生氧化还原反应生成碘单质和亚铁离子.
解答 解:A.小苏打溶液与过量的澄清石灰水反应可生成碳酸钙沉淀和水,反应的离子方程式为HCO3-+Ca2++OH-═CaCO3↓+H2O,故A正确;
B.少量SO2通入氢氧化钠溶液生成亚硫酸根离子,离子方程式为2OH-+SO2=SO32-+H2O,故B错误;
C.氯气与过氧化氢发生氧化还原反应生成氧气,方程式为Cl2+H2O2=2HCl+O2,故C正确;
D.铁离子与碘离子发生氧化还原反应生成碘单质和亚铁离子,离子方程式为2I-+Fe3O4+8H+=3Fe2++4H2O+I2,故D错误.
故选AC.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,侧重考查学生的分析能力,注意与量有关的离子反应及与氧化还原有关的离子反应均为解答的难点,题目难度较大.


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:选择题
| A. | 检验自来水中是否含有氯离子 | B. | 检验土豆中是否含有淀粉 | ||
| C. | 检验鸡蛋中是否含有碳酸钙 | D. | 检验无水酒精中是否含水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有化学键断裂或化学键形成的过程都是化学变化 | |
| B. | Na2O2和Na2O都属于碱性氧化物 | |
| C. | 溶液中的溶质粒子能透过滤纸,而胶体中的分散质粒子不能透过滤纸,所以可以用滤纸来分离溶液和胶体 | |
| D. | 食盐溶液能导电,但食盐溶液不是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属钠着火不能用CO2扑灭,推测:金属钾着火也不能用CO2扑灭 | |
| B. | 工业上电解熔融的MgCl2制Mg,推测:工业上电解熔融的AlCl3制Al | |
| C. | Fe与CuCl2溶液反应可以置换出Cu,推测:钠与CuCl2溶液反应也可以置换出Cu | |
| D. | Fe+S$\frac{\underline{\;\;△\;\;}}{\;}$FeS,推测:Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$CuS |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化性:A2>B2>C2>D2 | B. | 还原性:A->B->C->D- | ||
| C. | 2A-+D2═2D-+A2反应不可以进行 | D. | 2C-+B2═2B-+C2反应能进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 序号 | 古文 | 解释 |
| A | 烧酒非古法也,自元时创始,其法用浓酒和糟入甑(指蒸锅),蒸令气上,用器承滴露 | 白酒(烧酒)的制造过程中采用了蒸馏的方法来分离和提纯 |
| B | 白青(碱式碳酸铜)得铁化为铜 | 可以用铁来冶炼铜 |
| C | 初,人不知盖泥法,元时南安有黄长者为宅煮糖,宅垣忽坏,去土而糖白,后人遂效之 | 蔗糖的分离提纯采用了黄泥来吸附红糖中的色素 |
| D | 丹砂烧之成水银,积变又成丹砂 | 加热时丹砂(HgS)熔融成液态,冷却时重新结晶为HgS晶体 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y与氢元素所形成的化合物分子只含有极性键 | |
| B. | W2Y、W2Y2中阴、阳离子个数比均为1:2 | |
| C. | Z的最高价氧化物对应水化物的酸性比R的强 | |
| D. | 将XY2通入W单质与水反应后的溶液中,生成的盐只有一种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
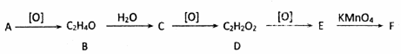
 ,其产量可以用来衡量一个国家石油化工的发展水平.
,其产量可以用来衡量一个国家石油化工的发展水平. ,且无环状结构的同分异构体有8种.(不考虑立体异构)
,且无环状结构的同分异构体有8种.(不考虑立体异构) .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com