
一定温度下,在恒容密闭容器中发生如下反应:2A(g)+B(g) 2C(g),若反应开始时充入2mol A和1mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数仍为a%的是
2C(g),若反应开始时充入2mol A和1mol B,达平衡后A的体积分数为a%。其他条件不变时,若按下列四种配比作为起始物质,平衡后A的体积分数仍为a%的是
A.3mol C B.0.5mol A、1.5mol B和1.5molC
C.1mol B和1mol C D.1mol A、0.5mol B和1mol C
科目:高中化学 来源:2017届北京市昌平区高三上学期期末化学试卷(解析版) 题型:选择题
纳米Fe3O4晶体材料可以作为核磁共振造影增强剂,用于疾病的诊断和治疗。其制备过程如图所示、下列叙述不合理的是
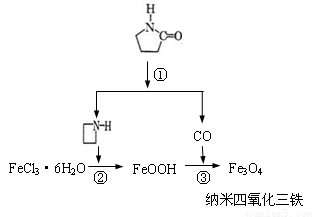
A.在反应②中,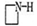 的作用可能是促进氯化铁水解
的作用可能是促进氯化铁水解
B.反应③的化学方程式是:6FeOOH + CO ==2Fe3O4+3H2O+CO2
C.直接加热FeCl3溶液也可以得到四氧化三铁
D.纳米四氧化三铁形成的分散剂,有可能产生丁达尔现象
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高一上期中化学试卷(解析版) 题型:选择题
一定量某营养液中溶质的配方分别如下( )
配方一:0.3mol KCl,0.2mol K2SO4,0.1 molZnSO4
配方二:0.1 mol KCl,0.3 mol K2SO4,0.1 molZnCl2
对于两种营养液的成分,下列说法中正确的是
A.只有n(K+)相同 B.只有n(Cl-)相同
C.各离子的物质的量完全不同 D.完全相同
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高一上期中化学试卷(解析版) 题型:选择题
今年8月天津港发生爆炸,其爆炸品中含“TNT”,则在“TNT”包装袋上的标签上应印有的警示标记是 ( )
A.  B.
B. 
C. 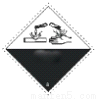 D.
D. 
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷(解析版) 题型:选择题
COCl2(g) CO(g)+Cl2(g) ΔH >0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,其中能提高 COCl2转化率的是
CO(g)+Cl2(g) ΔH >0,当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,其中能提高 COCl2转化率的是
A.①②④ B.①④⑥ C.②③⑤ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷(解析版) 题型:选择题
在密闭容器中进行反应X2(g)+Y2(g) 2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是 ( )
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1 mol·L-1、0.2 mol·L-1、0.2 mol·L-1,在一定条件下,当反应达到平衡时,各物质的浓度有可能是 ( )
A.Z为0.2 mol·L-1 B.Y2为0.35 mol·L-1
C.X2为0.3 mol·L-1 D.Z为0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江、吉林省两省六校高二上期中化学试卷(解析版) 题型:选择题
下列说法正确的是
A.化学反应除了生成新的物质外,还伴随着能量的变化
B.据能量守恒定律,反应物的总能量一定等于生成物的总能量
C.放热反应不需要加热就能发生
D.吸热反应不加热就不会发生
查看答案和解析>>
科目:高中化学 来源:2017届北京市海淀区高三上学期期末化学试卷(解析版) 题型:实验题
为探究FeCl3溶液中的离子平衡和离子反应,某小组同学进行了如下实验。
(1)配制50 mL 1.0 mol·L?1的FeCl3溶液,测其pH约为0.7,即c(H+) = 0.2 mol·L?1。
① 用化学用语解释FeCl3溶液呈酸性的原因: 。
② 下列实验方案中,能使FeCl3溶液pH升高的是 (填字母序号)。
a. 加水稀释 b. 加入FeCl3固体
c. 滴加浓KSCN溶液 d. 加入NaHCO3固体
(2)小组同学利用上述FeCl3溶液探究其与足量锌粉的反应。实验操作及现象如下:
操作 | 现象 |
向反应瓶中加入6.5 g锌粉,然后加入50 mL 1.0 mol·L?1的FeCl3溶液,搅拌 | 溶液温度迅速上升,稍后出现红褐色沉淀,同时出现少量气泡;反应一段时间后静置,上层溶液为浅绿色,反应瓶底部有黑色固体 |
收集检验反应过程中产生的气体 | 集气管口靠近火焰,有爆鸣声 |
已知:Zn的性质与Al相似,能发生反应:Zn + 2NaOH = Na2ZnO2 + H2 ↑
① 结合实验现象和平衡移动原理解释出现红褐色沉淀的原因: 。
② 用离子方程式解释反应后溶液为浅绿色的原因: 。
③ 分离出黑色固体,经下列实验证实了其中含有的主要物质。
i. 黑色固体可以被磁铁吸引;
ii. 向黑色固体中加入足量的NaOH溶液,产生气泡;
iii. 将ii中剩余固体用蒸馏水洗涤后,加入稀盐酸,产生大量气泡;
iv. 向iii反应后的溶液中滴加KSCN溶液,无变化。
a. 黑色固体中一定含有的物质是 。
b. 小组同学认为上述实验无法确定黑色固体中是否含有Fe3O4,理由是 。
(3)为进一步探究上述1.0 mol·L?1 FeCl3溶液中Fe3+和H+氧化性的相对强弱,继续实验并观察到反应开始时现象如下:
操作 | 现象 |
将5 mL 1.0 mol·L?1的FeCl3溶液与0.65 g锌粉混合 | 溶液温度迅速上升,开始时几乎没有气泡 |
将 与0.65 g锌粉混合 | 溶液中立即产生大量气泡 |
小组同学得出结论:在1.0 mol·L?1 FeCl3溶液中,Fe3+的氧化性比H+更强。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com