
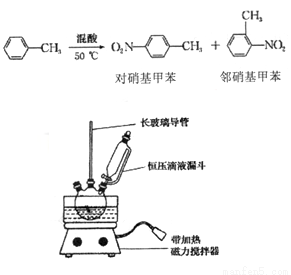
ʵ�����Ʊ�һ�����ױ�����Ҫ���������ױ��Ͷ������ױ����ķ�Ӧԭ����ʵ��װ
�ܶ�/��g��cm-3) | �е㣯�� | ʽ�� | �ܽ��� | |
�ױ� | 0.866 | 110.6 | 92 | ������ˮ��������һ�����ױ� |
�������ױ� | 1.286 | 237.7 | 137 | ������ˮ��������Һ̬�� |
�������ױ� | 1.162 | 222 | 137 | ������ˮ��������Һ̬�� |
ʵ�鲽�裺
�� ���ƻ��ᣬ��װ��ͼ��Ӧװ�á�ȡ100 mL �ձ�����10 mL Ũ������30 mL Ũ������
�ƻ��ᣬ�����ѹ��Һ©���У���15 mL �ױ����ۺ�����13.0g������������ƿ�С�
�� �������µļױ�����μӻ��ᣬ�ߵα߽��裬��Ͼ��ȡ�
�� ��50һ60�� �·�����Ӧ��ֱ����Ӧ������
�� ��ȥ���������������ˮ��10% NaCO3��Һϴ�ӣ������������ˮϴ�ӵõ��ֲ�Ʒ��
��ش��������⣺
��l������40mL ����IJ�����________________
��2��װ���л�ȱ��__________�����������ƣ�������¶ȳ���60�棬������____�����������ƣ����ɡ�
��3������ֲ�Ʒ��ˮ�IJ���������__________
��4����Ʒ��10% NaCO3��Һϴ��֮����������ˮϴ�ӣ������Ʒ�Ƿ�ϴ�ɾ��IJ�����_______
��5��Ϊ�˵õ�������������������������Һ���м���_______��ȥˮ��Ȼ�����������յõ���Ʒ������Ϊ13.70g����һ�����ױ��IJ�����________��
 �����Ծ���ĩ���100��ϵ�д�
�����Ծ���ĩ���100��ϵ�д� ˫��ͬ������ѵ��ϵ�д�
˫��ͬ������ѵ��ϵ�д� �Ƹ�С״Ԫͬ������������ϵ�д�
�Ƹ�С״Ԫͬ������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�߶���ѧ�ڻ���ѵ����15����ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������ֵ������˵������ȷ����
A. 46 g C2H6O�к��е�C-H����һ��Ϊ5 NA
B. ���³�ѹ�£�17 g����һ14CH3��������������Ϊ9NA
C. ��״���£�11.2.L C02����Ȳ�Ļ�����������м���ĿΪNA
D. CO2������������Na2O2��Ӧ����������28 gʱת����NA������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������ʡ�����и�һ��ѧ����ĩ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��10 mL��0.1 mol��L��1 BaCl2��Һǡ�ÿ�ʹ��ͬ�����������������п�������������Һ�е������������ȫת��Ϊ���ᱵ��������������������Һ�����ʵ���Ũ��֮���ǣ� ��
A. 3��2��2 B. 1��2��3 C. 1��3��3 D. 3��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��һ�������������Բ��ԣ��ģ���b�������ۻ�ѧ�Ծ��������棩 ���ͣ������
�й�Ӫ��ѧ�����䲼�ġ�ÿ����ʳӪ���ع�����������(Se)��Ϊ15��ÿ����ʳӪ����֮һ�����һ��������ÿ�������������������50 ~250��g���ش������й����⣺
(1) Se ԭ�ӵļ۵����Ų�ʽΪ_______����̬78 Se ԭ���У��������______�����������෴�ĵ��ӡ�
(2)���������������Һ�ܹ��ܽ��������ɶ���������(M2Sex)�����������Na2Se8���������У���ѧ��������________��Seԭ��֮���γɵĿռ乹��Ϊ_________________��
(3)As��S��Ԫ�����ڱ��о���Se ���ڣ����⻯��ֱ���AsH3��H2Se��H2S���⻯����ȶ���ǿ��˳��Ϊ______________________��
(4)SeCl2��BeCl2��Ϊ1��2��ɵķ��ӣ�SeCl2��Se�Ĺ���ӻ�������_______��BeCl2��Be�Ĺ���ӻ�������_________________��
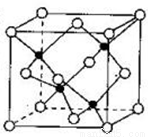
(5)Zn��Seͬ���ڣ�S��Seͬ���塣��Zn��S�γɵ�ZnS�������ư�ɫ�����ϼ�����������ۡ������ϡ���������ȡ�ZnS�����ṹ��ͼ��ʾ�����������ԭ���ھ����ڣ����������ԭ�ӳ��ڶ����⣬�����ԭ���ھ���_________ (��ڲ��������ϡ������ġ�)�����þ�����ܶ�Ϊ��g���M-3�������ӵ�����ΪNA mol-1���������������ⳤ=_____�M(�ú�p��NA�Ĵ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��һ�������������Բ��ԣ��ģ���b�������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ������е������۾���ȷ���Ҵ��������ϵ����
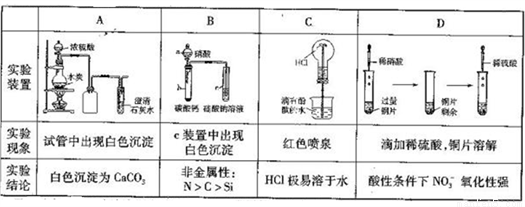
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㽭ʡ������2017�����1�½�ѧ������⻯ѧ�Ծ� ���ͣ��ƶ���
A��B��C��ΪʳƷ�г������л������F�������г���������ȼ�ϣ�Ҳ�Ǻ���ٷֺ�����ߵ��л��D��E����ͬ��Ԫ����ɡ�����֮���ת����ϵ��ͼ��
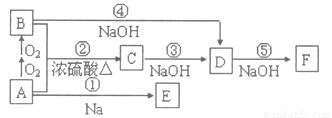
��ش�
��1���л���A�й����ŵ�������________
��2����Ӧ�ٵĻ�ѧ����ʽ___________
��3��F��������Ӧ������Ԫȡ������⻯ѧ����ʽ___________
��4������˵����ȷ����____________
A.3����Ӧ�е�NaOH���������
B.��Ӧ�����ڼӳɷ�Ӧ
C.A��ͬ���칹�岻��������Ʒ�Ӧ��������
D.1molB��1molC��ȫ��Ӧ����NaOH�����ʵ�����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㽭ʡ������2017�����1�½�ѧ������⻯ѧ�Ծ� ���ͣ�ѡ����
��֪��������ͣ�����C8H18��ʾ����ȼ�յ��Ȼ�ѧ����ʽ��
CH4(g)+2O2(g) CO2(g)+2 H2O(l) ��H=��890 kJ • mol��1��
CO2(g)+2 H2O(l) ��H=��890 kJ • mol��1��
C8H18(l)+12.5 O2(g) 8CO2(g)+9H2O(l) ��H=��5472 kJ • mol��1��
8CO2(g)+9H2O(l) ��H=��5472 kJ • mol��1��
ijѧУʳ����ѡ����Ȼ����Ϊ����ȼ�ϣ�����ѡ�����ݲ���ȷ����
A. �����������ͺͼ���ȼ�գ�������������������Ͷ࣬��˼������Ч
B. ������ͬ���������ɵĶ�����̼�����ͱȼ���࣬��˼������Ч
C. ���麬̼���ͣ�ȼ�ո���֣�����̿�����ײ���CO����˸�����
D. �����ʵ��������ͺͼ���ȼ�գ����Ͳ����������ȼ���࣬��˸�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㽭ʡ������2017�����1�½�ѧ������⻯ѧ�Ծ� ���ͣ�ѡ����
��ͼ��ʵ���ҳ����ġ�©����ʾ��ͼ����������ȡ��ˮ�������
A. 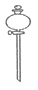 B.
B.  C.
C. 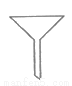 D.
D. 
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�찲��ʡ������ʮУ������3���������ۻ�ѧ�Ծ��������棩 ���ͣ������
Zn(OH)2�����ڰ�ˮ����[Zn(NH3)4]2+: Zn(OH)2+4NH3��H2O=Zn(NH3)4]2++4H2O+2OH-
��1��ԭ��������ZnԪ��С1��Ԫ�ط���Ϊ____����Ԫ��ԭ�ӻ�̬��������Ų�ʽΪ______��
��2��NH3��H2O�ķе������ͬ��Ԫ���⻯��ķе㣬����Ϊ________��
��3��NH3��Nԭ�ӹ�����ӻ�������______��
��4����H2O���ӻ�Ϊ�ȵ�����ķ���Ϊ_____��
��5����п����һ����Ȼ�纬ZnԪ�صĿ���侧��ṹ�����������壨����ͼ��ʾ������������ZnS����ṹ��S2-����λ��Ϊ________��Zn2+�ķ�������Ϊ��l/4,l/4,l/4������3/4, 3/4,l/4������3/4��l/4,3/4������1/4,3/4,3/4������S2-�ķ�������Ϊ______��

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com