
将9g 由CO和H2组成的混合气体在足量的O2中充分燃烧后,将生成的所有产物通过足量的Na2O2固体,Na2O2固体增加的
由CO和H2组成的混合气体在足量的O2中充分燃烧后,将生成的所有产物通过足量的Na2O2固体,Na2O2固体增加的 质量为( )
质量为( )
A.8g B.9g C.12g D.13.5g
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源:2017届宁夏高三上月考二化学卷(解析版) 题型:选择题
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同。下列分析正确的是
A.脱氧过程是吸热反应,可降低温度,延长糕点保质期
B.脱氧过程中铁作原电池正极,电极反应为:Fe-3e→Fe3+
C.脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4e→4OH-
D.含有1.12g铁粉的脱氧剂,理论上最多能吸收氧气336mL(标准状况)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林长春外国语学校高一上期末文化学卷(解析版) 题型:选择题
分散质粒子直径在1nm~100nm 之间的分散系是
A、溶液 B、乳浊液 C、胶体 D、悬浊液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林长春外国语学校高一上期末文化学卷(解析版) 题型:选择题
下列物质中,能够导电的电解质是
A、铜丝 B、熔融的MgCl2 C、NaCl溶液 D、蔗糖
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林长春外国语学校高一上期末理化学卷(解析版) 题型:实验题
某研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并共同解答下列问题:
探究一 设计如图所示装置进行“铁与水反应”的实验(夹持仪器略)。
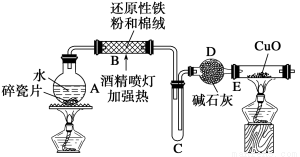
(1)硬质玻璃管B中发生反应的化学方程式为__________________________。
(2)反应前A中投放碎瓷片的目的是____________________。
(3)装置E中的现象是________________________________。
探究二 设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻璃管B冷却后,取少许其中的固体物质溶于稀硫酸后,将所得溶液分成两份。
①一份滴加几滴KSCN溶液。若溶液变血红色,推断硬质玻璃管B中固体物质的成分为________(选填序号,下同);若溶液未变血红色,推断硬质玻璃管B中固体物质的成分为________。
A.一定有Fe3O4 B.一定有Fe C.只有Fe3O4 D.只有Fe
② 另一份用胶头滴管滴加酸性KMnO4溶液,若溶液褪色,可以证明溶液中存在 (填离子符号)。
③ 下列试剂中,不能使Fe3+转化为Fe2+的是
A.氯气
B.Fe
C.H2O2
D.稀硝酸
E.Cu
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林长春外国语学校高一上期末理化学卷(解析版) 题型:选择题
将少量金属钠分别投入下列物质中,有气体放出,且溶液质量减轻的是( )
A.H2SO4 B.CuSO4 C.KNO3 D.KOH
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林长春外国语学校高一上期末理化学卷(解析版) 题型:选择题
某合金与铁的物理性质比较如下

(注:硬度以金刚石为10作标准,导电性以银的导电性100为标准)
已知某合金耐腐蚀、强度大.从以上性能看,该合金不适合制成( )
A.门窗框  B.炉具 C.导线 D.飞机外壳
B.炉具 C.导线 D.飞机外壳
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林长春外国语学校高二上期末化学试卷(解析版) 题型:选择题
“环 境保护”意识深入人心,下列关于酸雨的认识中错误的是
境保护”意识深入人心,下列关于酸雨的认识中错误的是
A..正常条件下,pH值小于5 .6的
.6的 降雨是“酸雨”
降雨是“酸雨”
B.冰岛火山喷发含有大量SO2,在局部区域形成酸雨
C.全球“低碳”行动能减少CO2排放量,也就能降低酸雨的形成及危害
D.汽车 尾气含有氮氧化合物,过量排放形成酸雨
尾气含有氮氧化合物,过量排放形成酸雨
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上学期期末化学试卷(解析版) 题型:填空题
汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体相互反应转化为无毒气体。
(1)(1)4CO(g)+2NO2(g) 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是________(填序号);


(2)汽车尾气中CO与H2O(g)在一定条件下可以发生反应:
CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0。
CO2(g)+H2(g) ΔH<0。
820 ℃时在甲、乙、丙三个恒容密闭容器中,起始时按照下表进行投料,达到平衡状态,K=1.0。
起始物质的量 | 甲 | 乙 | 丙 |
n(H2O)/mol | 0.10 | 0.20 | 0.20 |
n(CO)/mol | 0.10 | 0.10 | 0.20 |
①该反应的平衡常数表达式为___________
②平衡时,甲容器中CO的转化率是 。比较下列容器中CO的转化率:乙 甲;丙 甲(填“>”、“=”或“<”)。
③丙容器中,通过改变温度,使CO的平衡转化率增大,则温度 (填“升高”或“降低”),平衡常数K (填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com