
将一块镁铝合金放入过量盐酸中,写出发生反应的化学方程式和离子方程式。
科目:高中化学 来源: 题型:
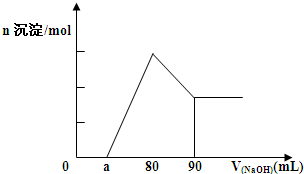 将一块镁铝合金投入1mol?L-1 的一定体积的稀盐酸中,待合金完全溶解后往溶液里滴入1mol?L-1的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积(单位为mL)的关系如图,下列说法中不正确的是( )
将一块镁铝合金投入1mol?L-1 的一定体积的稀盐酸中,待合金完全溶解后往溶液里滴入1mol?L-1的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积(单位为mL)的关系如图,下列说法中不正确的是( )| A、由图可以确定该镁铝合金中铝的质量为0.27克 | ||
| B、当滴入1 mol?L-1的NaOH溶液85mL时,所得沉淀的成分为Mg(OH)2和Al(OH)3 | ||
C、由图可以确定该合金中镁铝物质的量之比
| ||
| D、由图可以确定a的取值范围为:0≤a≤50 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A.Mg-2e-![]() Mg2+ B.Al+4OH--3e-
Mg2+ B.Al+4OH--3e-![]()
![]() +2H2O
+2H2O
C.4OH--4e-![]() 2H2O+O2↑ D.2H2O+2e-
2H2O+O2↑ D.2H2O+2e-![]() 2OH-+H2↑
2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
(2)将单质Fe、Cu与FeCl3、FeCl2、CuCl2溶液一起放进某容器内,根据下述不同情况,填写金属或金属离子。
①充分反应后,如果Fe有剩余,则容器内不可能有________。
②充分反应后,如果容器内还有大量Fe3+,则还会有_________,一定没有_____________。
③充分反应后,如果容器内有较多Cu2+和相当量的Cu,则容器内不可能有_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com