
科目:高中化学 来源: 题型:阅读理解
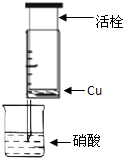 某研究性学习小组设计不同实验方案来研究硝酸的性质.
某研究性学习小组设计不同实验方案来研究硝酸的性质.| 组 | m(Cu)/g | 硝酸(过量) | 溶液颜色 |
| A | 1 | 浓HNO3(4mL) | 溶液为绿色 |
| 1 | 稀HNO3(4mL) | 溶液为蓝色 | |
| B | 0.5 | 浓HNO3(4mL) | 溶液为绿色 |
| 1 | 稀HNO3(4mL) | 溶液为蓝色 | |
| C | 2 | 浓HNO3(4mL) | 溶液为绿色 |
| 1 | 稀HNO3(4mL) | 溶液为蓝色 |
查看答案和解析>>
科目:高中化学 来源:物理教研室 题型:013
A.浓H2SO4 B.浓HNO3 C.稀HNO3 D.稀H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:013
有相同质量的铜,分别与足量的下列酸反应,当反应结束以后,产生的气体在标准状况下体积最大的是( )
A.浓H2SO4 B.浓HNO3 C.稀HNO3 D.稀H2SO4
查看答案和解析>>
科目:高中化学 来源:福建省三明一中2010-2011学年高一上学期第二次月考化学试题 题型:022
某校化学课外兴趣小组同学在做铜与浓硝酸、稀硝酸反应实验时发现:“相同质量的铜分别与等体积足量的浓硝酸、稀硝酸充分反应后,前者溶液颜色是绿色的,后者溶液的颜色是蓝色的.
(1)一种观点认为:这可能是Cu2+浓度差异所致,你同意这种看法吗?(填“同意”或“不同意”)________,原因是________;
(2)另一种观点认为:溶液呈绿色是铜与浓硝酸反应时产生的二氧化氮溶于过量浓硝酸显黄色,加上和蓝色的硝酸铜溶液混在一起,使溶液呈绿色.
为了验证推断是否正确,甲、乙、丙三位同学分别设计了三种方案进行验证:
甲方案:将盛绿色溶液的试管加热,看是否有红棕色气体产生.
乙方案:往绿色溶液试管加入一定量的蒸馏水,观察该试管溶液是否变为蓝色.
丙方案:在通风橱内,将一根下端弯成螺旋状且可抽动的铜丝插在盛有足量浓硝酸的试管甲中,立即可观察到试管中充满红棕色的NO2气体.将气体经导管通入到倾斜的另一支盛有淡蓝色Cu(NO3)2试管乙内,随着实验进行,试管乙中的溶液蓝色加深,很快又变成绿色,继续通入NO2,绿色保持不变,向上抽起铜丝,使反应停止.
请根据以上三位同学的方案回答下列问题:
①甲方案有明显不妥之处.试用化学反应方程式加以说明:________.
②请用化学方程式表示乙方案中的反应原理________.
③根据丙方案进行操作,若出现的现象与其叙述的现象相同,则能否证明第二种观点是正确?________;(填“能”或“不能”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com