
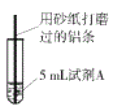
【题目】研究小组进行右图所示实验,试剂A为0.2mol/LCuSO4溶液,发现铝条表面无明显变化,于是改变实验条件,探究铝和CuSO4溶液、CuCl2溶液反应的影响因素。用不同的试剂A进行实验1~实验4,并记录实验现象:
实验序号 | 试剂A | 实验现象 |
1 | 0.2mol/LCuCl2溶液 | 铝条表面有气泡产生,并有红色固体析出 |
2 | 0.2mol/LCuSO4溶液,再加入一定质量的NaCl固体 | 开始铝条表面无明显变化,加NaCl后,铝条表面有气泡产生,并有红色固体析出 |
3 | 2mol/LCuSO4溶液 | 铝条表面有少量气泡产生,并有少量红色固体 |
4 | 2mol/LCuCl2溶液 | 反应非常剧烈,有大量气泡产生,溶液变成棕褐色,有红色固体和白色固体生成 |
(1)实验1中,铝条表面析出红色固体的反应的离子方程式为_________。
(2)实验2的目的是证明铜盐中的阴离子Cl-是导致实验1中反应迅速发生的原因,实验2中加入NaCl固体的质量为______g。
(3)实验3的目的是_________ 。
(4)经检验可知,实验4中白色固体为CuCl。甲同学认为产生白色固体的原因可能是发生了Cu+CuCl2=2CuCl的反应,他设计了右图所示实验证明该反应能够发生。

①A极的电极材料是_________。
②能证明该反应发生的实验现象是_________ 。
(5)为探究实验4中溶液呈现棕褐色的原因,分别取白色CuCl固体进行以下实验:
实验序号 | 实验操作 | 实验现象 |
i | 加入浓NaCl溶液 | 沉淀溶解,形成无色溶液 |
ii | 加入饱和AlCl3溶液 | 沉淀溶解,形成褐色溶液 |
iii | 向i所得溶液中加入2mol/LCuCl2溶液 | 溶液由无色变为褐色 |
查阅资料知:CuCl难溶于水,能溶解在Cl-浓度较大的溶液中,生成[CuCl2]
①由述球实验及资料可推断,实验4中溶液呈棕褐色的原因可能是[CuCl2]-与_____作用的结果。
②为确证实验4所得的棕褐色溶液中含有[CuCl2]-,应补充的实验是_______。
(6)上述实验说明,铝和CuSO4溶液、CuCl2溶液的反应现象与______有关。
【答案】 3Cu2+ + 2Al = 2Al3+ + 3Cu 0.117 证明增大CuSO4溶液的浓度能够使Al和CuSO4的反应发生 金属铜 电流计指针偏转,两极均有白色沉淀生成 Al3+、Cu2+ 取适量实验4的棕褐色溶液,加水稀释,观察是否出现白色沉淀 铜盐中阴离子的种类、铜盐溶液的浓度等
【解析】(1)实验1中,铝与氯化铜反应置换出铜,反应的离子方程式为3Cu2+ + 2Al= 2Al3+ + 3Cu,故答案为:3Cu2+ + 2Al= 2Al3+ + 3Cu;
(2)实验1中n(Cl-)=0.005L×0.2 mol·L-1×2=0.002mol,实验2的目的是证明铜盐中的阴离子Cl-是导致实验1中反应迅速发生的原因,实验2 中加入NaCl固体的质量为0.002mol×58.5g/mol= 0.117g,故答案为:0.117;
(3)实验3与原实验相比,增大了硫酸铜溶液的浓度,铝条表面有少量气泡产生,并有少量红色固体,说明增大CuSO4溶液的浓度能够使Al和CuSO4的反应发生,故答案为:证明增大CuSO4溶液的浓度能够使Al和CuSO4的反应发生;
(4)① Cu + CuCl2= 2CuCl反应中铜被氧化,铜应该做负极,CuCl2被还原,在正极放电,因此A极为负极,选用铜作负极,故答案为:铜;
② 构成原电池后,铜溶解进入溶液,与溶液中的氯离子反应生成白色沉淀,正极铜离子被还原,也生成白色沉淀,电流计指针偏转,故答案为:电流计指针偏转,两极均有白色沉淀生成;
(5)①由上述实验ii及资料可推断,实验4中溶液呈棕褐色的原因可能是[CuCl2]-与Al3+、Cu2+作用的结果,故答案为:Al3+、Cu2+;
②根据信息知,取适量实验4的棕褐色溶液,加水稀释,观察是否出现白色沉淀可以确证实验4所得的棕褐色溶液中含有[CuCl2]-,故答案为:取适量实验4的棕褐色溶液,加水稀释,观察是否出现白色沉淀;
(6)根据实验1和2、2和3、1和4中所用试剂的种类和浓度以及实验现象可知,铝和CuSO4溶液、CuCl2溶液的反应现象与铜盐中阴离子的种类、铜盐溶液的浓度等有关,故答案为:铜盐中阴离子的种类、铜盐溶液的浓度等。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】![]() 是食品加工中最为快捷的食品添加剂,用于焙烤食品;
是食品加工中最为快捷的食品添加剂,用于焙烤食品; ![]() 在分析试剂、医药、电子工业中用途广泛
在分析试剂、医药、电子工业中用途广泛![]() 请回答下列问题:
请回答下列问题:
(1)![]() 可作净水剂,其原理是 ______
可作净水剂,其原理是 ______ ![]() 用必要的化学用语和相关文字说明
用必要的化学用语和相关文字说明![]() .
.
(2)相同条件下, ![]() 的
的![]() 中
中![]() ______
______ ![]() 填“等于”、“大于”或“小于”
填“等于”、“大于”或“小于”![]() 中
中![]()
(3)均为![]() 的几种电解质溶液的pH随温度变化的曲线如图1所示.
的几种电解质溶液的pH随温度变化的曲线如图1所示.

①其中符合![]()
![]() 的pH随温度变化的曲线是 ______ ,导致pH随温度变化的原因是 ______ ;
的pH随温度变化的曲线是 ______ ,导致pH随温度变化的原因是 ______ ;
②![]() 时,
时, ![]() 的
的![]()
![]() 中
中![]() ___ mol/L
___ mol/L
(4)室温时,向100mL![]() 溶液中滴加
溶液中滴加![]() 溶液,溶液pH与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是 ______ 点;在b点,溶液中各离子浓度由大到小的排列顺序是 ______ .
溶液,溶液pH与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是 ______ 点;在b点,溶液中各离子浓度由大到小的排列顺序是 ______ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不能用勒夏特列原理解释的是( )
A. 红棕色的NO2,加压后颜色先变深后变浅
B. 高压比常压有利于合成SO3的反应
C. Fe(SCN)3溶液中加入固体KSCN后颜色变深
D. 由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向猪膀胱内注入一半质量分数为30%的蔗糖溶液,扎紧入口,然后将其浸入质量分数为5%的蔗糖溶液中,每隔10 min称一次猪膀胱的重量,能正确表示测定结果的是下图中的
A.  B.
B. 
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关阿伏伽德罗定律的说法不正确的是
A.同温同压下,相同质量的NO和C2H4(气体)体积相同
B.同温同压下,气体的密度之比等于摩尔质量之比
C.同温同压下,相同体积的H2和CO2的原子数之比为2:3
D.同温同体积的气体,若物质的量相同则压强相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图示是由3个圆所构成的类别关系图,其中I为大圆,II和III分别为大圆之内的小圆。下列选项中符合这种类别关系的是( )

A. I: DNA II: RNA III:核酸
B. I:还原性糖 II:果糖 III:蔗糖
C. I:固醇 II:胆固醇 III:维生素D
D. I:蛋白质 II:酶 III:激素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在核磁共振的图谱上只有三种峰的烷烃是
A. (CH3)2CHCH2CH2CH3 B. (CH3)2CHCH3
C. (CH3)2CHCH(CH3)2 D. (CH3)3CCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)如图所示,一密闭容器被无摩擦、可滑动的两隔板a、b分成甲、乙两室;标准状况下,在乙室中充入NH3 0.4 mol,甲室中充入HCl、N2的混合气体,静止时隔板位置如图所示。已知甲、乙两室中气体的质量差为17.3g。

(1)甲室中气体的质量为________。
(2)甲室中HCl、N2的物质的量之比为______。
(3)将隔板a去掉,当HCl与NH3充分反应生成NH4Cl固体(反应方程式为:HCl(g)+NH3(g)=NH4Cl(s),仅发生此反应),隔板b将位于刻度“________”处(填数字,不考虑固体物质产生的压强),此时体系的平均摩尔质量________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《天工开物》中记载了古人冶金、制陶瓷、硫磺、火药等的过程,是我国古代闪耀的“科技之光”,下列冶炼铁的过程中发生化学变化的是
A.凡铁场所在有之,其铁浅浮土面,浮者拾之 | B.取来淘洗 | C.入炉熔化 | D.凡铁一炉载土二千余斤,或用硬木柴,或用煤炭,或用木炭,土化成铁 |
|
|
|
|
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com