
1mol某有机物充分燃烧,只生成88g二氧化碳气体和54g水,下列正确的是( )
A. 该有机物的分子式为CH4
B. 该有机物的分子式一定为C2H6
C. 该有机物的分子式一定为C2H6O
D. 该有机物的分子中碳原子和氢原子的个数比为1:3,可能含有氧原子
考点: 有关有机物分子式确定的计算.
专题: 烃及其衍生物的燃烧规律.
分析: 根据n= 计算出该有机物燃烧生成二氧化碳、水的物质的量,再根据C、H质量守恒计算出该有机物分子中含有的C、H数目;有机物燃烧生成二氧化碳和水,其分子一定只含有C、H元素,可能含有氧元素,据此对各选项进行判断.
计算出该有机物燃烧生成二氧化碳、水的物质的量,再根据C、H质量守恒计算出该有机物分子中含有的C、H数目;有机物燃烧生成二氧化碳和水,其分子一定只含有C、H元素,可能含有氧元素,据此对各选项进行判断.
解答: 解:1mol该有机物完全燃烧88g二氧化碳气体和54g水,
则:n(C)=n(CO2)= =2mol,
=2mol,
n(H)=2n(H2O)=2× =6mol,
=6mol,
该有机物分子中含有C、H数目分别为: =2、
=2、 =6,
=6,
A.根据计算可知,该有机物分子中C、H数目分别为2、6,所以一定不是甲烷,故A错误;
B.该有机物分子中可能含有氧元素,分子式可能为C2H6O,不一定为烃,故B错误;
C.该有机物分子式可能为C2H6,不一定为C2H6O,故C错误;
D.根据计算结果可知,该有机物分子中碳原子和氢原子的个数比为1:3,其分子中可能含有氧原子,故D正确;
故选D.
点评: 本题考查了有机物分子式确定的计算,题目难度不大,注意掌握根据有机物燃烧及质量守恒确定有机物分子式的计算方法,明确完全燃烧生成二氧化碳和水的化合物不一定为烃,可能含有氧元素.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | P4和CO2分子中都只含有共价键 |
|
| B. | CCl4和NH3的分子的立体结构都是正四面体形 |
|
| C. | BF3分子中各原子均达到8e﹣稳定结构 |
|
| D. | 甲烷的结构式为 |
查看答案和解析>>
科目:高中化学 来源: 题型:
面对目前世界范围内的能源危机,甲醇作为一种较好的可再生能源,具有广泛的应用前景.
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g)⇌CH3OH(g)△H1=﹣90kJ•mol﹣1
②CO(g)+H2O(g)⇌CO2(g)+H2(g)△H2=﹣41kJ•mol﹣1
写出由二氧化碳、氢气制备甲醇的热化学方程式: .
(2)在容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡时的转化率与温度、压强的关系如图所示.
①p1 小于p2(填“大于”、“小于”或“等于”);
②在其他条件不变的情况下,再增加a mol CO与2a mol H2,达到新平衡时,CO的转化率(填“增大”、“减小”或“不变”,下同),平衡常数 .
(3)已知在T℃时,CO(g)+H2O(g)⇌CO2(g)+H2(g)的平衡常数K=0.32,在该温度下,已知c始(CO)=1mol•L﹣1,c始(H2O)=1mol•L﹣1,某时刻经测定CO的转化率为10%,则该反应没有(填“已经”或“没有”)达到平衡,原因是Qc K,此时刻v正 v逆(填“>”或“<”).

查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质的燃烧热相等的是( )
A. 碳和二氧化碳 B. 1mol碳和3mol碳
C. 3mol乙炔(C2H2)和1mol苯 D. 淀粉和纤维素
查看答案和解析>>
科目:高中化学 来源: 题型:
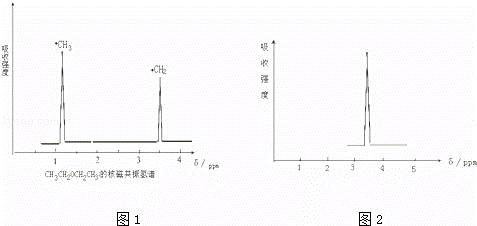
利用核磁共振技术测定有机物分子的三维结构的研究获得了2002年诺贝尔化学奖.在有机物分子中,不同氢原子的核磁共振谱中给出的峰值(信号)也不同,根据峰值(信号)可以确定有机物分子中氢原子的种类和数目.例如二乙醚的结构简式为:
CH3﹣CH2﹣O﹣CH2﹣CH3其核磁共振谱中给出的峰值(信号)有两个,如图1所示:
(1)下列物质中,其核磁共振氢谱中给出的峰值(信号)只有一个的是 .
A.CH3CH3 B.CH3COOH C.CH3COOCH3 D.CH3OCH3
(2)化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图2所示,则A的结构简式为: ,请预测B的核磁共振氢谱上有 个峰(信号).
(3)用核磁共振氢谱的方法来研究C2H6O的结构,简要说明根据核磁共振氢谱的结果来确定C2H6O分子结构的方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,A+ 比B﹣少一个电子层,B原子得一个电子填入3p轨道后,3p轨道已充满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等子中子数.R是由A、D两元素形成的离子化合物,其中A+与D2﹣离子数之比为2:1.请回答下列问题:
(1)A元素形成的晶体内晶胞类型应属于 (填写“六方”、“面心立方”或“体心立方”)堆积,空间利用率为 .
(2)C3﹣的电子排布式为 ,在CB3分子中C元素原子的原子轨道发生的是杂化,CB3分子的VSEPR模型为 .
(3)C的氢化物在水中的溶解度如何
(4)D元素与同周期相邻元素的第一电离能由大到小的关系是:(用元素符号表示);用一个化学方程式说明B、D两元素形成的单质的氧化性强弱:
(5)如图所示是R形成的晶体的晶胞,该晶胞与CaF2晶胞结构相似,设晶体密度是 ρg•cm﹣3.试计算R晶体中A+和D2﹣最短的距离 .(阿伏加德罗常数用NA表示,只写出计算式,不用计算)

查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中除了H+、OH﹣以外,还含有大量的Mg2+、Fe3+、Cl﹣,且这三种离子的物质的量浓度之比为1:1:6,下列有关该溶液判断正确的是( )
A. 向该溶液中加入KI溶液后,原有的5种离子的物质的量不变
B. 向该溶液中滴加稀NaOH溶液,立即出现白色沉淀
C. 向该溶液中加入过量铁粉,只发生置换反应
D. 若溶液中c (Cl﹣)=0.6mol/L,则该溶液的pH=1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com