
| A、酸性:H2SO4>HClO4>HBrO4 |
| B、碱性:RbOH>KOH>NaOH |
| C、非金属性:Cl>S>P |
| D、气态氢化物稳定性:HF>HCl>HBr |


 能力评价系列答案
能力评价系列答案科目:高中化学 来源: 题型:
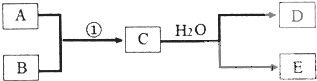 已知物质A、B、C、D、E是由短周期元素构成的单质或化合物,它们可发生如图所示的转化关系:
已知物质A、B、C、D、E是由短周期元素构成的单质或化合物,它们可发生如图所示的转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、④⑤③ | B、⑥①⑤③ |
| C、⑧①⑦③ | D、⑤②⑥③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、W、Y、Z的非金属性大小顺序一定是Z>Y>W |
| B、W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z |
| C、Y、Z形成的分子空间构型可能是正四面体 |
| D、XZ3中含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、OH-、Ba2+、NH4+、Cl- |
| B、K+、Fe2+、H+、NO3- |
| C、NH4+、Al3+、Cl-、NO3- |
| D、Mg2+、SO42-、SiO32-、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应除了生成新物质外,还伴随着能量的变化 |
| B、物质燃烧和中和反应均放出热量 |
| C、分解反应肯定是吸热反应 |
| D、化学反应是吸热还是放热决定于生成物具有的总能量和反应物具有的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、32g O2占有的体积约为22.4L |
| B、22g二氧化碳与标准状况下11.2L HCl含有相同的分子数 |
| C、标准状况下,22.4L水的质量约为18g |
| D、22.4L N2含有阿伏加德罗常数个N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、键能越大,表示该分子越容易受热分解 |
| B、共价键都具有方向性 |
| C、在分子中,两个成键的原子间的距离叫键长 |
| D、H-Cl的键能为431.8kJ?mol-1,H-Br的键能为366kJ?mol-1,说明HCl比HBr分子稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com