
【题目】科学家正在研究温室气体CH4、CO2的转化和利用。
(1)在Ni基催化剂的作用下,CH4和CO2反应可获得化工原料CO和H2。
①基态Ni外围价电子中有_________对成对电子。
②CH4、CO2、H2分子中有孤对电子的是_________.
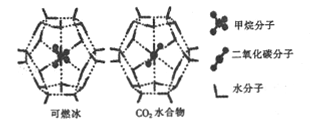
(2)一定条件下,CH4和CO2都能与H2O形成笼状结构(如图所示)的水合物晶体,其相关参数如下表。CH4与H2O形成的水合物俗称“可燃冰”。
参数 分子 | 分子直径/mm | 分子与H2O的结合能(E) |
CH4 | 0.436 | 16.40 |
CO2 | 0.512 | y |
①CO2水合物分子间存在的两种作用力是___________.
②为开采深海海底的“可燃冰”,科学家已经证明可用CO2置换CH4。已知上图中笼状结构的空腔直径为xnm,根据上述图表,从物质的结构与性质的角度分析:x_____0.512;y_______16.40。(填“>”“<"或“=”)
③写出CH4的一种等电子体: __________;SiO2与CO2是否互为等电子体?_________(填“是”或“不是”),理由是________.
【答案】 4 CO2 范德华力、氢键 > > SiH4 不是 SiO2不是分子,两者化学键类型不同
【解析】(1)①Ni为28号元素,基态Ni原子的电子排布式为![]() ,有4对成对电子;②CH4中C最外层有4个电子,有4对共用电子对,因而没有孤对电子;H2中H最外层有1个电子,有1对共用电子对,因而没有孤对电子; CO2中O最外层有6个电子,有2对共用电子对,因而O含有孤对电子;故答案为: ① 4 ② CO2
,有4对成对电子;②CH4中C最外层有4个电子,有4对共用电子对,因而没有孤对电子;H2中H最外层有1个电子,有1对共用电子对,因而没有孤对电子; CO2中O最外层有6个电子,有2对共用电子对,因而O含有孤对电子;故答案为: ① 4 ② CO2
(2)①可燃冰中存在水分子,水分子间存在范德华力和氢键;②由表格可以知道:二氧化碳的分子直径小于笼状结构的空腔直径,即x>0.512,能顺利进入笼状空腔内,且二氧化碳与水的结合能力强于甲烷,即y >16.40; ③等电子体是指价电子数和原子数相同,并且具有相同结构的微粒,可以是分子、离子或原子团,SiH4是CH4的一种等电子体;SiO2是原子晶体,CO2是分子晶体,二者不能互为等电子体;故答案为:①范德华力、氢键 ②> 、 > ③SiH4 、 不是 、 SiO2不是分子,两者化学键类型不同


科目:高中化学 来源: 题型:
【题目】化学对社会发展与进步产生着巨大的贡献。德国化学家哈伯(F.Haber)的重要贡献是( )
A. 实验证实了夸克的存在
B. 发现了黄绿色气体氯气
C. 开发了合成氨的生产工艺
D. 提出了蛋白质分子的螺旋结构模型
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
① 含有大量AlO2-的溶液中,NH4+、NO3-、H+、Cl-可以大量共存
② 0.1 molL-1的AlCl3溶液中,Na+、K+、SO42-、HCO3-可以大量共存
③ 向AlCl3溶液中加入过量的稀氨水,发生反应:Al3++4NH3H2O=AlO2-+4NH4++2H2O
④ 加入铝粉能放出H2的溶液中,Ca2+、Fe2+、Cl-、NO3-一定能够大量共存
⑤ 用NaOH溶液除去铝条表面的氧化膜:Al2O3+2OH-=2AlO2-+H2O
⑥ 依据铝热反应原理,能发生反应2Al+3MgO![]() 3Mg+Al2O3
3Mg+Al2O3
⑦ 向明矾溶液中加入过量Ba(OH)2溶液,发生反应:2SO42-+2Ba2++Al3++4OH-=2BaSO4↓+AlO2-+2H2O
⑧ 常温下,铝可溶于过量浓硝酸,也可溶于过量NaOH溶液
A. ⑤⑦ B. ②③⑤ C. ④⑤⑥ D. ②⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
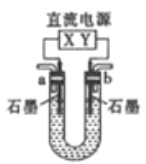
【题目】用如图所示装置(X、Y是直流电源的两极)分别进行下列各组实验,则下表中各项所列对应关系均正确的一组是
选项 | X极 | 实验前U形管中液体 | 通电后现象及结论 |
A | 正极 | Na2SO4溶液 | U形管两端滴入酚酞后,a管中呈红色 |
B | 正极 | AgNO3溶液 | b管中电极反应式是4OH--4e-=O2↑+2H2O |
C | 负极 | CuCl2溶液 | b管中有气体逸出 |
D | 负极 | NaOH溶液 | 溶液PH降低 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
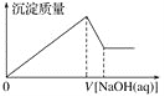
【题目】某溶液中可能含有大量的Mg2+、Al3+、H+、Cl-和少量OH-,向该溶液中逐滴加入0.5 mol·L-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积之间的关系如下图所示,则可判断原溶液中( )
A. 有Mg2+,没有Al3+
B. 有Al3+,没有Mg2+
C. 有Mg2+和Al3+
D. 有大量的H+、Mg2+和Al3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20世纪90年代初,国际上提出“预防污染”这一新概念,绿色化学是预防污染的基本手段,下列各项属于绿色化学的是
A.减少有毒物B.治理污染点C.处理废弃物D.杜绝污染源
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)质量数为37的氯原子符号为_______。
(2)S2-的结构示意图为______。
(3)氮原子的电子式为______,N2的电子式为______,NH4+的电子式为_________
(4)磷原子的核外电子排布式为______,其价电子排布式为_____, 其价电子排布图为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.1mol/L的三种盐溶液,NaX、NaY、NaZ的pH分别为7、8、9,则下列判断中正确的是
A. HX、HY、HZ的酸性依次增强
B. 离子浓度:c(Z-)>c(Y-)>c(X-)
C. 电离常数:K(HZ)<K(HY)
D. c(X-)=c(Y-)+c(HY)=c(Z-)+c(HZ)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com