
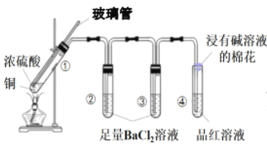
����Ŀ��ijͬѧ����ͼ��ʾʵ��װ��̽��ͭ��Ũ����ķ�Ӧ����¼ʵ���������������˵����ȷ����
�Թ� | �� | �� | �� | �� |
ʵ������ | ��Һ��Ϊ��ɫ���а�������ɫ������� | �д�����ɫ�������� | ��������ɫ�������� | Ʒ����Һ��ɫ |
A.���а�ɫ������BaSO3
B.���п����в���Ũ����ӷ���
C.Ϊ��ȷ�����а�ɫ�����Ƿ�Ϊ����ͭ��������ȴ����Թ���ע��ˮ����
D.ʵ��ʱ������װ����ͨ������N2���ټ����Թܢ٣�ʵ������
���𰸡�B
��������
ʵ��̽��ͭ��Ũ����ķ�Ӧ��װ��1Ϊ����װ�ã���Һ��Ϊ��ɫ��ԭ������ǻ����ϵ��ˮ̫�٣��������ͭ���ӣ��а���˵��������Һ���Ĺ��̣�ͬʱ������ɫ���壬�ù����������ˮ����ͭ���Թ�2��3���а�ɫ�������ɣ��ó���ӦΪ���ᱵ��˵����Ӧ������SO3���ɻ�������ӷ���3�г������٣�˵�����������ӷ���������������ȫ���Թ�4��Ʒ����ɫ˵����Ӧ�����ɶ��������м�������Դ���β�����ݴ˷�������
A. �����������Ȼ�����Һ��Ӧ����ɫ������������BaSO3����A����
B. ���ݷ�����֪���п����в�������ӷ��ˣ���B��ȷ��
C. ��ȴ����Թ�������Ũ����ʣ�࣬Ũ����ϡ�ͷ��ȣ����ܽ�ˮע���Թܣ��ᱩ�з���Σ�գ���C����
D. ��Ӧ������SO3�����������������������ɣ�������װ����ͨ������N2����ϵ��û������������SO3���ɣ��Թ�2��3�н�����������ʵ���������仯����D����
�ʴ�ΪB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ܿ�����ָʾ���ʹ������Ʊ�����ˮ�ܿ�(��Ҫ�ɷ�ΪCo2O3��������Fe2O3��A12O3��MnO��MgO��CaO��SiO2��)��ȡCoC2O42H2O������������

��֪���ٽ���Һ���е���������Ҫ��H+��Co2+��Fe2+��Mn2+��Ca2+��Mg2+��Al3+�ȣ�
�ڲ���������������������ʽ����ʱ��Һ��pH������
������ | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
��ȫ������pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(1)Co2O3��Co�Ļ��ϼ���________________
(2)д������������Na2SO3��Co2O3������Ӧ�����ӷ���ʽ��________________________________________
(3)����Һ�м���NaClO3��Ŀ����______________________________________
(4)��Na2CO3��ʹ����Һ��ijЩ��������ת�����������������������Al(OH)3�⣬���еijɷ���____________��(�ѧʽ)�������ӷ���ʽ�ͱ�Ҫ�����ּ�����ԭ���� _____________________________________________________________________________________
(5)��ȡ���Խ������ӵ���ȡ����pH�Ĺ�ϵ��ͼ����ȡ����������____________________����ʹ�õ�����pH��Χ��_____��
A��2.0��2.5 B��3.0��3.5 C��4.0��4.5

(6)��ҺI�����ơ�þ���ǽ���ת��ΪMgF2��CaF2��������֪Ksp(MgF2)=7.35��10��11��Ksp(CaF2)=1.05��10��10�����������NaF��������Һ c(Mg2+)/c(Ca 2+) =_______��
(7)��m1 kgˮ�ܿ�(��Co2O3 60%)�Ʊ�CoC2O42H2O�����յõ���Ʒ m2 kg������Ϊ________________��(��Ҫ��ó���������ֻ���г����ּ���ʽ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ε������ӵ�ع㷺Ӧ�����ֻ��͵��Եȵ��Ӳ�Ʒ�С�ij��������ӵ�طŵ�ʱ��ص��ܷ�ӦΪ��Li1-xCoO2+LixC6=LiCoO2+ C6(x<1)��2018���й�������ȫ��ɻ�������ӵ��������69%�����ֽ��ҹ��Ͼɵ�ػ����������Ͷ��ܼ��Ͳ�ҵ��Ч��������ߡ�һ�ֻ��ո�����ӵ���е�﮺��ܵ����̣�
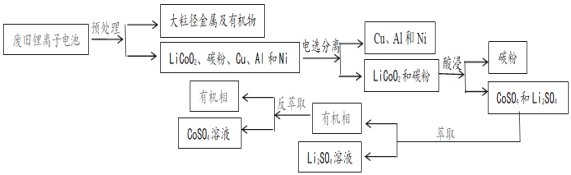
��֪���� Na2S2O3��һ���е�ǿ�ȵĻ�ԭ������ǿ��ֽ�
�� Li2CO3�ܽ�����¶����߶���С
��1�����ڸ�����ӵ��˵������ȷ����_______________________________
A������ӵ��������ﮣ���ŵ�����У�Li+�������缫֮������Ƕ�����Ƕ
B������Ԥ����ʱ��Ϊ��ֹ��ʱ���ڿ��ٷŵ�����ȼ��������ը��Ӧ�Ƚ��зŵ紦��
C�����ʱ��ת��0.01mol���ӣ�ʯī�缫������0.07g
D�����ʱ�������ĵ缫��ӦʽΪLiCoO2��xe��===Li1��xCoO2��xLi��
��2��LiCoO2��һ�־���ǿ�����Ե����ܸ��Ͻ����������Co3+�ڳ��¡�pH=0.5�����¼���ʼˮ�⡣LiCoO2�����������CoSO4�����������ʱ����Ҫ����Na2S2O3�����ܼ����ӻ�ѧ��Ӧԭ���ĽǶȽ���ԭ��_______________________________��д������CoSO4�����ӷ�Ӧ����ʽ��__________________
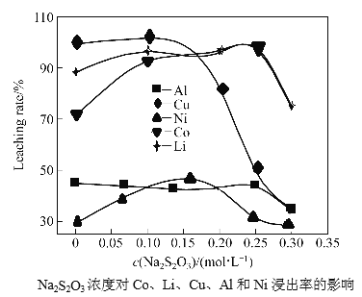
��3������������Ũ��Ϊ4mol/L����Ӧ�¶�90���������ͬʱ�������ӵĽ�������Na2S2O3��Һ�ı仯��ϵ��ͼ�������ʱӦѡ��Ũ��Ϊ_______mol/L��Na2S2O3��Һ��Na2S2O3��ҺŨ������0.3mol/Lʱ��LiCoO2�Ľ����������½������ܵ�ԭ����_________________���û�ѧ����ʽ�������˵����
��4���������չ����У���ѭ��ʹ�õ�������_____________________
��5����֪15������Li2CO3��KspΪ3.210��2�����¶���Li2CO3���ܽ��ԼΪ_____g������ȡ���Li2SO4��Һ������95�������뱥��Na2CO3��Һ����Ӧ10min��________________�����������Li2CO3��ĩ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������±������KOH����Һ�м��Ȳ�������ȥ��Ӧ���ǣ� ��
��![]() ��
��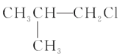 ��(CH3)3CCH2Cl ��CHCl2-CHBr2 ��
��(CH3)3CCH2Cl ��CHCl2-CHBr2 ��![]() ��CH3Cl
��CH3Cl
A.�٢ۢ�B.�ڢۢ�C.ȫ��D.�ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ����������������������Ҵ��Ʊ�1��2һ���������װ����ͼ��ʾ��

�й������б����£�
�Ҵ� | 1.2�������� | ���� | |
״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
�ܶ�/g/cm��3 | 0.79 | 2.2 | 0.71 |
�е�/�� | 78.5 | 132 | 34.6 |
�۵�/�� | ��130 | 9 | ��116 |
�밴Ҫ��ش��������⣺
��1��д��Aװ���еĻ�ѧ��Ӧ����ʽ_____��
��2��װ��C��ʢ������������Һ����������_____
��3���ڴ��Ʊ�ʵ���У�Ҫ������Ѹ�ٵذѷ�Ӧ�¶���ߵ�170�����ң�������ҪĿ����_____
��4���жϸ��Ʊ���Ӧ�Ѿ��������������_____��
��5����������������δ��Ӧ��Br2�������_____ϴ�ӳ�ȥ��������ȷѡ��ǰ����ĸ��
a ˮ b ���������� c �⻯����Һ d �Ҵ�
��6����Ӧ������Ӧ����ˮ��ȴװ��D������ҪĿ����_____�����ֲ��ܹ�����ȴ�����ñ�ˮ������ԭ����_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ�� X��Y��Z��M��ԭ���������������������һ���Ŵط���Z2M2Y4(YX)2���ṹ��ͼ��ʾ��X��M������������������������Yԭ�Ӻ��������������������������![]() ������˵����ȷ����
������˵����ȷ����

A.�����Ӱ뾶: Z>M>Y
B.������Z��M�ĵ��ʾ�������Ũ����
C.X��Y����γɵĻ����������ӻ�����
D.��ҵ�ϳ��õ��Z���Ȼ��������Һ����ȡZ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ա����������ͼ��ʾ��װ���������ᣬ�����й�˵����ȷ����( )

A.a ������b ����
B.��������������������������
C.�����¿��������������������һ������ 50%
D.������ӦʽΪ SO2��2H2O��2e-=SO42-��4H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�����л���ѧ�й㷺����ϵͳ������������ϵͳ������ԭ�ش��������⣺
��ϵͳ������������������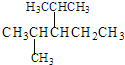 ___��
___��
��3��4��������2����ϩ�Ľṹ��ʽ��___��
��2��![]() �к��еĹ����ŵ�����Ϊ__��
�к��еĹ����ŵ�����Ϊ__��
��3����Ҫ����д���л�ѧ����ʽ��
�ټױ��Ʊ�TNT___��
��ʵ�����Ʊ���ϩ___��
��4���������ʵķе㰴�ɸߵ��͵�˳��������ȷ����__��
��CH3(CH2)2CH3 ��CH3(CH2)3CH3 ��(CH3)3CH ��(CH3)2CHCH2CH3
A.�ܢۢڢ� B.�ڢܢۢ� C.�ڢܢ٢� D.�ܢڢ٢�
��5����������6������������������ص��л����CH3COOH(��ζ��)��HCOOCH3(�̲�Ѭ����)��![]() (�Ʒ�ȩ��֬)��
(�Ʒ�ȩ��֬)�� (����ɱ���)��CH2=CH��CH=CH2(�ϳ���ԭ��)��HCHO(������)��������ٻ�Ϊͬ���칹�����___(�����)��
(����ɱ���)��CH2=CH��CH=CH2(�ϳ���ԭ��)��HCHO(������)��������ٻ�Ϊͬ���칹�����___(�����)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CO2�������Ƽ״����Ǽ���ǰ��������������Դ���о�������ijCO�������Ƽ״��ķ�Ӧ��ϵ�У���������Ҫ��Ӧ�У�
i.CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ��H1=-49.4kJ��mol-1
CH3OH(g)+H2O(g) ��H1=-49.4kJ��mol-1
��.CO2(g)+H2(g) ![]() CO(g)+H2O(g) ��H2=+41.2kJ��mol-1
CO(g)+H2O(g) ��H2=+41.2kJ��mol-1
��.CO(g)+2H2(g) ![]() CH3OH(g) ��H3
CH3OH(g) ��H3
��1����H3________ kJ��mol-1
��2��5MPaʱ����ij�ܱ������а�Ͷ�ϱ�n��H2��:n��CO2��=3��1����H2��CO2����Ӧ�ﵽƽ��ʱ����ø���ֵ����ʵ����������¶ȱ仯��������ͼ��ʾ��
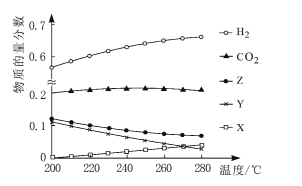
����ϵ��CO2�����ʵ����������¶ȵ�Ӱ�첻��ԭ����____��
��250��ʱ����Ӧii��ƽ�ⳣ��____1���������������=������
�����д�ʩ�У�����״����ʵ���____�����ţ���
A ��������CO B ����ѹǿ C ѭ������ԭ���� D �����¶�
����ͼ��X��Y�ֱ����____���ѧʽ����
��3����Ӧi���ܵķ�Ӧ��������ͼ��ʾ��
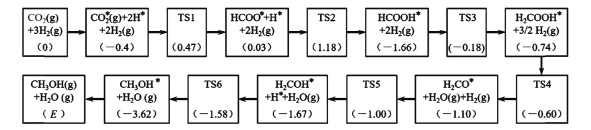
ע�������ڰ��������༰��Ŀ���������������������������ֻ���ĸ����λ��eV�������У�TS��ʾ����̬��*��ʾ�����ڴ����ϵ�����
�ٷ�Ӧ�����У����ɼ״��ľ��ٲ���ķ�Ӧ����ʽΪ____��
�����������E=____������������2λС����������֪��leV=1.6��10-22kJ��
��4���õ�ⷨҲ��ʵ��CO2�����Ƽ״���ϡ�������������Һ�������ʱ�������ص�____��ͨ�������������ϵĵ缫��ӦΪ____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com