
(1)地球上的能源主要源于太阳,绿色植物的光合作用可以大量吸收CO2以减缓温室效应,主要过程可以描述分为下列三步(用“C5”表示C5H10O4,用“C3”表示C3H6O3):
Ⅰ、H2O(l)═2H+(aq)+ 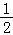 O2(g)+2e﹣△H=+284kJ/mol
O2(g)+2e﹣△H=+284kJ/mol
Ⅱ、CO2(g)+C5(s)+2H+(aq)═2C3+(s)△H=+396kJ/mol
Ⅲ、12C3+(s)+12e﹣═C6H12O6(葡萄糖、s)+6C5(s)+3O2(g)△H=﹣1200kJ/mol
写出绿色植物利用水和二氧化碳合成葡萄糖并放出氧气的热化学方程式_________.
(2)降低大气中CO2的含量及有效地开发利用CO2,目前工业上有一种方法是用CO2来生产燃料甲醇.为探究反应原理,现进行如下实验,在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=﹣49.0kJ/mol.
CH3OH(g)+H2O(g)△H=﹣49.0kJ/mol.
测得CO2和CH3OH(g)的浓度随时间变化如图1所示

①一定温度下,不能说明该反应达到平衡状态的是:_________(填序号)
a.体系的压强不再改变
b.体系的密度不再改变
c.各气体的浓度不再改变
d.各气体的质量分数不再改变
e.反应速率v(CO2)正∶v(H2)逆=1∶3
②从反应开始到平衡,氢气的平均反应速率v(H2)=________mol/(L•min);
③氢气的转化率=____________;
④该反应的平衡常数为K=_________保留三位有效数字);
⑤下列措施中能使平衡体系中n(CH3OH)/ n(CO2)增大的是________.
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离出去 D.再充入1mol CO2和3mol H2
⑥当反应达到平衡时,H2的物质的量浓度为c1,然后向容器中再加入一定量H2,待反应再一次达到平衡后,H2的物质的量浓度为c2.则c1____c2的关系(填>、<、=).
(3)减少温室气体排放的关键是节能减排,大力开发利用燃料电池就可以实现这一目标.如图2所示甲烷燃料电池(在上面).请回答:
①通入甲烷一极的电极反应式为___________;
②随着电池不断放电,电解质溶液的pH______(填“增大”、“减小”或“不变”).
③通常情况下,甲烷燃料电池的能量利用率____(填“大于”、“小于”或“等于”)甲烷燃烧的能量利用率.
④用该燃料电池以石墨电极电解2.0L 0.25 mol·L-1 CuSO4溶液,5min后在一个电极上有6.4gCu析出。则阳极的电极反应式为____________________; 此时得到的O2在标准状况下的体积为______L;向电解后的溶液中加入下列哪种物质可使电解质溶液恢复原来的浓度:____________
A. CuSO4 B.H2O C.CuO D.CuCO3
科目:高中化学 来源:2016-2017学年江西省南昌市高一下学期分班考试化学试卷(解析版) 题型:选择题
相同质量的下列物质分别与等浓度的NaOH溶液反应,至体系中均无固体物质,消耗碱量最多的是( )
A. Al B. Al(OH)3 C. AlCl3 D. Al2O3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省牡丹江市高二上学期开学检测化学试卷(解析版) 题型:选择题
某有机物其结构简式为 ,关于该有机物下列叙述正确的是( )
,关于该有机物下列叙述正确的是( )
A. 在加热和催化剂作用下,最多能和4mol H2反应
B. 不能使溴水褪色
C. 不能使酸性KMnO4溶液褪色
D. 一定条件下,能和NaOH醇溶液反应
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三2月月考理科综合化学试卷(解析版) 题型:实验题
实验室从含碘废液(除H2O外,还含有CCl4、I2、I-等)中回收碘和CCl4,其实验过程如下:
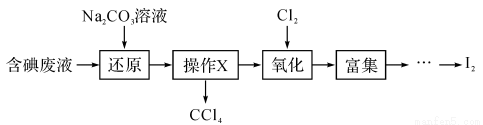
(1)向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为
______________;该操作将I2还原为I-的主要目的是 ____________ 。
(2)操作X的名称为 ___。
(3)氧化时,在三颈烧瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在40℃左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是_____________;锥形瓶里盛放的溶液为_______________
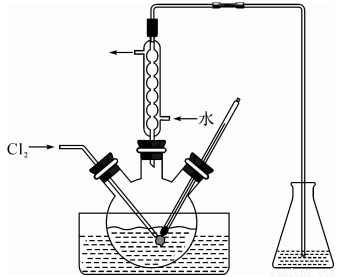
(4)在教材碘水的萃取实验中,最后要从碘的CCl4溶液中回收利用CCl4,可以采用下列方法:先水浴加热蒸馏碘的CCl4溶液,收集得到浅红色的液体。再向该液体中加入少量块状的活性炭,静置。待溶液的浅红色消失。操作Y,即可得无色透明的CCl4液体。
①收集得到浅红色的液体说明,收集得到的液体中含有 ___(化学式),②加入少量活性炭的目的是 ______ ,③操作Y的名称是 ___。
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三2月月考理科综合化学试卷(解析版) 题型:选择题
“绿色化学实验”已走进课堂,下列做法符合“绿色化学”的是( )
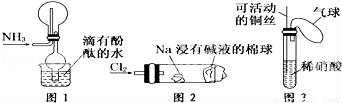
①实验室收集氨气采用图1所示装置
②实验室中做氯气与钠反应实验时采用图2所示装置
③实验室中采用图3所示装置进行铜与稀硝酸的反应
④实验室中用玻璃棒分别蘸取浓盐酸和浓氨水做氨气与酸生成铵盐的实验.
A. ②③④ B. ①②④ C. ①②③ D. ①③④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省菏泽市高二上学期期末学分认定考试B卷化学试卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A. 将过量SO2通入稀氨水中:SO2+NH3•H2O=HSO3﹣+NH4+
B. Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
C. 大理石溶于醋酸中:CaCO3+2H+=Ca2++H2O+CO2↑
D. AlCl3溶液中加入过量稀氨水:Al3++4NH3•H2O=[Al(OH)4]﹣+4NH4+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省菏泽市高二上学期期末学分认定考试B卷化学试卷(解析版) 题型:选择题
在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
物质 | X | Y | Z |
初始浓度/mol•L﹣1 | 0.1 | 0.2 | 0 |
平衡浓度/mol•L﹣1 | 0.05 | 0.05 | 0.1 |
下列说法错误的是( )
A. 反应达到平衡时,X的转化率为50﹪
B. 反应可表示为X+3Y 2Z
2Z
C. 改变温度可以改变此反应的平衡常数
D. 增大压强使平衡向生成Z的方向移动,平衡常数增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省马鞍山市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列有关热化学方程式及其叙述正确的是
A. 氢气的燃烧热为285.5 kJ·mol-1,则水分解的热化学方程式为2H2O(l)===2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1
B. 已知2C(石墨,s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1,则石墨的燃烧热为110.5 kJ·mol-1
C. 已知N2(g)+3H2(g)  2NH3(g) ΔH=-92.4 kJ·mol-1,则在一定条件下将1 mol N2 和3 mol H2置于一密闭容器中充分反应后最多可放出92.4 kJ的热量
2NH3(g) ΔH=-92.4 kJ·mol-1,则在一定条件下将1 mol N2 和3 mol H2置于一密闭容器中充分反应后最多可放出92.4 kJ的热量
D. 已知乙醇和乙烯的燃烧热分别为1 366.8 kJ·mol-1和1 411.0 kJ·mol-1,则乙烯水化制乙醇的热化学方程式为C2H4(g)+H2O(l)===C2H5OH(l) ΔH=-44.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江省牡丹江市高一下学期开学检测化学试卷(解析版) 题型:选择题
配制一定物质的量浓度的H2SO4溶液时,造成所配溶液浓度偏高的原因可能是( )
A. 容量瓶中原来含有少量蒸馏水
B. 烧杯中稀释浓H2SO4后,未经冷却即转移至容量瓶并洗涤烧杯和玻璃棒后立即定容
C. 溶解浓H2SO4的烧杯没有洗涤
D. 向容量瓶中加水定容时眼睛一直仰视刻度线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com