
科目:高中化学 来源:不详 题型:填空题
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | | 有白色沉淀生成,证明待测液中含SO42-。 |
| 步骤② | | |
| 步骤③ | | |
| …… | | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
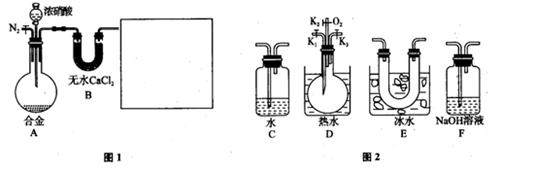
 _________________(2分).
_________________(2分).查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 名称 | 乙二酸 | 乙二酸晶体 |
| 分子式 | H2C2O4 | H2C2O4·2H2O |
| 颜色状态 | 无色固体 | 无色晶体 |
| 溶解度(g) | 8.6(20℃) | — |
| 熔点(℃) | 189.5 | 101.5 |
| 密度(g·cm-3) | 1.900 | 1.650 |
 华,157℃时大量升华,并开始分解。草酸钙不溶于水。根据上述材料提供的信息,回答下列问题:
华,157℃时大量升华,并开始分解。草酸钙不溶于水。根据上述材料提供的信息,回答下列问题: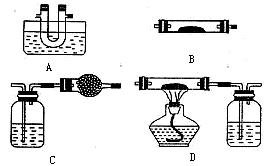
| A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色 |
| B.测定相同浓度的草酸和硫酸溶液的pH |
| C.测定草酸钠(Na2C2O4)溶液的pH |
| D.将草酸溶液加入Na2CO3溶液中,有CO2放出 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 生反应,设计并完成了如图所示
生反应,设计并完成了如图所示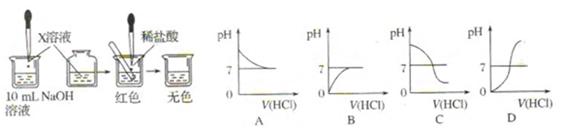
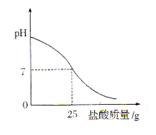
 试管中,用胶头滴管慢慢滴入稀盐酸,不断振荡溶液,同时测定溶液的pH,直至盐酸过量。
试管中,用胶头滴管慢慢滴入稀盐酸,不断振荡溶液,同时测定溶液的pH,直至盐酸过量。| 加入盐酸的 体积( 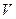 )/mL )/mL | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 |
| 溶液温度上升 | 5.2 | 9.6 | 12.0 | 16.0 | 18.2 | 16.7 | 15.7 | 14.7 | 13.7 |
 度上升与加入盐酸体积之间的变化关系图,并在曲线上画出能表示两者之间恰好完全反应的点,并用字母P表示。
度上升与加入盐酸体积之间的变化关系图,并在曲线上画出能表示两者之间恰好完全反应的点,并用字母P表示。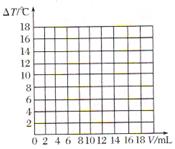
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
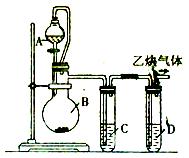
 化学方程式:__________________________。
化学方程式:__________________________。 ____________。
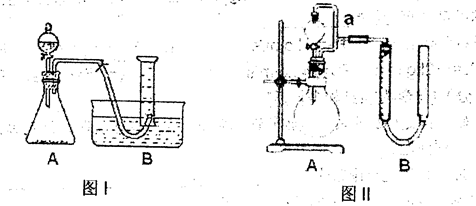
____________。 为了测量产生的乙炔气体的体积,该小组同学设计了下图所示的两种装置。则应选择装置_______
为了测量产生的乙炔气体的体积,该小组同学设计了下图所示的两种装置。则应选择装置_______ __(填Ⅰ或Ⅱ)。
__(填Ⅰ或Ⅱ)。
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
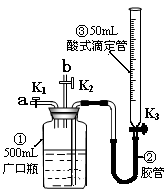
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com