
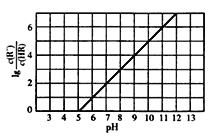
【题目】常温下,向lL0.lmol·L-1一元酸HR溶液中逐渐通人氨气[已知常温下Kb(NH3H2O)=1.76×10-5],使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如右图所示。下列叙述正确的是( )
A. 0.1 mol·L-1HR溶液的pH约为3
B. HR为弱酸,常温时Ka (HR)=1×l0-7
C. 当通入0.1molNH3时,c(R-)>c(NH4+)
D. 当c(HR) =c(R-)时,溶液必为中性
【答案】A
【解析】A.pH=5时,lg![]() =0,则
=0,则![]() = 1,说明HR在溶液中不能完全电离,HR是弱酸,根据HR
= 1,说明HR在溶液中不能完全电离,HR是弱酸,根据HR![]() H++R-可知,Ka(HR) =
H++R-可知,Ka(HR) = ![]() ,pH=5时,Ka(HR)=c(H+)=10-5mol/L,因溶液温度不变,则Ka始终不变。设0.1 mol·L-1HR溶液中H+的浓度为xmol/L,则Ka =
,pH=5时,Ka(HR)=c(H+)=10-5mol/L,因溶液温度不变,则Ka始终不变。设0.1 mol·L-1HR溶液中H+的浓度为xmol/L,则Ka = ![]() =
=![]() =10-5mol/L,解得x=10-3mol/L,则pH=-lgc(H+)=3,故A正确;B.根据A项分析可知,HR是弱酸,常温时Ka(HR)=10-5mol/L,故B错误;C. lL0.lmol·L-1一元酸HR溶液中n(HR)=0.1mol,当通入0.1molNH3 时,恰好与HR完全反应,得NH4R溶液,因Ka(HR)<Kb(NH3H2O),所以R-的水解程度大于NH4+的水解程度,则c(R-)<c(NH4+),故C错误;D.据图可知,当c(HR) =c(R-)时,lg
=10-5mol/L,解得x=10-3mol/L,则pH=-lgc(H+)=3,故A正确;B.根据A项分析可知,HR是弱酸,常温时Ka(HR)=10-5mol/L,故B错误;C. lL0.lmol·L-1一元酸HR溶液中n(HR)=0.1mol,当通入0.1molNH3 时,恰好与HR完全反应,得NH4R溶液,因Ka(HR)<Kb(NH3H2O),所以R-的水解程度大于NH4+的水解程度,则c(R-)<c(NH4+),故C错误;D.据图可知,当c(HR) =c(R-)时,lg![]() =0,pH=5,溶液成酸性,故D错误;答案选A。
=0,pH=5,溶液成酸性,故D错误;答案选A。


科目:高中化学 来源: 题型:
【题目】环丁基甲酸(![]() )是有机合成中一种重要的中间体。实验室以链状分子A为原料合成环丁基甲酸的路线如下:
)是有机合成中一种重要的中间体。实验室以链状分子A为原料合成环丁基甲酸的路线如下:
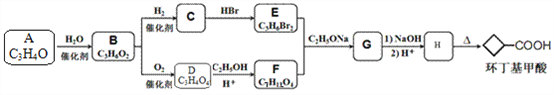
已知: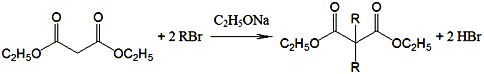
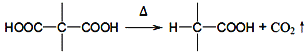
请回答下列问题:
(1)化合物A的化学名称是______,由A生成B的反应类型是_______。
(2)化合物B中所含官能团的名称为___________。
(3)化合物C和D反应所形成高聚物的结构简式是___________。
(4)写出E+F→G的化学方程式: ___________。
(5)X是环丁基甲酸的同分异构体,能与饱和碳酸氢钠溶液反应放出气体,且能使溴水褪色,X共有______种;其中核磁共振氢谱为三组峰,峰面积比为6:1:1的结构简式为___________。
(6)写出用1,3一丁二烯和化合物F为原料制备环戊基甲酸的合成路线___________。(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关各实验的叙述中正确的是
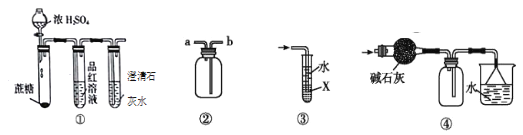
A. ①澄清石灰水变浑浊,证明蔗糖与浓硫酸反应生成了CO2
B. ②进行H2、NH3、CO2、Cl2、NO、NO2等气体的收集
C. ③当X选用苯时可进行NH3或HCl的吸收,并防止倒吸
D. ④可用于NH3的干燥,收集并吸收多余NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或有关化学用语的表达正确的是( )
A. 在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量
B. 基态Fe原子的外围电子排布图为![]()
C. 因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大
D. 根据原子核外电子排布的特点,Cu在元素周期表中位于s区
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组在实验室制取 Na2O2。查阅资料可知:钠与空气在 453473K 之间可生成 Na2O,迅速提高温度到 573673K 之间可生成 Na2O2,若温度提高到 733873K 之间 Na2O2 可分解。
(1)甲组设计制取 Na2O2 装置如图1。
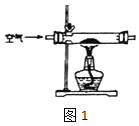
①使用该装置制取的 Na2O2 中可能含有的杂质为_____。.
A.NaCl B.Na2CO3 C.Na2O D.NaOH E.NaHCO3
②该小组为测定制得的 Na2O2 样品的纯度,设计可能用到的装置如图 2:烧瓶中发生的主要反应的化学方程式是_________。测定装置的接口从 左至右正确的连接顺序是_____。
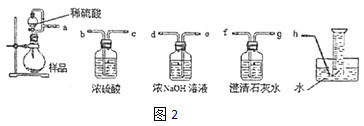
(2)乙组从反应历程上分析该测定反应存在中间产物,从而导致测定结果_____ (填“偏大”或“偏 小”)。为证明其分析的正确性,设计实验方案如下:
实验方案 | 产生的现象 |
Ⅰ.取烧瓶中的反应液加入少量 MnO2 粉末 | 有大量气泡逸出 |
Ⅱ.向 NaOH 稀溶液中加入 23 滴酚酞试液,然后加入少量的反应液 | 溶液先变红后褪色开始无明显现象。 |
Ⅲ.向反应液中加入 23 滴酚酞试液,充分振荡,然后逐滴加入 过量的 NaOH 稀溶液 | 加 NaOH 溶液先 变红后褪色 |
在上述实验中,能够证明乙组分析正确的最佳方案是_________ (填实验序号)。_______________组实验得不出结论,原因是_____。
(3)丙组根据上述提供的有关信息,设计一个方案可准确的测定样品的纯度。请简述实验操作和需 要测定的有关数据__________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)金晶体的最小重复单元(也称晶胞)是面心立方体,即在立方体的8个顶角各有一个金原子,各个面的中心有一个金原子。金晶体每个晶胞中含有________个金原子。
(2)金和铜可以形成多种金属化合物,其中一种的晶体结构如下图所示(为面心立方结构)。该金属化合物的化学式________。
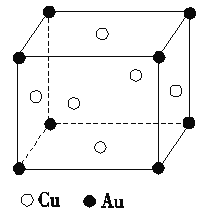
(3)1183 K以下纯铁晶体的基本结构单元如图1所示,1 183 K以上转变为图2所示结构的基本结构单元,在两种晶体中最邻近的铁原子等距离且最近的铁原子数为________个;在1 183 K以上的纯铁晶体中,与铁原子等距离且最近的铁原子数为________。
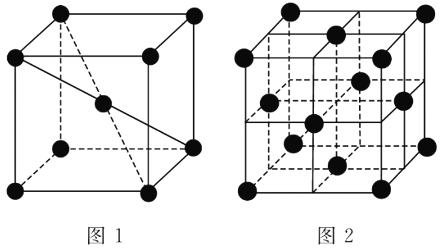
(4)如图为NaCl晶体结构图,图中直线交点处为NaCl晶体中Na+与Cl-所处的位置(不考虑体积的大小)。从晶胞中可以看出Na+周围与它最近时且距离相等的Na+共有________个。
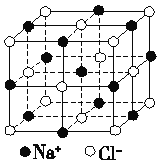
(5)某离子晶体晶胞结构如图所示,X位于立方体的顶点,Y位于立方体中心。试分析:
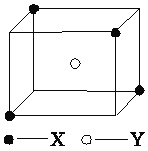
①晶体中每个Y同时吸引着________个X,每个X同时吸引着________个Y。
②晶体中在每个X周围与它最接近且距离相等的X共有________个。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中少量杂质所需除杂试剂及方法不正确的是( )
物质(杂质) | 除杂试剂 | 除杂方法 | |
A | 乙醇(水) | CaO | 蒸馏 |
B | 淀粉溶液(NaCl) | ——— | 渗析 |
C | CO2(HCl) | NaOH溶液 | 洗气 |
D | NaCl溶液(I2) | CCl4 | 萃取分液 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】长期以来一直认为氟的含氧酸不存在,但1971年美国科学家将F2通入细冰沫获得HFO(次氟酸)。
(1)HFO的电子式为________。
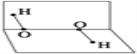
(2)HFO与水反应得到物质A(结构如图所示),写出HFO与水反应的化学方程式________________。
(3)分子A中存在________键。A.仅有σ键 B.仅有π键 C.同时含有σ键、π键 D.同时存在极性键和非极性键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com