
X和Y元素的原子,在化学反应中都容易失去电子而形成与Ne相同的电子层结构,已知X的原子序数比Y的原子序数大,下列说法中正确的是
A. X的金属性比Y的金属性强
B. X和Y都不能从水中置换出氢
C. Y元素的氢氧化物碱性比X元素的氢氧化物碱性弱
D. X元素的最高化合价比Y元素的最高化合价高
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案科目:高中化学 来源:2017届湖南省怀化市高三上学期期末化学试卷(解析版) 题型:选择题
下列实验中对应的现象以及结论都正确的是( )
选项 | 实验 | 现象 | 结论 |
A | 用洁净铂丝蘸取少量待测液在酒精灯火焰上灼烧 | 火焰呈现黄色 | 待测液中只含Na+,不含K+ |
B | 用铁作电极电解饱和食盐水 | 两极上均产生气体 | 阴、阳极分别生成H2和Cl2 |
C | 向饱和氯水中加人少量石灰石 | 产生无色气体 | 酸性:HClO>H2CO3 |
D | 向Ba(ClO)2溶液中 通入足量的SO2 | 产生不溶于稀盐酸的白色沉淀 | Ba(C1O)2具有氧化性 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高一上模拟考试化学卷(解析版) 题型:选择题
下列离子能大量共存的是
A.使 无色酚酞试液呈红色的溶液中:Na+、K+、SO
无色酚酞试液呈红色的溶液中:Na+、K+、SO 、CO
、CO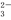
B.无色透明的溶液中:Cu2+、K+、SO 、NO
、NO
C.含有大量Ba(NO3)2的溶液中:Mg2 +、NH
+、NH 、SO
、SO 、Cl-
、Cl-
D.使紫色石蕊试液呈红色的溶液中:Na+、K+、CO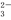 、NO
、NO
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上模拟考试化学卷(解析版) 题型:填空题
甘肃马家窑遗址出土的青铜刀是我国最早冶炼的青铜器,由于时间久远,其表面有一层“绿锈”,“绿锈”俗称“铜绿”,是铜和空气中的水蒸气、CO2、O2作用产生的,化学式为[Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐、CO2和H2O。某同学利用以下反应实现了“铜→铜绿→……→铜”的转化。

(1)从物质分类标准看,“铜绿”属于________(填字母)。
A.酸 B.碱 C.盐 D.氧化物
(2)写出B的化学式:_____________。
(3)请写出铜绿与盐酸反应的化学方程式:_______________________。
(4)上述转化过程中属于化合反应的是_____________,属于氧化还原 反应的是____________。
反应的是____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上模拟考试化学卷(解析版) 题型:选择题
1 mol X能与足量碳酸氢钠溶液反应放出44.8 L CO2(标准状况),则X的分子式是
A. C5H10O4 B. C4H8O4 C. C3H6O4 D. C2H2O4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上模拟考试化学卷(解析版) 题型:选择题
下列各元素的氧化物中,既能与盐酸反应生成盐和水,又能够与NaOH溶液反应生成盐和水的是
A. 元素W:它的焰色反应颜色呈紫色
B. 元素X:它的原子中M层比L层少2个电子族
C. 元素Y:它的二价阳离子核外电子总数与氩原子相同
D. 元素Z:位于元素周期表中的第三周期第ⅢA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省高二上模拟考试化学卷(解析版) 题型:选择题
标准状况下,将V L A气体(摩尔质量为M g·mol-1)溶于0.1 L水中,所得溶液密度为ρ g·cm-3,则此溶液的物质的量浓度(mol·L-1)为
A.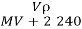
B.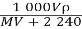
C.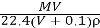
D.100VρM(MV+2240)
查看答案和解析>>
科目:高中化学 来源:2017届四川省绵阳市高三第二次诊断性考试化学试卷(解析版) 题型:选择题
常温下,用0.1000 mol/L的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示。下列有关叙述正确的是
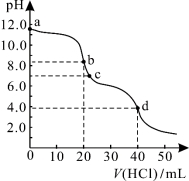
A.a点溶液呈碱性的原因用离子方程式表示为:CO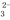 +2H2O
+2H2O H2CO3+2OH-
H2CO3+2OH-
B.c点处的溶液中c(Na+)-c(Cl-)=c(HCO )+2c(CO
)+2c(CO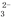 )
)
C.滴定过程中使用甲基橙作为指示剂比酚酞更准确
D.d点处溶液中水电离出的c(H+)大于b点处
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:实验题
活性氧化锌是一种多功能性的新型材料.某小组以粗氧化锌(含铁、铜的氧化物)为原料模拟工业生产活性氧化锌,步骤如下:
已知各相关氢氧化物沉淀pH范围如下表所示:
Zn(OH)2 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | |
开始沉淀pH | 5.4 | 7.0 | 2.3 | 4.7 |
完全沉淀pH | 8.0 | 9.0 | 4.1 | 6.7 |
步骤II中,在酸性溶液中加入KMnO4的作用是将Fe2+ 氧化成Fe3+,离子方程式为 ;
(2)用ZnO调节pH,以除去含铁杂质。检验沉淀是否完全的实验操作是 ;调节pH的适宜范围是 。
(3)步骤III中加入Zn粉的作用是① ,②进一步调节溶液PH值。
(4)用如下方法测定所得活性氧化锌的纯度(假设杂质不参与反应):
取1.000g活性氧化锌,用15.00mL 1.00mol/L硫酸溶液完全溶解,滴入几滴指示剂,再用0.50mol/L的标准氢氧化钠溶液滴定剩余硫酸,到达终点时消耗氢氧化钠溶液12.00mL,通过计算可以得到活性氧化锌的纯度,由表中Zn(OH)2PH变化可知,滴入的最理想的指示剂是 (填“酚酞”、“甲基橙”或“石蕊试剂”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com