
有 X
X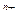 和
和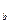 Y
Y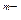 两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是
两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是
| A.X与Y处于同一周期 | B.原子序数:a<b |
| C.a-b=m+n | D.离子半径:X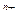 >Y >Y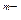 |
科目:高中化学 来源: 题型:
| 代号 | 结构简式 | 水中溶解度/g(25℃) | 熔点/℃ | 沸点/℃ |
| X | 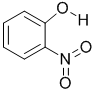 |
0.2 | 45 | 100 |
| Y | 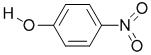 |
1.7 | 114 | 295 |

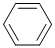 ④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是
④HCHO四种分子均能与H2发生加成反应,加成时这些分子中发生断裂的共价键的类型是查看答案和解析>>
科目:高中化学 来源: 题型:
(1)写出下列元素的元素符号:B________,D________;写出E的两种常见同素异形体的名称________;C、E的氢化物的沸点高低关系是________(用分子式和“>”表示)。
(2)X是C的最高价氧化物的水化物,它是重要的化学试剂,其浓溶液需避光保存,这是因为(用化学方程式表示)____________________________________。
(3)Y是C的最高价氧化物的水化物和其氢化物反应生成的化合物,常温时,pH=a的X、Y两种溶液中由水电离出来的H+浓度之比为__________________。
(4)X与A、B组成的某化合物在一定条件下反应制得一种常见的烈性炸药,其反应的化学方程式为____________________________________。
(5)由上述元素组成的某化合物其化学式为B
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
考生从两道化学题中各任选一题作答
1[化学——物质结构与性质]Q、R、X、Y、Z五种元素的原子序数依次递增。已知:
①Z的原子序数为29,其余的均为短周期主族元素;
②Y原子价电子(外围电子)排布为msnmpn;
③R原子核外L层电子数为奇数;
④Q、X原子p轨道的电子数分别为2和4。
请回答下列问题:
(1)Z2+的核外电子排布式是___________。
(2)在[Z(NH3)4]2+离子中,Z2+的空轨道接受NH3分子提供的_________形成配位键。
(3)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是_________。
a.稳定性:甲>乙,沸点:甲>乙 b.稳定性:甲>乙,沸点:甲<乙
c.稳定性:甲<乙,沸点:甲<乙 d.稳定性:甲<乙,沸点:甲>乙
(4)Q、R、Y三种元素的第一电离能数值由小至大的顺序为_________(用元素符号作答)。
(5)Q的一种氢化物相对分子质量为26,其分子中σ键与π键的键数之比为_________。
(6)五种元素中,电负性最大与最小的两种非金属元素形成的晶体属于_________(填晶体类型)。
2[化学——有机化学基础]有机物A是常用的食用油抗氧化剂,分子式为C10H12O5,可发生如下转化:
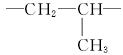
已知B的相对分子质量为60,分子中只含一个甲基。C的结构可表示为: 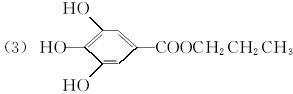 (其中:—X、—Y均为官能团)。
(其中:—X、—Y均为官能团)。
请回答下列问题:
(1)根据系统命名法,B的名称为________________。
(2)官能团—X的名称为____________,高聚物E的链节为____________。
(3)A的结构简式为________________________。
(4)反应⑤的化学方程式为____________________________________。
(5)C有多种同分异构体,写出其中2种符合下列要求的同分异构体的结构简式。
ⅰ.含有苯环 ⅱ.能发生银镜反应 ⅲ.不能发生水解反应
(6)从分子结构上看,A具有抗氧化作用的主要原因是____________(填序号)。
a.含有苯环 b.含有羰基 c.含有酚羟基
查看答案和解析>>
科目:高中化学 来源: 题型:
16.(12分)A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,A与D、C与F分别为同一主族,A、D两元素的原子核内的质子数之和是C、F两元素原子核内质子数之和的一半。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)B元素的原子结构简图____________,
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为 。
(3)E是非金属元素,但能表现出一些金属元素的性质,请写出工业上制取单质E的化学方程式 。
(4)一定条件下,B、E能形成用于制造轴承、永久模具的新型无机非金属材料,又查资料得知该材料与熔融的氢氧化钠能很快转变为硅酸盐和氨,该反应的化学方程式为______________。
(5)写出六种元素中所形成的常见单质,在常温常压下为气体的三种单质间两两反应的化学方程式,并注明反应条件
。
查看答案和解析>>
科目:高中化学 来源:2014届吉林省高一下学期期末考试化学试卷(解析版) 题型:推断题
已知W、X、Y、Z为四种短周期元素,原子序数逐渐增大。其中W形成的单质是自然界中最轻的气体;X原子的最外层电子数是次外层电子数的2倍;Y元素是地壳中含量最多的元素;Z元素是短周期中原子半径最大的元素。回答下列问题:
(1)X6W6的结构简式为 ,分子空间构型为 。
(2)Y与Z形成的两种常见化合物的电子式分别为 和
(3)由W、X、Y三种元素形成的最简式为XW2Y的化合物有A和B两种,其中A的相对分子质量是60,是日常生活中的一种调味品的主要成分,则A的结构简式为 ;B的相对分子质量是A的3倍,在正常人的血液里含有0.1%的B,则B的分子式 。将B物质的溶液与新制的Cu(OH)2悬浊液共热,观察到得现象是 。
(4)将B在酒化酶的作用下可制得另外一种具有特殊香味的液态有机物C,同时得到一种能导致温室效应的气体。写出该反应的化学方程式
(5)C是一种可以再生的清洁燃料,写出其燃烧的化学方程式
。C还可以在Cu或Ag的催化作用下被氧气氧化成具有刺激性气味的液体,该反应的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com