
将5mol/L的Mg(NO![]() )2溶液a mL稀释至b mL,稀释后溶液中NO
)2溶液a mL稀释至b mL,稀释后溶液中NO![]() 的物质的最浓度为( )
的物质的最浓度为( )
![]() A.5a/b mol/L B.10a/b mol/L C.b/5a mol/L D.a/b mol/L
A.5a/b mol/L B.10a/b mol/L C.b/5a mol/L D.a/b mol/L
科目:高中化学 来源:湖北省黄冈中学、襄樊五中2007届高三年级11月联考、化学试题 题型:038
| |||||||||||||||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
将5mol/L的Mg(NO3)2溶液a mL稀释至b mL,稀释后溶液中NO3-的物质的最浓度为
A.5a/b mol/L B.10a/b mol/L C.b/5a mol/L D.a/b mol/L
查看答案和解析>>
科目:高中化学 来源:2010—2011学年浙江省金华十校高二下学期期中考试化学试卷 题型:填空题
(9分)已知25℃时,CH3COOH和NH3·H2O的电离平衡常数分别为Ka(CH3COOH)=l.7×10-5mol/L,Kb(NH3·H2O)=1.7×l0-5mol/L。现有常温下1 mol/L的醋酸溶液和l mol/L的氨水,且知醋酸溶液的pH=a,试回答下列问题:
(1)醋酸溶液中存在的电离平衡用电离方程式表示为 ,
(2)将上述两种溶液等体积混合,所得溶液的pH= 。
(3)饱和氯化铵溶液显酸性,原因是(用离子方程式表示) ;向饱和氯化铵溶液中加入少量Mg(OH)2固体,固体完全溶解。甲、乙两位同学分别提出了不同的解释:
甲同学:由于NH4+水解呈酸性,其H+结合Mg(OH)2电离的OH-,使Mg(OH)2溶解
乙同学:由于Mg(OH)2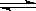 Mg2++2OH-,NH4++OH-
Mg2++2OH-,NH4++OH-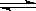 NH3·H2O,使Mg(OH)2溶解。请你设计一个实验验证两位同学的解释 。
NH3·H2O,使Mg(OH)2溶解。请你设计一个实验验证两位同学的解释 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com