
下列依据相关实验得出的结论正确的是( )
编号 实验 结论
A 向某溶液中加入稀盐酸,将产生的气体通入澄清石灰水,石灰水变浑浊 该溶液一定是碳酸盐溶液
B 用铂丝蘸取少量某溶液在酒精灯火焰上进行焰色反应,火焰呈黄色 该溶液不一定是钠盐溶液
C 往淀粉溶液中加稀硫酸,加热片刻,滴加银氨溶液并水浴加热,无银镜出现 该淀粉未发生水解
D 向某溶液中滴加KSCN 溶液,溶液不变色,滴加氯水后溶液显红色 该溶液中一定含Fe2+
A. A B. B C. C D. D
考点: 常见离子的检验方法.
分析: A、二氧化硫通入澄清石灰水也会变浑浊;
B、钾元素的焰色反应若不用钴玻璃也会发出黄色火焰;
C、银镜反应必须在碱性条件下进行;
D、依据亚铁离子的检验方法分析判断.
解答: 解:A、向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液可能是碳酸盐溶液或碳酸氢盐溶液或亚硫酸盐溶液,故A错误;
B、用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,钾元素的焰色反应若不用钴玻璃也会发出黄色火焰,该溶液可能是含钾元素的溶液,故B正确;
C、银镜反应必须在碱性条件下进行,在做银镜反应前没有中和过量的酸,所以实验不成功,不能说明淀粉是否水解,故C错误;
D、向某溶液中滴加KSCN 溶液,溶液不变色,说明不含铁离子,滴加氯水后溶液显红色,氯气氧化亚铁离子为铁离子,遇到硫氰酸钾溶液生成血红色溶液证明该溶液中一定含Fe2+,故D正确;
故选BD.
点评: 本题考查了常见离子检验方法和现象判断,主要是碳酸盐、亚硫酸盐、淀粉水解、亚铁离子等物质性质的分析应用,焰色反应的实验方法应用,题目难度中等.


 高中必刷题系列答案
高中必刷题系列答案科目:高中化学 来源: 题型:
将有机物完全燃烧,生成CO2和H2O.将12g该有机物完全燃烧后的产物通过浓H2SO4,浓H2SO4增重14.4g,再通过碱石灰,碱石灰增重26.4g.该有机物分子式为( )
A. C4H10 B. C2H6O C. C3H8O D. C2H4O2
查看答案和解析>>
科目:高中化学 来源: 题型:
用一种试剂就能鉴别乙醇、乙酸、乙醛、甲酸四种物质.该试剂可以是下列中的( )
A. 银氨溶液 B. 溴水
C. 碳酸钠溶液 D. 新制氢氧化铜悬浊液
查看答案和解析>>
科目:高中化学 来源: 题型:
将过量铁粉放入硝酸锌和硝酸银的混合溶液中,充分反应后过滤,滤液中的金属离子是( )
A. Fe2+ B. Fe2+、Zn2+ C. Fe2+、Ag+ D. Fe2+、Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液仅含Fe2+、Na+、Al3+、Ba2+、SO42﹣、NO3﹣、Cl﹣中的4种离子,所含离子的物质的量均为1mol.若向该溶液中加入过量的稀硫酸,有气泡产生,且溶液中阴离子种类不变(不考虑水的电离和离子的水解).下列说法不正确的是( )
A. 若向该溶液中加入过量的稀硫酸和KSCN溶液,溶液显血红色
B. 若向该溶液中加入过量的稀硫酸,产生的气体遇空气能变成红棕色
C. 该溶液中所含的离子是:Fe2+、Na+、SO42﹣、NO3﹣
D. 若向该溶液中加入足量的NaOH溶液,充分反应后,过滤、洗涤、灼烧,最终所得固体的质量为72g
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
阳离子 K+ Na+ Cu2+Al3+
阴离子 SO42﹣HCO3﹣NO3﹣ OH﹣
为了鉴别上述化合物.分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B为紫色(透过蓝色钴玻璃);
④在各溶液中加入硝酸钡溶液,再加过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀;
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验填空:
(1)写出B、D的化学式:B ,D .
将含1mol A的溶液与含1mol E的溶液反应后蒸干,仅得到一种化合物,该化合物的化学式为 .
(3)在A溶液中加少入量澄清石灰水,其离子方程式为 .
(4)C常用作净水剂,用离子方程式表示其净水原理 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某强酸性溶液X中仅含有Ba2+、Al3+、NH4+、Fe2+、Fe3+、CO32﹣、SO32﹣、SO42﹣、Cl﹣、NO3﹣中的一种或几种,取该溶液进行连续实验,实验过程如下:

根据以上信息,回答下列问题:
(1)仅根据上述连续实验不能确定溶液X中是否含有的阳、阴离子分别是
用离子方程表达下列反应:
①中生成气体A: .
②中生成溶液H: .
(3)若②中所用氢氧化钠浓度为2mol/L,当加入l0ml时开始产生沉淀,55ml时沉淀的量达到最大值0.03mol,继续滴加沉淀的量保持不变,随后再滴加沉淀部分溶解,到60ml时沉淀的量降为0.025mol且保持不变,则原溶液中c(Fe2+)为 mol/L、c(Fe3+)为 mol/L、c(Cl﹣)为 mol/L.(若有些离子不存在,请填0mol/L)
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应mA(s)+nB(g)⇌eC(g)+fD(g)反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度(T)和不同压强(p)的条件下随时间(t)的变化关系如图所示.下列叙述正确的是()

A. 达到平衡后,若使用催化剂,C的体积分数将增大
B. 达到平衡 后,增加A的质量,化学平衡向不移动
后,增加A的质量,化学平衡向不移动
C. 化学方程式中,n>e+f
D. 达到平衡后,若温度升高,化学平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
有下列各组物质:(A)S2和S4 (B)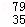 Br和
Br和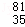 Br (C)CH4和C8H18(D) CH3﹣CH2﹣CH2﹣CH3和
Br (C)CH4和C8H18(D) CH3﹣CH2﹣CH2﹣CH3和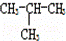
(E) 和
和
① 组两物质互为同位素
② 组两物质互为同素异形体
③ 组两物质互为同分异构体
④ 组两物质互为同系物
⑤ 组为同一物质.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com