
为测定某有机化合物A的结构,进行如下实验:
(一)分子式的确定:
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4g H2O和8.8g CO2,消耗氧气6.72L(标准状况下),则该物质中各元素的原子个数比是____________。
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为____________,该物质的分子式是____________。
(3)根据价键理论,预测A的可能结构并写出结构简式____________。
(二)结构式的确定:
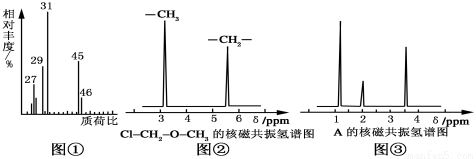
核 磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:甲基氯甲基醚(Cl2—CH2—O—CH3)有两种氢原子如图②。经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为__________________。
磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:甲基氯甲基醚(Cl2—CH2—O—CH3)有两种氢原子如图②。经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为__________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届湖南省岳阳市华容县四校高三联考二化学试卷(解析版) 题型:选择题
下列有关物质性质的描述和该性质的应用均正确的是( )
A.氨气具有氧化性,用浓氨水检验氯气管道是否泄漏
B.氢氟酸具有强酸性.用氢氟酸蚀刻玻璃
C.二氧化硫具有还原性,用二氧化硫水溶液吸收溴蒸气
D.铜的金属活动性比 铝弱,可用铜罐代替铝罐贮运浓硝酸
铝弱,可用铜罐代替铝罐贮运浓硝酸
查看答案和解析>>
科目:高中化学 来源:2017届北京市海淀区高三上学期期中化学试卷(解析版) 题型:选择题
柠檬中含有的柠檬酸(其结构简式如下)对鲜切苹果具有较好的保鲜效果,可以在一段时间内防止鲜切苹果表面变色。下列说法不正确的是

A.柠檬酸的分子式是C6H8O7
B.柠檬酸是易溶于水的有机物
C.柠檬酸分子中含有羧基和羟基
D.柠檬酸只能发生取代反应
查看答案和解析>>
科目:高中化学 来源:2017届北京市高三上学期期中化学试卷(解析版) 题型:选择题
铝自然形成的氧化膜易脱落。以硫酸为电解液,分别以石墨和铝材做阴、阳极材料,经过电解处理形成的氧化铝膜,抗蚀能力强。其制备的简要流程如右图。下列用来解释流程中反应的方程式不正确的是

A.碱洗目的是除去铝材表面的自然氧化膜:2OH-+Al2O3=2AlO2-+H2O
B.碱洗时铝材表面会出现气泡:2Al+2OH-+2H2O=2AlO2-+3H2↑
C.用稀氨水洗去耐蚀铝材表面的酸:NH3·H2O+H+=NH4++H2O
D.获得耐蚀铝材的电极反应为:4Al–12e-+3O2=2Al2O3
查看答案和解析>>
科目:高中化学 来源:2017届北京市高三上学期期中化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.两种二肽互为同分异构体,二者的水解产物可能相同
B.用溴水可以鉴别苯酚溶液、2,4-己二烯和甲苯
C.室温下,在水中的溶解度:甘油>苯酚>溴乙烷
D.核磁共振氢谱不能区分CH3CH2OH和CH3OCH3
查看答案和解析>>
科目:高中化学 来源:2017届湖南湖南省长沙市高三月考试卷三化学试卷(解析版) 题型:实验题
硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,是分析化学中重要的试剂,常用于代替硫酸亚铁。硫酸亚铁铵在500℃时隔绝空气加热完全分解。回答下列问题:
(1)硫酸亚铁铵隔绝空气加热完全分解,发生了氧化还原反应,固体产物可能有FeO和Fe2O3,气体产物可能有NH3、SO3、H2O、N2和 。
(2)为检验分解产物的成份,设计如图所示实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。
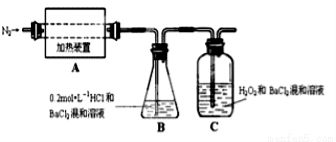
①A中固体充分加热较长时间后,通入氮气,目的是 。
②为验证A中残留物是否含有FeO,需要选用的试剂有 。
A.KSCN溶液
B.稀硫酸
C.浓盐酸
D.KMnO4溶液
③装置B中BaCl2溶液的作用是为了检验分解产物中是否有 气体生成,若含有该气体,观察到的现象为 。
④若A中分解产物有N2,固体残留物只有Fe2O3,Fe2O3的物质的量为bmol,C中沉淀物质的量为amol,则
b a(填“大于”、“小于”或“等于”)
⑤实验中,观察到C中有白色沉淀生成,则C中发生的反应为 (用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源:2017届湖南湖南省长沙市高三月考试卷三化学试卷(解析版) 题型:选择题
生活中的某些问题常常涉及化学知识,下列叙述错误的是
A.纯碱可用于制造玻璃,也可用于除去物品表面的油污
B.用聚氯乙烯代替木材生产包装盒、快餐盒等,以减少木材的使用
C.黄河人海口沙洲的形成和卤水点豆腐,都体现了胶体聚沉的性质
D.“煤改气”、“煤改电”等燃料改造工程有利于减少环境污染
查看答案和解析>>
科目:高中化学 来源:2017届江苏省徐州、宿迁、连云港、淮安四市高三11月模拟化学卷(解析版) 题型:选择题
80℃时,NO2(g)+SO2(g) SO3(g)+NO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列判断不正确的是( )
SO3(g)+NO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列判断不正确的是( )
起始浓度 | 甲 | 乙 | 丙 |
c(NO2)/mol ·L-1 | 0.10 | 0.20 | 0.20 |
c(SO2)/mol ·L-1 | 0.10 | 0.10 | 0.20 |
A.平衡时,乙中SO2的转化率大于50%
B.当反应平衡时,丙中c(SO2)是甲中的2倍
C.温度升至90℃,上述反应平衡常数为25/16,则正反应为吸热反应
D.其他条件不变,若起始时向容器乙中充入0.10mol ·L-1 NO2和0.20 mol ·L-1 SO2,达到平衡时c(NO)与原平衡不同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com