
科目:高中化学 来源:2016-2017学年江西省南昌市、洪都中学、麻丘中学、十七中、桑海中学高二3月联考化学试卷(解析版) 题型:简答题
Ⅰ某化合物的结构如图甲,,图乙是计算机软件模拟出的该分子氢原子的核磁共振波谱图,单位是ppm;氢原子在分子中的化学环境(原子之间相互作用)不同,在核磁谱图中就处于不同的位置,化学环境相同的氢原子越多,吸收峰面积(或高度)越大(或高).其核磁共振波谱图如:

参考上述结构式,分析核磁谱图,回答下列问题:
(1)分子中共有________种化学环境不同的氢原子;谱线最高者表示有________个环境相同的氢原子,谱线最低者表示有________个环境相同的氢原子。
(2)结构式中的Et—表示烷烃基,从图谱中可以推断结构式中的这个烷烃基是________________(写出结构简式)
Ⅱ某含氧有机化合物,它的相对分子质量为88.0,含C的质量分数为68.2%,含H的质量分数为13.6%,经红外光谱测定含有一个羟基,核磁共振氢谱显示该分子中有3个甲基,且有三种不同环境的氢原子。
(3)其分子式为_____________,结构简式为________________。
(4)其同分异构体中与其含有相同官能团的共有__________种(不含此有机物,填数字)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省枣庄市北校区高一下学期第一次月考化学试卷(解析版) 题型:选择题
依据元素周期表及元素周期律,下列推断正确的是
A. H3BO3的酸性比H2CO3的强
B. Mg(OH)2的碱性比Be(OH)2的强
C. HCl、HBr、HI的热稳定性依次增强
D. 若M+和R2-的核外电子层结构相同,则原子序数:R>M
查看答案和解析>>
科目:高中化学 来源:2017届安徽省安庆市高三第二次模拟考试理科综合化学试卷(解析版) 题型:选择题
新一代全固体锂离子电池使用硫化物固体电解质,利用薄层成膜技术和加压成型技术,提高了材料颗粒间的离子传导性,从而实现了无需机械加压的充放电。电池的工作原理为:LiMO2+nC Li1-xMO2+LixCn (M可以是Co、Ni、Fe等),内部结构如图所示。下列有关说法正确的是
Li1-xMO2+LixCn (M可以是Co、Ni、Fe等),内部结构如图所示。下列有关说法正确的是
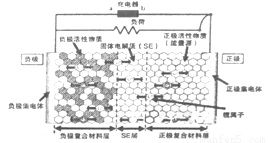
A. 电池放电时,负极发生的反应为:nC+xLi++xe-=LixCn
B. 充电器的a 端接电源的负极,b端接电源的正极
C. 电池充电时Li+自左向右移动
D. 电池工作时,固体电解质因熔融而导电
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古赤峰市宁城县高三一模理科综合化学试卷(解析版) 题型:简答题
氮是地球上含量丰富的一种元素,“固氮”在工农业生产中有着重要作用,是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分K值。
反应 | 大气固氮 N2(g)+O2(g) | 工业固氮 N2(g)+3H2(g) | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
K | 3.84×10-31 | 0.1 | 5×10-8 | 2×104 | 7×103 |
(1)①分析数据可知:大气固氮反应属于___________(填“吸热”或“放热”)反应。
②在一定温度下,将一定足的N2和O2通入到体积为1L的密闭容器中,当“大气固氮”反应达到平衡后,改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是_______。
a.增大压强 b.增大反应物的浓度 c.使用催化剂 d.升高温度
③ 从分子结构角度解释“大气固氮”和“工业固氮”反应的活化能都很高的原因:________。
(2)分析表格数据可知“大气固氮”的反应正向进行的程度小,不适合大规模生产,故世界各国均采用合成氨的方法进行工业固氮。
①从平衡移动角度考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因_______________________。
②将0.1molN2和0.1molH2通入一容积可变的容器中进行工业固氮反应,则下图所示N2的平衡转化率在不同压强(P1,P2)下随温度变化的曲线正确的是____________(填“A” 或“B”);比较P1、P2的大小关系________;若300℃、压强P2时达到平衡,容器容积恰为100L,则此状态下反应的平衡常数K=______________ (计算结果保留2位有效数字)。
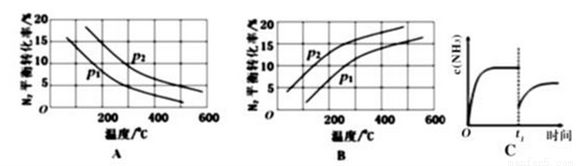
③合成氨反应达到平衡后,t1时刻氨气浓度欲发生图C变化可采取的措施是____________。

(3)近年近年,又有科学家提出在常温、常压、催化剂等条件下合成氨气的新思路,反应原理为:2N2(g)+6H2O(l)?4NH3(g)+3O2(g),则其反应热△H=____________。
(已知:N2(g)+3H2(g)?2NH3(g) △H1=-92.4kJ•mol-1;2H2(g)+O2(g)?2H2O(l) △H2=-571.6kJ•mol-1 )
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三2月模拟理科综合化学试卷(解析版) 题型:实验题
红矾钠(重铬酸钠: )是重要的基本化工原料,应用十分广泛。工业制备红矾钠的流程如下:
)是重要的基本化工原料,应用十分广泛。工业制备红矾钠的流程如下:

请回答下列问题:
(1) 的基态电子排布式为____________。
的基态电子排布式为____________。
(2)锻烧铬铁矿发生反应:____________ 配平上述化学反应方程式。
配平上述化学反应方程式。
(3)溶液甲中加入H2SO4时,可以观察到溶液由黄色变为橙色,并放出无色气体,有 关反应的离子方程式为____________。
(4)制备红矾钠的废水必须进行处理。首先酸化废水,将含+6价铬的酸性废液放入电解槽内,用铁作阳极进行电解,阴极析出H2,阳极产物被 氧化然后转化为Cr(OH)3、 Fe(0H)3 沉淀。
氧化然后转化为Cr(OH)3、 Fe(0H)3 沉淀。
①阳极的电极反应式为(不考虑后续反应):____________。
②溶液中金属离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因:______。
③已知某含 的酸性废水中Cr元素的含量是52.5mg/L,处理后Cr元素最高允许 排量为0.5 mg/L。要处理100 m3废水达到排放标准,至少消耗铁_____kg。
的酸性废水中Cr元素的含量是52.5mg/L,处理后Cr元素最高允许 排量为0.5 mg/L。要处理100 m3废水达到排放标准,至少消耗铁_____kg。
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三2月模拟理科综合化学试卷(解析版) 题型:选择题
“天宫一号”使用镍氢电池供电。镍氢电池的负极材料为储氢合金(用—表示,氢以单原子填入合金晶格),总反应为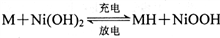 ,下列说法正确的是
,下列说法正确的是
A. 电池充电时氢原子被氧化
B. 电池放电时正极为NiOOH
C. 电池充电时,与电源负极相连的电极反应为:
D. 电池放电时,负极反应为:
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二2月联考化学试卷(解析版) 题型:选择题
将一定量的SO2(g)和O2(g)分别通入体积为2L的恒容密闭容器中,在不同温度下进行反应:2 SO2(g)+ O2(g) 2SO3(g) △H<0。得到如表中的两组数据:
2SO3(g) △H<0。得到如表中的两组数据:
实验编号 | 温度/℃ | 平衡常数/mol-1·L | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |||
SO2 | O2 | SO2 | O2 | |||||
1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 | |
2 | T2 | K2 | 4 | 2 | 0.4 | y | t | |
下列说法不正确的是( )
A. 实验1在前6min的平均反应速率υ(SO2)=0.2 mol·L-1·min-1
B. T1、T2的关系:T1 > T2
C. K1、K2的关系:K2>K1
D. x= 1.6,y=0.2 ,t<6
查看答案和解析>>
科目:高中化学 来源:2017届四川省成都市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
下列过程对应的离子方程式正确的是
A. 碳酸钠溶于水中:CO32-+2H2O H2CO3+2OH-
H2CO3+2OH-
B. 硫酸氢铵与少量氢氧化钠溶液混合共热:NH4++OH-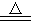 NH3↑+H2O
NH3↑+H2O
C. 氯化铝溶液中滴入过量浓氨水:Al3++4NH3·H2O==A1O2-+4 NH4++2H2O
D. 酸性高锰酸钾溶液与草酸溶液混合:5H2C2O4+6H++2MnO4- ==2Mn2++10CO2↑+8H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com