
【题目】一定条件下,体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g)![]() Z(g)(正反应为放热反应)该反应经过60 s时,生成0.3 mol Z,下列说法正确的是( )
Z(g)(正反应为放热反应)该反应经过60 s时,生成0.3 mol Z,下列说法正确的是( )
A.以X浓度变化表示的反应速率为0.01 mol·(L·s)-1
B.反应经过60 s时一定能达到化学平衡
C.反应放出的热量可用于提高反应速率
D.反应达到平衡时,n(X):n(Y)=1:1
 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】某化学小组以苯甲酸和异丙醇为原料,制取苯甲酸异丙酯(![]() ),已知有关物质的沸点如表:
),已知有关物质的沸点如表:

在如图圆底烧瓶中加入12.2g苯甲酸和30mL异丙醇(密度约为0.79g/cm3),再小心加入3mL浓硫酸,混匀后,加入几块碎瓷片,小心加热30分钟,使反应充分,得苯甲酸异丙酯粗产品。
![]()
(1)加入碎瓷片的作用是______,加入浓硫酸的作用是_____;
(2)若反应产物水分子中有同位素18O,写出能表示反应前后18O位置的化学反应方程式:_______;
(3)苯甲酸异丙酯粗产品中往往含有少量异丙醇、苯甲酸和水等,现拟用下列流程图进行精制,操作①中用到的一种重要玻璃仪器是_________;操作②的名称是__________。

(4)在进行操作②收集苯甲酸异丙酯时应控制的温度范围_______。
A.80℃~100℃ B.200℃~249℃ C.217℃~219℃ D.249℃以上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如下图,则此有机物可发生的反应类型有( )
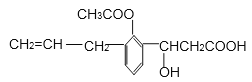
①取代 ②加成 ③消去 ④酯化 ⑤水解 ⑥氧化。
A. ①②③⑤⑥B. ②③④⑤⑥
C. ①②③④⑤D. ①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B都是芳香族化合物,1摩尔A水解得到1摩尔B和1摩尔醋酸。A、B的相对分子质量都不超过200,完全燃烧都只生成CO2和H2O,且B分子中碳和氢元素总的质量百分含量为65.2%。A的溶液具有酸性,不能使FeCl3溶液显色。
(1)A、B的分子量之差为____________
(2)A的分子式是___________________
(3)B可能的三种结构简式是____________ 、_____________ 、__________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素Ⅹ、Y、Z、W的原子序数依次增大,Ⅹ、W同主族且W原子核电荷数等于X原子核电荷数的2倍,Y、Z原子的核外电子数之和与Ⅹ、W原子的核外电子数之和相等。下列说法中一定正确的是
A. Ⅹ的原子半径比Y的原子半径大
B. Ⅹ形成的氢化物分子中不含非极性键
C. Z、W的最高价氧化物对应的水化物是酸
D. Y单质与水反应,水可能作氧化剂也可能作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2SO3+I2+H2O=H2SO4+2HI,将0.1molCl2通入100ml含等物质的量的HI与H2SO3的混合溶液中,有一半的HI被氧化,则下列说法正确的是
A.物质的还原性:HI>H2SO3>HCl
B.HI与H2SO3的物质的量浓度为0.6 mol·L-1
C.通入0.1molCl2发生反应的离子方程式为:5Cl2+4H2SO3+2I-+4H2O=4SO42-+I2+10Cl-+16H+
D.若再通入0.05molCl2,恰好能将HI和H2SO3完全氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】支撑海港码头基础的钢管桩,常用下图的方法进行防腐,工作原理如图所示,其中高硅铸铁为惰性辅助阳极。下列有关表述不正确的是( )

A. 该保护方法称为外加电流的阴极保护法
B. 通电后外电路电子被强制从高硅铸铁流向钢管柱
C. 高硅铸铁的作用是作为损耗阳极材料和传递电流
D. 通入的保护电流应该根据环境条件变化进行调整
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在半导体工业中有这样一句话:“从沙滩到用户”,其中由粗硅制纯硅的常用方法为:Si(粗)+2Cl2=SiCl4SiCl4+2H2=Si(纯)+4HCl。
若在25℃、101kPa条件下反应生成HCl气体49L,(注:25℃、101kPa条件下气体摩尔体积为24.5Lmol-1)则:
(1)反应生成HCl气体的质量为__,转移电子的总数为___。
(2)反应生成的HCl气体溶于127mL水中,得到密度为1.20gmL-1的盐酸,此盐酸的物质的量浓度为___。
(3)“从沙滩到用户”涉及多个反应,其中制取粗硅的反应方程式为___。纯净的石英与烧碱反应可以制得水玻璃,反应的离子方程式为__。
(4)普通玻璃若以氧化物形式表示其组成为(质量分数):Na2O13%,CaO11.7%,SiO275.3%。现以石灰石、纯碱和石英为原料生产这种玻璃10t,石灰石的利用率为80%,纯碱和石英的利用率为95%,至少需耍上述原料的质量是___t。(保留两位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com