
���÷Ͼ�п��Ƥ�Ʊ�����Fe3O4�������Ӽ�������ZnO��һ���Ʊ�����ͼ���£�

��1����NaOH��Һ�����Ͼ�п��Ƥ������Ӧ�Ļ�ѧ����ʽΪ____________��
��2��������ҺA�еμ�ϡH2SO4���������ܽ������Zn(OH)2���ɸ��õķ�����____________��
����Zn(OH)2������ZnOǰ�����ϴ�ӣ��������ϴ���Ƿ�ɾ��ķ�����______________��
��3�������м���NaC1O3������Ӧ�����ӷ���ʽΪ______________��
��4��������ҺB�Ƶ�Fe3O4�������ӵĹ�����ͨ��N2��ԭ����____________��
����ҺB����Ҫ���������ӷ�Ӧ����ʽΪ________________��
��ȷ����ҺB�к���Fe2+��ʵ�鷽����_____________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017�����ɹŰ�ͷ�и�����ѧ�ڵ�һ��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
����п�̸ɵ���ڵĺ�ɫ����ˮ�����̼������(��MnO2��C��Hg2+�ȣ���ȡMnSO4 • H2O ��ʵ���������£�

��֪:25��ʱ������������ܶȻ���������:
���� | FeS | MnS | HgS |
�ܶȻ� | 5.0��l0-18 | 4.6��l0-14 | 2.2��l0-54 |
25��ʱ�����ֽ���������������������ʽ����ʱ��Һ��pH���±���ʾ:
������ | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
��ʼ������pH | 2.7 | 7.6 | 8.3 |
��ȫ������pH | 3.7 | 9.7 | 9.8 |
��1�����������У�����ʵ�����ʱ�õ��Ĺ����β��ʵ�������______________��
��2���ڼ��������¡���ȡ������ԭ����__________________����ȡʱ����MnSO4��Fe2(SO4)3�Ļ�ѧ����ʽΪ__________________________��
��3������I�ijɷ�ΪMnO2��C��____________(�ѧʽ��������ȡ��Ӧ��25��ʱ���У�FeS���������ֽ�ȡ����Һ�е�c(Hg2+)/C(Fe2+)= ____________(����ֵ����
��4����������ʱ�����ӷ���ʽΪ____________������ʱ����H2O2����MnO2��H2O2�ĵ���ʽΪ_______��
��5���к�ʱ��Ӧ�õ�����ҺpH�ķ�Χ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�����и�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
��ͼ�Ǹ��ֲ�ͬ�ܶȵ�����������Ӧ����ͬ�¶ȣ�ʱ��Ҫ��ԭ����ķֲ�ͼ���������ͼ�������ش��й����⡣

(1)������������ȷ���ǣ�����ţ�_______________��
A.ͼ�к�������������ܶȣ�������ܶ�Խ����Ũ��ԽС��
B.����ԭ�����¶���ͬʱ����ͬŨ�ȵ����ᱻ��ԭ�IJ��ﲻ�ǵ�һ�ģ�ֻ����ijŨ��ʱ����ij�ֲ���Ϊ�����ѡ�
C.�����Ũ��Խ��ԭ������NԪ�صͻ��ϼ۲���Խ��
D.�������ܶȴ���1.3g��cm-3ʱ����ԭ������ҪΪNO��NO2
(2)����ͼ��ѡ��������ҩƷ��֤��������1.36 g��cm-3���ᷴӦ�����������к���NO��N2��O2�����������ɿ��ƣ�����װ�ú̶�װ��ʡ�ԣ�

��֪����.NO+NO2+2OH-=2NO2-+H2O
��.�����£�NO2��N2O4��ϴ��ڣ���0��ʱ����ֻ����ɫ��N2O4Һ�������ڡ�
������������˳����������ӣ�����ӿڵı�ţ�Ϊ______________��
�ڷ�Ӧǰ��ͨ��N2��Ŀ����___________________��
��ȷ�������к���������__________________��
��װ��F��������________________��
������A�����Ļ��������NO2��NO������ֱ�ΪV1mL��V2mL��V1��V2����Ϊ0�����ұ���װ�������ܽ�������������ȫ���գ���װ����������Ҫ�������������Ϊ��________mL����ͬ״̬�£���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�����и�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���н�����ʵ�����ӷ���ʽ����ȷ����
A��Na����ˮ�У��������壺2Na + 2H2O �� 2Na+ + 2OH�� + H2��
B��FeCl3��Һ���ڵ��۵⻯����ֽ�ϣ���ֽ������2Fe3+ + 2I���� 2Fe2+ + I2
C��������ϡ���ᣬ��Һ��ƣ�3Fe + 8H+ + 2NO3���� 3Fe2+ + 2NO��+ 4H2O
D��AlƬ����NaOH��Һ�У��������壺2Al + 2OH��+ 2H2O �� 2AlO2�� + 3H2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ��ͨ�и����߿�ȫ��ģ�⣨�壩��ѧ �Ծ��������棩 ���ͣ������
���������仯��������Ҫ�Ĵ����ͺϽ���ϡ�
��1����̬Vԭ�ӵļ۲�����Ų�ʽΪ________�������Ų�ʱ������ߵĵ�����ռ���ܼ���ԭ�ӹ����________����չ����
��2��VO2+��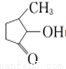 �������
���γ����� �У����ַǽ���ԭ�ӵĵ�һ�������ɴ�С��˳��Ϊ________����Ԫ�ط��ű�ʾ����Cԭ�ӵ��ӻ��������Ϊ_________��
�У����ַǽ���ԭ�ӵĵ�һ�������ɴ�С��˳��Ϊ________����Ԫ�ط��ű�ʾ����Cԭ�ӵ��ӻ��������Ϊ_________��
��3�����γɵ�[Ni(NH3)6]2+��[Ni(CN)4]2-�У�NH3������Nԭ�ӵļ۲���Ӷ���ĿΪ______����CN-��Ϊ�ȵ������һ�ַ��ӵĻ�ѧʽΪ__________��
��4��La-Ni�Ͻ�����Ҫ�Ĵ�����ϣ������ľ�����ͼ��ʾ��

�ٺϽ��У�1��Laԭ����Χ�����������ȵ�Laԭ����ĿΪ_______��
�ں���1mol Niԭ�ӵĺϽ��д���H2�����ʵ���Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ��ͨ�и����߿�ȫ��ģ�⣨�壩��ѧ �Ծ��������棩 ���ͣ�ѡ����
�����֢��һ�������Ұ����������ڷ�������л���Ŵ������Ұ���������������ת����

����˵��������ǣ� ��
A. �Ұ�����������ᷴӦ��������NaOH��Һ��Ӧ
B. 1mol�����������Ũ��ˮ��Ӧ���������3molBr2
C. ���ǻ�����ͪ���������ͬһƽ���ϵ�̼ԭ��������7��
D. ���ǻ�����ͪ����Ӻ˴Ź���������4���壬��1������̼ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ��ͨ�и����߿�ȫ��ģ�⣨�壩��ѧ �Ծ��������棩 ���ͣ�ѡ����
���ֶ���������Ԫ��W��X��Y��Z��ԭ��������������W��X�ļ����Ӿ�����ͬ���Ӳ�ṹ��X��ԭ�Ӱ뾶�Ƕ���������Ԫ��ԭ�������ģ�W��Yͬ�壬Z��X�γɵ����ӻ������ˮ��Һ�����ԡ�����˵����ȷ���ǣ� ��
A. �����Ӱ뾶��W<X<Z B. W��X�γɵĻ���������ˮ����Һ�ʼ���
C. ��̬�⻯������ȶ��ԣ�W<Y D. ����������ˮ��������ԣ�Y>Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�긣��ʡ���ݰ�һ�С�Ȫ��ʵ����ѧ��һ��ѧ����ĩ������ѧ�Ծ��������棩 ���ͣ������
���а������ʣ����� ��������A12O3 ��H2SO4 ��ϡ�����ϡ��ˮ��Ba(OH)2�����A12(SO4)3�밴Ҫ��ش��������⣺
��1�����ڵ���ʵ���______________������ţ���
��2��m mol �ڵ�����Ϊa g����b g�������ڱ�״���µ����Ϊ_______L (��m��a��b��ʾ) ��
��3��17.1g ������ˮ���500mL��Һ������Һ��SO42�������ʵ���Ũ��Ϊ__________��
��4��д����������ȡAl(OH)3�����ӷ���ʽ��__________________��
��5����������Һ�䷢����Ӧ�����ӷ���ʽΪH++ OH�D �� H2O����д���÷�Ӧ�Ļ�ѧ����ʽ��______________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ��һ��ѧ�ڵ�һ�Σ�3�£��μ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
���������Ȼ�ѧ����ʽ�ó��Ľ�����ȷ����( )
A. ��֪2H2(g)��O2(g)=2H2O(g) ��H��-483.6kJ��mol-1����������ȼ����Ϊ241.8kJ��mol-1
B. ��֪NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)����H��-57.4kJ��mol-1 ��20.0gNaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�����28.7kJ������
C. ��֪C(ʯī��s)=C(���ʯ��s) ����H>0����ʯī�Ƚ��ʯ�ȶ�
D. ��֪2C(s)+2O2(g)=2CO2(g)����H=a��2C(s)+O2(g)=2CO (g)����H=b ��a>b
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com