
解析:NaOH和NaHCO3的固体混合物在加热条件下,先发生酸式盐和碱的中和反应:
NaHCO3+NaOH![]() Na2CO3+H2O↑ ①
Na2CO3+H2O↑ ①
若NaOH过量,则只发生反应①;若NaHCO3过量,则过量的NaHCO3继续受热分解,发生反应:
2NaHCO3![]() Na2CO3+H2O↑+CO2↑ ②
Na2CO3+H2O↑+CO2↑ ②
因此,计算前,必须先根据反应①的质量差判断NaHCO3是否过量。
![]()
124 18
18.4 g x
解得 x=2.67 g
若实际质量差=2.67 g,则NaHCO3、NaOH恰好完全反应;
若实际质量差>2.67 g,则NaHCO3过量,发生反应①和②;
若实际质量差<2.67 g,则NaOH过量,只发生反应①。
现实际固体质量差为18.4 g-16.6 g=1.8 g<2.67 g,则NaOH过量,按不足量的NaHCO3计算。设NaHCO3质量为y。
NaHCO3+NaOH====Na2CO3+H2O↑ Δm
84 18
y ![]()
![]() =18.4 g-16.6 g=1.8 g
=18.4 g-16.6 g=1.8 g
解得 y=8.4 g
m(NaOH)=18.4 g-8.4 g=10.0 g
w(NaOH)=![]() ×100%=54.3%。
×100%=54.3%。
答案:54.3%


科目:高中化学 来源: 题型:阅读理解
 (2012?信阳二模)如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.
(2012?信阳二模)如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视.为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究.
查看答案和解析>>
科目:高中化学 来源: 题型:
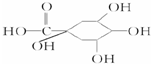
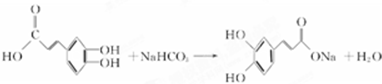
 (2012?长春三模)[化学-选修 有机化学基础]注射用双黄链以绿原酸为主要成分(其结构如图)绿原酸有广泛的药理作用.
(2012?长春三模)[化学-选修 有机化学基础]注射用双黄链以绿原酸为主要成分(其结构如图)绿原酸有广泛的药理作用.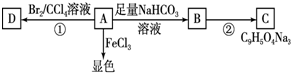


| a |
| 112 |
| b |
| 90 |
| a |
| 112 |
| b |
| 90 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
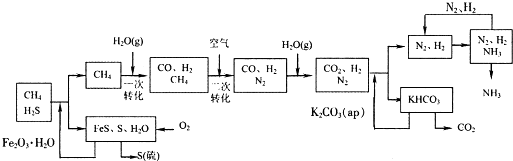
 (2011?南平二模)火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的.
(2011?南平二模)火力发电厂释放出大量的氮氧化物(NOx)、二氧化硫和二氧化碳等气体会造成环境污染.对燃煤废气进行脱硝、脱硫和脱碳等处理,可实现绿色环保、节能减排、废物利用等目的.
 NH3?H2O+H+
NH3?H2O+H+ NH3?H2O+H+
NH3?H2O+H+查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com