
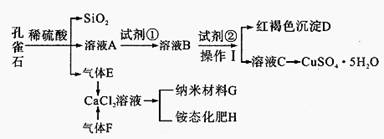
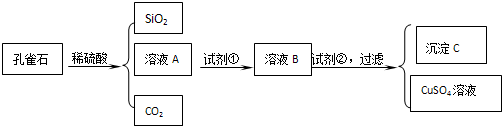
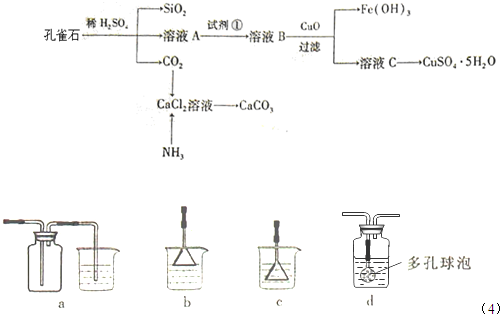
孔雀石主要含Cu2 (OH)2CO3,还含少量Fe、Si的化合物。某工厂以孔雀石为主要原料制备CuSO4·5 H2O及纳米材料G,主要步骤如下:
已知该条件下,通过调节溶液的酸碱性而使Fe3+、Fe2+、Cu2+生成沉淀的pH分别如下:
|
物质 |
开始沉淀时的pH |
完全沉淀时的pH |
|
Fe(OH)3 |
2.2 |
3.2 |
|
Fe(OH)2 |
7.6 |
9.6 |
|
Cu(OH)2 |
4.7 |
6.4 |
请回答下列问题:
(1)写出孔雀石主要成分Cu2(OH)2CO3与稀硫酸反应的化学方程式 。
(2)溶液A的金属离子有Cu2+、Fe2+、Fe3+。要检验其中的Fe2+应选择下列试剂中的 。
a.KMnO4 b.NaOH c.H2O2 d.KSCN
(3)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。试剂①是一种氧化剂,把Fe2+氧化成Fe3+的目的是 。该工厂选用试剂①最好为下列中的 (填代号)。
a.H2O2 b.空气 c.Cl2 d.KSCN
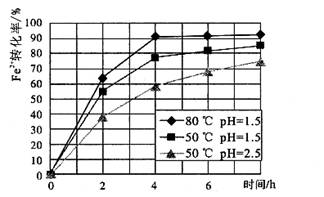
(4)根据下图有关数据,你认为工业上氧化操作时应采取的措施是 。
(5)向溶液B中加入试剂②的化学式为 ,操作I的名称是 。
(6)气体E和气体F应该先通人CaCl2溶液中的是 (填化学式)。写出制备G和H的化学反应方程式 。
(7)欲测定溶液A中Fe2+的浓度,可用KMnO4标准溶液滴定,反应中MnO4-还原为Mn2+,则该反应的离子方程式为 。取A溶液20.00 mL,用去0.0240mol/LKMnO4溶液16.00 mL时,恰好达到滴定终点,则A溶液中Fe2+浓度为 。
(1)Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑(2分)
(2)a(1分)
(3)调节溶液的PH时,Fe3+在Cu2+开始沉淀之前就能沉淀完全,从而把铁杂质除去(1分)
a(1分)
(4)溶液温度控制在80℃,PH控制在1.5,氧化时间为4小时左右(1分)
(5)CuO(1分) 过滤(1分)
(6)NH3(1分) 2NH3+CO2+CaCl2+H2O==CaCO3↓+2NH4Cl(2分)
(7)MnO4- + 5Fe2+ + 8H+=== Mn2+ + 5Fe3+ + 4H2O(2分) 0.0960mol/L(2分)
【解析】(1)Cu2(OH)2CO3属于碱式盐,和稀硫酸反应生成硫酸铜、CO2和水,反应式为Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑。
(2)亚铁离子具有还原性,能使酸性高锰酸钾溶液褪色,所以可选择a。
(3)要制备硫酸铜,则必须出去铁离子和亚铁离子。根据表中数据可知要通过沉淀法直接出去亚铁离子,则铜离子也将被同时除去,所以应该把亚铁离子氧化生成铁离子,然后再通过沉淀法出铁离子。因为当氢氧化铁完全沉淀后,铜离子还留在溶液中。所选择的氧化剂不能再引入新的杂质,所以应该选择绿色氧化剂双氧水。
(4)根据图像可知,在80℃pH等于1.5时转化率最高,所以应该控制的条件就是溶液温度控制在80℃,PH控制在1.5,氧化时间为4小时左右。
(5)要得到氢氧化铁沉淀,就有增大溶液的pH,同时还不能引入杂质,所以可选择氧化铜。要分离固液混合物,需要过滤。
(6)E是CO2,CO2和氯化钙是不反应的,要得到碳酸钙沉淀,就降低溶液的酸性,因此首先通入氨气,使溶液显碱性,然后在通入CO2即可生成碳酸钙和氯化铵。反应式为2NH3+CO2+CaCl2+H2O==CaCO3↓+2NH4Cl。
(7)参加反应的高锰酸钾是0.0240mol/L×0.016L=0.000384mol,高锰酸钾氧化亚铁离子的方程式为MnO4-
+ 5Fe2+ + 8H+=== Mn2+ +
5Fe3+ + 4H2O,所以消耗的亚铁离子为0.000384mol×5=0.00192mol,所以浓度为 。
。


科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:

| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 2.7 | 3.7 |
| Fe2+ | 7.6 | 9.6 |
| Cu2+ | 4.7 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com