
【题目】下列各组顺序的排列不正确的是( )
A. 热稳定性:HCl>H2S>PH3
B. 离子半径:Na+>Mg2+>Al3+>F-
C. 碱性强弱:KOH>NaOH>Mg(OH)2>Al(OH)3
D. 酸性强弱:H2SO4>H2CO3>H2SiO3
科目:高中化学 来源:2017届江苏省南通市高三高考全真模拟(四)化学 试卷(解析版) 题型:简答题
三氯氧磷(POCl3)常温下为无色液体,有广泛应用。近年来三氯氧磷的工业生产由三氯化磷的“氧气直接氧化法”代替传统的三氯化磷“氯化水解法”(由氯气、三氯化磷和水为原料反应得到)。
(1)氧气直接氧化法产生三氯氧磷的化学方程式是________________;从原理上看,与氯化水解法相比,其优点是____________________。
(2)氯化水解法生产三氯氧磷会产生含磷(主要为H3PO4、H3PO3等)废水。在废水中先加入适量漂白粉,再加入生石灰将磷元素转化为磷酸的钙盐沉淀并回收。
①漂白粉的主要作用是__________________________。
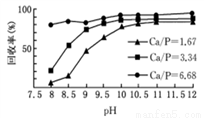
②下图表示不同条件下对磷的沉淀回收率的影响(“Ca/P”表示钙磷比,及溶液中Ca2+与PO43-的浓度比),则回收时加入生石灰的目的是__________________________。
(3)下述方法可以测定三氯氧磷产品中氯元素含量,实验步骤如下:
Ⅰ.先向一定量产品中加入足量NaOH溶液,使产品中的氯元素完全转化为Cl-;
Ⅱ._________________________;
Ⅲ.再加入少量硝基苯并振荡,使其覆盖沉淀,避免沉淀与水溶液接触;
Ⅳ.最终加入几滴NH4Fe(SO4)2溶液后,用NH4SCN溶液沉淀溶液中过量的Ag+,并记录NH4SCN的用量。
已知相同条件下的溶解度:AgSCN<AgCl。
①步骤Ⅱ的操作为_______________________。
步骤Ⅳ中当溶液颜色变为____________色时,即表明溶液中的Ag+恰好沉淀完全
②若取消步骤Ⅲ,会使步骤Ⅳ中增加一个化学反应,该反应的离子方程式是________________;该反应使测定结果偏低,运用平衡原理解释器原因:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 12C、13C、14C、金刚石、石墨都是碳元素的同位素
B. 互为同位素的原子,质子数一定相同
C. 同种元素的原子,质量数一定相同
D. 由一种元素组成的物质,一定是纯净物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列顺序排列不正确的是( )
A. 热稳定性:H2O>HF>H2S B. 原子半径:Na>Mg>O
C. 酸性:HClO4>H2SO4>H3PO4 D. 非金属性:F>Cl>Br
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y为短周期元素,X位于IA族,X与Y可形成化合物X2Y,下列说法正确的是( )
A.X的原子半径一定大于Y的原子半径
B.X与Y的简单离子不可能具有相同的电子层结构
C.两元素形成的化合物中,原子个数比不可能为1 :1
D.X2Y可能是离子化合物,也可能是共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向四个体积相同的密闭容器中分别充入一定量的SO2和O2, 开始反应时, 按正反应速率由大到小的顺序排列, 正确的是
①500 ℃, 10 mol SO2和5 mol O2反应
②500 ℃, 用V2O5作催化剂, 10 mol SO2和5 mol O2反应;
③450 ℃, 8 mol SO2和5 mol O2反应
④500 ℃, 8 mol SO2和5 mol O2反应。
A.①②③④ B.②①③④ C.②①④③ D.④③②①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是
A.构成原电池的正极和负极的材料必须是两种金属
B.由铜、锌作电极与硫酸铜溶液组成的原电池中铜是负极
C.马口铁(镀锡铁)破损时与电解质溶液接触时锡先被腐蚀
D.铜锌原电池工作时,若有13 g锌被溶解,电路中就有0.4 mol电子通过
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为检验某卤代烃中的卤元素,进行如下操作,正确的顺序是( )
①加热 ②加入 AgNO3溶液 ③取少量该卤化物 ④加入足量稀硝酸酸化 ⑤加入NaOH溶液 ⑥冷却
A.③①⑤⑥②④ B.③⑤①⑥④②
C.③②①⑥④⑤ D.③⑤①⑥②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对热化学方程式C(s)+H2O(g)===CO(g)+H2(g) ΔH =+131.3 kJ·mol-1最准确的理解是
A.碳和水反应吸收131.3 kJ热量
B.1 mol碳和1 mol水反应生成一氧化碳和氢气,同时放出131.3 kJ热量
C.1 mol碳和1 mol水蒸气反应生成1 mol CO和1 mol H2,同时吸收131.3 kJ热量
D.1个固态碳原子和1分子水蒸气反应吸热131.1 kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com