
【题目】一定温度下,在2L恒容密闭容器中发生反应:2N2O5(g) ![]() 4NO2(g)+ O2(g),反应吸热。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示,下列说法正确的是( )
4NO2(g)+ O2(g),反应吸热。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示,下列说法正确的是( )
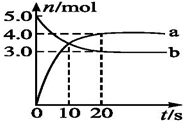
A.10min时,反应达到平衡
B.曲线a表示NO2的物质的量随反应时间的变化
C.0~20min内平均反应速率v(N2O5)=0.1molL-1min-1
D.达到平衡时,N2O5的转化率为60%
【答案】B
【解析】
试题分析:A、10min时,反应中的有关物质的物质的量还在变化,所以反应未达平衡状态,故A错误;B、在反应2N2O5(g)![]() 4NO2(g)+O2(g)中N2O5为反应物,NO2为生成物,它们的计量数之比为1:2,也就是说NO2增加的物质的量是N2O5减小的物质的量的两倍,结合图中的数据可知曲线a表示NO2的物质的量随反应时间的变化,曲线b表示N2O5的物质的量随反应时间的变化,故B正确;C、在反应2N2O5(g)
4NO2(g)+O2(g)中N2O5为反应物,NO2为生成物,它们的计量数之比为1:2,也就是说NO2增加的物质的量是N2O5减小的物质的量的两倍,结合图中的数据可知曲线a表示NO2的物质的量随反应时间的变化,曲线b表示N2O5的物质的量随反应时间的变化,故B正确;C、在反应2N2O5(g)![]() 4NO2(g)+O2(g)中N2O5为反应物NO2为生成物,它们的计量数之比为1:2,也就是说NO2增加的物质的量是N2O5减小的物质的量的两倍,所以曲线a表示NO2的物质的量随反应时间的变化,曲线b表示N2O5的物质的量随反应时间的变化,根据v=
4NO2(g)+O2(g)中N2O5为反应物NO2为生成物,它们的计量数之比为1:2,也就是说NO2增加的物质的量是N2O5减小的物质的量的两倍,所以曲线a表示NO2的物质的量随反应时间的变化,曲线b表示N2O5的物质的量随反应时间的变化,根据v= ![]() =
=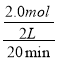 = 0.05 mol(Lmin)-1,故C错误;D、在反应2N2O5(g)
= 0.05 mol(Lmin)-1,故C错误;D、在反应2N2O5(g)![]() 4NO2(g)+O2(g)中N2O5为反应物NO2为生成物,它们的计量数之比为1:2,也就是说NO2增加的物质的量是N2O5减小的物质的量的两倍,所以曲线a表示NO2的物质的量随反应时间的变化,曲线b表示N2O5的物质的量随反应时间的变化,根据图象可知,达到平衡时N2O5的物质的量的变化量是2mol,所以N2O5的转化率为
4NO2(g)+O2(g)中N2O5为反应物NO2为生成物,它们的计量数之比为1:2,也就是说NO2增加的物质的量是N2O5减小的物质的量的两倍,所以曲线a表示NO2的物质的量随反应时间的变化,曲线b表示N2O5的物质的量随反应时间的变化,根据图象可知,达到平衡时N2O5的物质的量的变化量是2mol,所以N2O5的转化率为![]() ×100%=40%,故D错误;故选B。
×100%=40%,故D错误;故选B。


科目:高中化学 来源: 题型:
【题目】H2C2O4为二元弱酸。20℃时,配制一组c(H2C2O4)+ c(HC2O4–)+ c(C2O42–)=0.100 mol·L–1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示。下列指定溶液中微粒的物质的量浓度关系一定正确的是

A.pH=2.5的溶液中:c(H2C2O4)+c(C2O42–)>c(HC2O4–)
B.c(Na+)=0.100 mol·L–1的溶液中:c(H+)+c(H2C2O4)=c(OH–)+c(C2O42–)
C.c(HC2O4–)=c(C2O42–)的溶液中:c(Na+)>0.100 mol·L–1+c(HC2O4–)
D.pH=7的溶液中:c(Na+)<2c(C2O42–)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠是重要的防腐剂。某化学兴趣小组以碳和浓硝酸为起始原料,设计如下装置利 用一氧化氮与过氧化钠反应制备亚硝酸钠。(夹持装置和A中加热装置已略,气密性已检验),查阅资料:①HNO2为弱酸,室温下存在反应3HNO2=HNO3+2NO↑+H2O;
②在酸性溶液中,NO2-可将MnO4-还原为Mn2+。
③NO不与碱反应,可被酸性KMnO4溶液氧化为硝酸
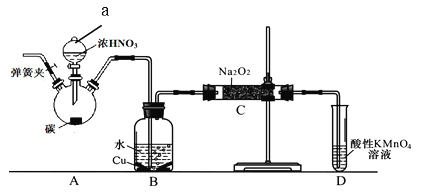
实验操作:①关闭弹簧夹,打开A中分液漏斗活塞,滴加一定量浓硝酸,加热;
②一段时间后停止加热;③从C中取少量固体,检验是否是亚硝酸钠。
回答下列问题:
(1)装置中仪器a的名称为 ;D装置的作用是 。
(2)A中反应的化学方程式是 ;C中反应生成NaNO2的化学方程式是 。
(3)检验C中产物有亚硝酸钠的正确操作是 。
a.取少量生成物溶于水充分振荡,滴加酚酞试液,若溶液变红,则含有NaNO2。
b.取少量生成物溶于稀硫酸,若产生无色气体并在液体上方变为红棕色,则含有NaNO2。
(4)经检验C产物中亚硝酸钠含量较少。
①.甲同学认为C中产物不仅有亚硝酸钠,还可能有其它固体物质。为排除干扰,甲在B、C装置间增加装置E,E中盛放的试剂应是__________(写名称)。
②.乙同学认为除上述干扰因素外,还会有空气参与反应导致产品不纯,所以在实验操作①前应增加一步操作,该操作是 。
(5)NaNO2有毒,国家规定肉制品中NaNO2含量不能超过30mg/kg。从1000g隔夜熟肉中提取NaNO3与NaNO2后,配成溶液,再用0.00500mol/L的高锰酸钾(酸性)溶液滴定,消耗高锰酸钾溶液16.00mL,由此计算隔夜熟肉中NaNO2的含量是____________mg/kg。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质分类的叙述正确的是( )
A.NaCl晶体不导电,所以NaCl是非电解质
B.Na2O2能与酸反应,所以Na2O2是碱性氧化物
C.BaSO4难溶于水,但BaSO4是强电解质
D.NH4Cl不含有金属离子,所以NH4Cl不是盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验的反应原理用方程式或电极反应式表示正确的是
A.室温下,测得氯化铵溶液pH<7,证明一水合氨是弱碱:NH4++2H2O=NH3·H2O+H3O+
B.钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-=Fe3+
C.用铂做电极,KOH溶液作电解质溶液,甲烷燃料电池的总反应:CH4+2O2=CO2+2H2O
D.铅酸蓄电池充电时接直流电源的正极反应:PbSO4+2H2O-2e-= PbO2+4H++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.乙烯的结构简式可以表示为CH2CH2
B.苯、乙醇和乙酸都能发生取代反应
C.丙烯所有原子可能在一个平面上
D.水煤气和天然气的主要成分都是甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。
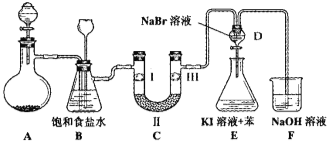
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:__ __。
(2)装置B中饱和食盐水的作用是_________________________________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象__________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入__ _。
A | B | C | D | |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)设计装置D、E的目的是 。打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是_______________________________。
(5)某同学建议将装置F中的药品改用足量的NaHSO3溶液吸收余氯,老师认为不妥,用总反应的离子方程式解释原因_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为提高资源的利用率,可以将富锰渣(主要成分为Mn、SiO2、Al2O3、Fe)里面的锰再提炼以利用。下图为由富锰渣制备无水氯化锰的工艺流程,回答下列问题:
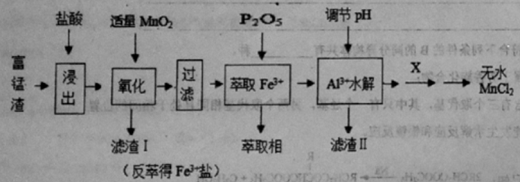
(1)“浸出”前将富锰渣粉碎成细颗粒,其目的是 。
(2)滤渣I的主要成分是 (填化学式)。
(3)加入MnO2氧化时,发生反应的离子方程式为 。
(4)结合下表数据(25℃),应调节pH的范围为 ,从下表中数据计算可得Al(OH)3的溶度积,该温度下Ksp[Al(OH)3]约为 。
离子 | 开始沉淀时的pH | 完全沉淀时的pH | 沉淀开始溶解时的pH |
Al3+ | 4.0 | 5.2 | 7.8 |
Mn2+ | 8.8 | 10.4 | 14 |
(5)已知MnCl2溶液呈弱酸性,操作X为 (填字母序号)。
A.蒸发结晶 B.降温结晶 C.渗析 D.盐析
(6)MnO2的生产方法之一是以惰性电极电解MnCl2和HCl混合溶液,阳极的电极反应是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】绿色化学对化学反应提出了“原子经济性”(原子节约)的新概念及要求。理想的“原子经济性”反应是原料分子中的原子全部转变成所需产物,不产生副产物,实现零排放。以下反应中符合绿色化学原理的是
A.乙烯与氧气在银催化作用下生成环氧乙烷(![]() )
)
B.乙烷与氯气制备氯乙烷
C.苯和乙醇为原料,在一定条件下生产乙苯
D.乙醇与浓硫酸共热制备乙烯
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com