
下列反应属于氧化还原反应的是 ( )
| A.CaCO3+2HCl===CaCl2+CO2↑+H2O | B.CO2+H2O===H2CO3 |
| C.2H2O2催化剂 2H2O+O2↑ | D.CaCO3 CaO+CO2↑ CaO+CO2↑ |
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源:2013-2014广西桂林市下学期高二年级期末考试化学试卷(解析版) 题型:填空题
(5分)元素Cu的一种氯化物晶体的晶胞结构如图所示,计算推出该氯化物的化学式是______,它可与浓盐酸发生非氧化还原反应,生成配合物H2CuCl3,反应的化学方程式为____________________。

查看答案和解析>>
科目:高中化学 来源:2013-2014广东肇庆市毕业班第二次模拟考试理综化学试卷(解析版) 题型:填空题
.(15分)药物Z可用于治疗哮喘、系统性红斑狼疮等,可由X(1,4-环己二酮单乙二醇缩酮)和Y(咖啡酸)为原料合成,如下图:

(1)化合物X的有 种化学环境不同的氢原子。
(2)下列说法正确的是 。
A.X是芳香化合物 B.Ni催化下Y能与5molH2加成
C.Z能发生加成、取代及消去反应 D.1mol Z最多可与5mol NaOH反应
(3)Y与过量的溴水反应的化学方程式为 。
(4)X可以由 (写名称)和M( )分子间脱水而得;一定条件下,M发生1个—OH的消去反应得到稳定化合物N(分子式为C6H8O2),则N的结构简式为 (已知烯醇式不稳定,会发生分子重排,例如:
)分子间脱水而得;一定条件下,M发生1个—OH的消去反应得到稳定化合物N(分子式为C6H8O2),则N的结构简式为 (已知烯醇式不稳定,会发生分子重排,例如:
 )。
)。
(5)Y也可以与环氧丙烷( )发生类似反应①的反应,其生成物的结构简式为 (写一种);Y的同分异构体很多种,其中有苯环、苯环上有三个取代基(且酚羟基的位置和数目都不变)、属于酯的同分异构体有 种。
)发生类似反应①的反应,其生成物的结构简式为 (写一种);Y的同分异构体很多种,其中有苯环、苯环上有三个取代基(且酚羟基的位置和数目都不变)、属于酯的同分异构体有 种。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一种离子与多种酸根离子构成的盐称为“混盐”,如氯化硝酸钙[Ca(NO3)Cl];而“复盐”则是指含有多种简单阳离子和一种酸根阴离子的盐,如KAl(SO4)2。据此,下列各化合物中属于混盐的是
| A.(NH4)2Fe(SO4) | B.BiONO3 | C.CaOCl2 | D.K3[Fe(CN)6] |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
“化学是一门中心学科,与社会、生活、科研密切的关系”。下列叙述中,不正确的是
| A.大量使用燃煤发电是形成雾霾的主要原因 |
| B.天然气、煤气大量泄漏遇到明火会爆炸 |
| C.利用化学反应可实现12C到14C的转化 |
| D.晶体硅可用于光伏发电、制造芯片 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列反应中,在高温下不能自发进行的是( )
A.CO(g) C(s)+O2(g) C(s)+O2(g) |
B.NH4Cl(s) NH3(g)↑+HCl(g)↑ NH3(g)↑+HCl(g)↑ |
C.(NH4)2CO3(s) NH4HCO3(s)+NH3(g) NH4HCO3(s)+NH3(g) |
D.MgCO3(s) MgO(s)+CO2(g) MgO(s)+CO2(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
(本题16分)工业上用白云石制备高纯氧化镁的工艺流程如下: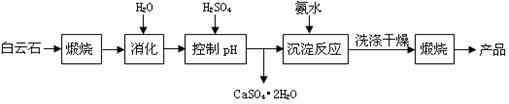
已知Ⅰ.白云石主要成分可表示为:CaO 32.50%;MgO 20.58%;Fe2O3 2.18%;SiO2 0.96%;其他 43.78%。
(1)为了提高白云石的煅烧效果,可以采取的措施是将矿石 。若在实验室中煅烧白云石,需要的仪器除酒精灯、三脚架以外,还需要 (填序号)。
A.蒸发皿 B.坩埚 C.泥三角 D.石棉网
(2)加入H2SO4控制pH时,终点pH对产品的影响如图8所示。则由图示可得到的结论及原因是:
①pH过高会导致___________________________下降,其原因是_______________________
②pH过低会引起____________________________ ,其原因可能是__________(填序号)
A.Fe2O3溶于H2SO4最终使产品混有杂质 B.SiO2溶于H2SO4最终使产品混有杂质
C.酸性过强,形成可溶的Ca(HSO4)2,最终使产品混有含钙的杂质
(3)已知MgSO4、CaSO4的溶解度如下表:
| 温度(℃) | 40 | 50 | 60 | 70 |
| MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
| CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
| pH | < 8.0 | 8.0 ~ 9.6 | > 9.6 |
| 颜色 | 黄色 | 绿色 | 蓝色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com