
下列现象或事实不能用同一原理解释的是( )
A.浓硝酸和氯水用棕色试剂瓶保存
B.硫化钠和亚硫酸钠固体长期暴露在空气中变质
C.常温下铁和铂都不溶于浓硝酸
D.SO2和Na2SO3溶液都能使氯水褪色
科目:高中化学 来源:2017届天津市五区县高三上学期期末考试化学试卷(解析版) 题型:选择题
常温下,现向50 mL 0.1 mol·L-1 NH4HSO4溶液中滴加0.05 mol·L-1 NaOH溶液,得到溶液的pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生)。下列说法正确的是

A.b点溶液中离子浓度由大到小的顺序为:c(Na+)>c(SO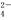 )>c(NH
)>c(NH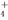 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
B.图中b、c、d三点溶液中水的电离程度最大的是c点
C.b点后滴加NaOH溶液过程中,NH3·H2O的电离程度逐渐减小
D.pH=7时,溶液中c(H+)+c(Na+)+c(NH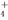 )=c(SO
)=c(SO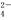 )+c(OH-)
)+c(OH-)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省惠州市高二上学期高二质量检测化学试卷(解析版) 题型:选择题
在容积不变的密闭容器中进行如下反应:N2+3H2 2NH3,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是
2NH3,若将平衡体系中各物质的浓度都增加到原来的2倍,则产生的结果是
A.平衡不发生移动 B.平衡沿着逆反应方向移动
C.正逆反应速率都增大 D.NH3的质量分数减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省定西市通渭县高二上学期期末化学试卷(解析版) 题型:选择题
已知25℃时,Mg(OH)2的Ksp = 5.6×10-12,MgF2的Ksp=7.4×10-11。下列说法正确的是( )
A.25℃时,在Mg(OH)2的悬浊液中加入少量的NH4Cl固体,c(Mg2+)增大
B.25℃时,饱和Mg(OH)2溶液与饱和MgF2溶液相比,前者c(Mg2+)大
C.25℃时,Mg(OH)2固体在同体积同浓度的氨水和NH4Cl溶液中的Ksp 比较,前者小
D.25℃时,在Mg(OH)2的悬浊液中加入饱和NaF溶液后,Mg(OH)2不可能转化成MgF2
查看答案和解析>>
科目:高中化学 来源:2016-2017黑龙江牡丹江第一高级中学高一上期末化学卷(解析版) 题型:推断题
下列框图所示的转化关系中,A、C均为常见的金属单质, E为固体非金属单质。B为棕红色固体氧化物,X为常见的无色液体。L焰色为黄色,且能使酚酞变红(反应过程中生成的水及其他产物已略去)

请回答以下问题:
(1)F的化学式为 ;
(2)I与氯水反应的离子方程式为 ;
(3)A与B生成C和D的反应是 (填“放出”或“吸收”)大量热量的反应;
(4)D与L反应的离子方程式为 。
(5)检验“黄色溶液”中金属阳离子的试剂是 (写化学式)
查看答案和解析>>
科目:高中化学 来源:2016-2017黑龙江牡丹江第一高级中学高一上期末化学卷(解析版) 题型:选择题
下列各组中的两种物质作用,反应条件(温度或者反应物用量)改变,不会引起产物种类改变的是
A.N a和O2 B.Cu和HNO3 C.N2和O2 D.Na2CO3和HCl
a和O2 B.Cu和HNO3 C.N2和O2 D.Na2CO3和HCl
查看答案和解析>>
科目:高中化学 来源:2016-2017黑龙江牡丹江第一高级中学高一上期末化学卷(解析版) 题型:选择题
下列离子方程式错误的是( )
A.小苏打溶液中加入过量的烧碱溶液:HCO3-+OH-=CO32-+H2O
B.澄清石灰水中通入过量的CO2:CO2+OH―=HCO3―
C.向氯化铝溶液中加入足量氨水:Al3++4NH3·H2O=AlO2―+2H2O +4NH4+
D.Cl2与水反应生成盐酸和次氯酸Cl2+H2O=H++Cl―+HClO
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高一12月月考化学卷(解析版) 题型:选择题
如图表示金属X、Y及它们的合金Z分别与足量盐酸反应放出H2量的情况,横坐标表示消耗金属的物质的量,纵坐标表示在标准状况下产生H2的体积.下列有关合金组成的判断正确的是
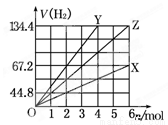
A.n(Na)∶n(Fe)=2∶1 B.n(Mg)∶n(K)=1∶2
C.n(Na)∶n(Al)=1∶3 D.n(K)∶n(Al)=1∶1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市部分区高一上学期期末化学试卷(解析版) 题型:填空题
饮用水质量是关系人类健康的重要问题。
(1)在我国,一些贫困山区的农民至今还饮用井水,但暴雨过后井水混浊,无法饮用。为了能让暴雨过后井水尽快变的澄清,你会建议他们最好向井水中投入下列中的 ________(填序号)。
A.NaCl B.Na2CO3 C.KAl(S O4)2·12H2O D.CuSO4
O4)2·12H2O D.CuSO4
(2)氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为:__________________________。
(3)写出工业上制取漂白粉的化学反应方程式:________________________。
(4)臭氧,也称作超氧,可以替代氯气给自来水消毒,既提高了消毒效率且安全无副作用,臭氧的分子式为_____________;该物质、氯水以及SO2均可以作漂白剂,三者的漂白原理分别是:_________________;___________________;____________________。
(5)ClO2 是一种广谱型的消毒剂,将逐渐取代Cl2成为生产自来水的消毒剂。工业上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反应制得,反应中NaClO3和Na2SO3的物质的量之比为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com