
����Ŀ��ijǿ������ɫ��Һ�п��ܺ��±������е����������ӡ�
������ | Mg2+��NH4+��Ba2+��Al3+��Fe2+ |
������ | SiO32-��MnO4-��Cl-��NO3-��SO42- |
ʵ���:ȡ������ǿ������ҺA��������ʵ�顣
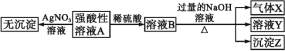
ʵ���:Ϊ�˽�һ��ȷ������Һ�����,ȡ100 mLԭ��ҺA,�����Һ�еμ�1 mol��L-1��NaOH��Һ,��������������������������Һ����Ĺ�ϵ��ͼ��ʾ��
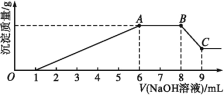
�ش���������:
(1)������ʵ��Ϳ����ƶϳ�,�ϱ��е�����һ�������ڵ���________�֡�
(2)ͨ��ʵ������ȷ������Һ��һ�����ڵ���������_________����������X�ķ�����_______________;����Z�Ļ�ѧʽΪ_____________��
(3)д��ʵ����ͼʾ��BC�ζ�Ӧ��Ӧ�����ӷ���ʽ:________________��
(4)A���Ӧ�Ĺ�������Ϊ____ g��
(5)ͨ��������Ϣ,�������Һ�������ӵ�Ũ��Ϊ________ mol��L-1��
���𰸡�4 NO3- �����Ӽ�һ��ʪ��ĺ�ɫʯ����ֽ��������X,��ֽ���� Mg(OH)2 Al(OH)3+OH-=AlO2-+2H2O 0.136 0.08
��������
ijǿ������ɫ��Һ��Fe2+��SiO32-��MnO4-��SO32-һ�������ڣ���Һ����������������ְ�ɫ����������һ������Cl-������ҺΪ�����Կ�֪һ����������ΪNO3-����Һ������������������һ������Ba2+������������������ƣ����ȣ��������������壬��һ������Mg2+��NH4+��Ϊ�˽�һ��ȷ������Һ����ɣ�ȡ100mLԭ��Һ�������Һ�еμ�1mol/L��NaOH��Һ����ͼ�в�������������������������Һ����Ĺ�ϵ��֪һ������Al3+���Դ������
(1)��ijǿ������ɫ��Һ��Fe2+��SiO32-��MnO4-��SO32-һ�������ڣ�
�ʴ�Ϊ��4��
(2)��ǿ������ɫ��Һ��Fe2+��SiO32-��MnO4-��SO32-һ�������ڣ���Һ����������������ְ�ɫ����,����һ������Cl-������������������,һ������Ba2+������������������ƣ����ȣ��������������壬��һ������Mg2+��NH4+��ͨ��ʵ��I����ȷ������Һ��һ�����ڵ���������NO3-������X�ǰ��������鷽���������Ӽ�һ��ʪ��ĺ�ɫʯ����ֽ��������x����ֽ����������Z�Ļ�ѧʽΪMg(OH)2��
�ʴ�Ϊ��NO���� �Ӽ�һ��ʪ��ĺ�ɫʯ����ֽ��������x����ֽ������Mg(OH)2��
(3)��ʵ��II��ͼ����BC�����������������������ƵĹ���, ��Ӧ�����ӷ���ʽΪ��Al(OH)3+OH-=AlO2-+2H2O��
�ʴ�Ϊ��Al(OH)3+OH-=AlO2-+2H2O ��
(4)��BC�ζ�Ӧ�����ӷ���ʽ��Al(OH)3+OH-=AlO2-+2H2O�����ĵ�����������0.001mol�����Ժ�����������0.001mol������þ���Ӻ�������һ��������������0.005mol������þ�������ʵ���Ҳ��0.001mol��A����õ��Ĺ�����������þ0.001mol����������0.001mol��������0.001mol��58g/ mol + 0.001mol��78g/mol= 0.136g��
�ʴ�Ϊ��0.136��
(5)������Һ�д��ڵ���������NO3-������ͼ����Һ������������0.001mol������笠�������0.002mol�������ӡ�þ���Ӹ���0.001 mol�����ݵ���غ㣬������������ʵ���n= 0.001mol+0.002mol+0.002mol+0.003mol = 0.008mol��![]() ��
��
�ʴ�Ϊ��0.08��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������л���������ص�˵����ȷ����![]() ����
����![]()
A.���ࡢ��֬�������ʶ���ˮ��,��ˮ����ﲻͬ
B.�ı�����ϩ![]()
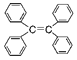
![]() ������̼ԭ��һ������ͬһƽ��
������̼ԭ��һ������ͬһƽ��
C.![]() ��һ��������������H2��Ӧ����4mol H2
��һ��������������H2��Ӧ����4mol H2
D.����ʽΪC7H8�ķ�������H2��ȫ�ӳ����ò����һ�ȴ�����5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��A��B��C��D��E��F����Ԫ�أ����ǵ�ԭ��������A��F�������������ڱ��У�A��ԭ�Ӱ뾶��С��BԪ�ص�ԭ���������������ڲ��������������CΪ�ؿ��к�������Ԫ�أ�D��ԭ�Ӱ뾶���Ķ���������Ԫ�أ�D����ȼ��ʱ���ֻ�ɫ���棬D�ĵ����ڸ�������C�ĵ��ʳ�ַ�Ӧ�����Եõ���E������ɫ��ͬ�ĵ���ɫ��̬�����D��F�γɵ����ӻ�����DF�dz��õĵ�ζƷ���Ը������������ش�
��1��Ԫ�����ƣ�
A________��B________��C________��D________��
��2��E��Ԫ�����ڱ��е�λ�ã�_________________________________________________��
��3��F���ӽṹʾ��ͼ��_____________________________________________________��
��4��A��B��ɵ���������������____________________________________________��
��5��C��D��ԭ�Ӹ�����1��1��ɵ�һ�ֻ�������ˮ������Ӧ�Ļ�ѧ����ʽΪ___________________________________________________________��
��6����˵��E�ķǽ����Ա�F�ķǽ�����____������ǿ����������������ʵ��________����һ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1���ڴ���CuSO4��5H2O�����г���������Fe2+��
�����ᴿʱΪ�˳�ȥFe2+����������ʵ���������ʹFe2+ת��ΪFe3+���������ʿ�������������__(����ĸ)��
A.KMnO4 B.H2O2 C.��ˮ D.HNO3
��Ȼ���ټ����ʵ����ʵ�����ҺpH��4��ʹFe3+ת��ΪFe(OH)3��������ҺpH��ѡ��___(����ĸ)��
A.NaOH B.NH3��H2O C.CuO D.Cu(OH)2
��2����ͬѧ���ɵ�����ҺpH��4�Ƿ��ܴﵽ��ȥFe3+������ʧCu2+��Ŀ�ģ���ͬѧ��Ϊ����ͨ������ȷ�����������й����ϵõ��������ݣ�������Fe(OH)3���ܶȻ�Ksp=1.0��10-38��Cu(OH)2���ܶȻ�Ksp=3.0��10-20��ͨ����������Һ�е�����Ũ��С��1.0��10-5mol��L-1ʱ�ͱ��϶�Ϊ������ȫ������Һ��CuSO4��Ũ��Ϊ3.0mol��L-1����Cu(OH)2��ʼ����ʱ��Һ��pHΪ__��Fe3+��ȫ����[��c(Fe3+)��1.0��10-5mol��L-1]ʱ��Һ��pHΪ__��ͨ������ȷ����������__(����������������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A.��״���£�22.4 Lˮ�������ķ�����ԼΪ6.02��1023��
B.1 mol Cl2�к��е�ԭ����ΪNA
C.��״���£�aL�����͵����Ļ���ﺬ�еķ�����ԼΪ![]() ��6.02��1023��
��6.02��1023��
D.���³�ѹ�£�11.2 L CO��������0.5NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ֽ���������ĩ15g�������������ᷴӦ���ɱ�״����11.2L������������������Ľ����������(����)
A.Mg��FeB.Zn��AgC. Fe��ZnD.Mg��Al
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����κ����ʳƷ��ҽҩ�ȷ������Ź㷺��;��һ�ֺϳɰ�κ��ķ�Ӧ�ɱ�ʾΪ
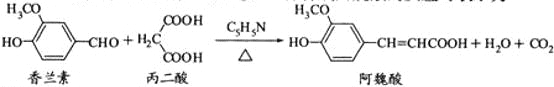
����˵����ȷ����
A. ��������![]() ��Һ���������Ӧ�Ƿ��а�κ������
��Һ���������Ӧ�Ƿ��а�κ������
B. �����ء���κ�������![]() ��
��![]() ��Һ��Ӧ
��Һ��Ӧ
C. ͨ�������£������ء���κ�ᶼ�ܷ���ȡ�����ӳɡ���ȥ��Ӧ
D. �������ػ�Ϊͬ���칹�壬��������4�ֲ�ͬ��ѧ�������⣬���ܷ���������Ӧ�ķ�����ﹲ��2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H �Ǻϳɿ���ҩ��������ƵĹؼ��м��壬����һ�ֺϳ�·�����£�

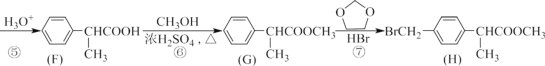
(1)A ����������Ϊ_________��H �зǺ���������������_________��
(2)E �Ľṹ��ʽΪ_________����Ӧ���ķ�Ӧ����Ϊ_________��
(3)Ӧ���Ļ�ѧ����ʽΪ_________����Ӧ���Ļ�ѧ����ʽΪ_________��
(4)д���������������� F ��ͬ���칹��Ľṹ��ʽ_________��
I.�ܷ���ˮ�ⷴӦ������ʹ�
��.�ܷ���������Ӧ
��.�˴Ź��������� 5 ����ҷ����֮��Ϊ 3:2:2:2:1
(5)����H �ĺϳ��ߣ����һ����![]() �ϳ�
�ϳ�![]() �ĺϳ�·��________��
�ĺϳ�·��________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ������˵������ȷ���ǣ� ��
A.0.1 L 0.5 mol��L��1 CH3COOH��Һ�к��е�H����Ϊ0.05NA
B.1 mol Na2O2������CO2��H2O��ַ�Ӧ��ת�Ƶĵ�����������
C.m g CO��N2�Ļ������������������ĿΪ![]() NA
NA
D.18 g 2H216O�к��е�����������������Ϊ10NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com