
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2015-2016学年福建晨曦、冷曦、正曦、岐滨四校高二上联考化学卷(解析版) 题型:选择题
在甲酸的下列性质中,可以证明它是弱电解质的是
A.在相同条件下,甲酸的导电性比强酸溶液的导电性弱
B.甲酸能与水以任意比互溶
C.10mL 1mol/L甲酸恰好跟10 mL 1mol/L NaOH溶液完全反应
D.1mol/L甲酸溶液中c(H+)约为1×10-2mol/L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省五校高一上第一次月考化学试卷(解析版) 题型:填空题
2010年10月1日,我国西昌卫星发射中心用“长征三号丙”运载火箭成功发射嫦娥二号探月卫星,火箭的燃料之一是铝粉与高氯酸铵(NH4ClO4)的固体混合物,点燃时,铝粉被氧化放热引发高氯酸铵反应:2NH4ClO4===N2↑+4H2O+Cl2↑+2O2↑,反应放出大量热。
(1)该反应中被氧化的元素是___________。
(2)对该反应的反应类型判断正确的是____________。
A.氧化还原反应 B.复分解反应 C.置换反应 D.分解反应
(3)氧化产物与还原产物的质量之比为_________。
(4)该反应中若生成1 mol Cl2,则电子转移数为______________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期期中(理)化学试卷(解析版) 题型:选择题
根据电子排布的特点,Br在周期表属于
A.s区 B.p区 C.d 区 D.ds区
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省高二上学期期中(文)化学试卷(解析版) 题型:选择题
下列各组成金属和溶液,能组成原电池的是
A.Cu、Cu、稀硫酸 B. Ag、Cu、稀硫酸
C.Cu、Zn、酒精 D. Zn、Cu、CuSO4溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上学期第三次段考化学试卷(解析版) 题型:实验题
某学生用0.1 mol·L-1的KOH标准溶液滴定未知浓度的盐酸,其操作分解为如下几步:
A.移取20 mL待测盐酸注入洁净的锥形瓶,并加入2~3滴酚酞
B.用标准溶液润洗滴定管2~3次
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液
D.取标准KOH溶液注入碱式滴定管至“0”刻度以上1~2 cm
E.调节液面至“0”或“0”以下某一刻度,记下读数
F.把锥形瓶放在滴定管的下面,用标准KOH溶液滴定至终点并记下滴定管液面的刻度
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)__________________;
(2)上述B步骤操作的目的是_______________________;
(3)上述A步骤操作之前,先用待测液润洗锥形瓶,则对滴定结果的影响是______________;
(4)判断到达滴定终点的实验现象是______________________;
(5)若滴定时在晃动锥形瓶的过程中不小心将液体洒出,对实验结果的影响是_______;
(6)若称取一定量的KOH固体(含少量NaOH)配制标准溶液并用来滴定上述盐酸,则对滴定结果产生的影响是__________________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高一上学期第三次段考化学试卷(解析版) 题型:选择题
下列关于金属钠的叙述中,说法正确的是( )
A.Na在空气中燃烧,发出黄色火焰 B.Na在空气中燃烧,产物是Na2O
C.Na是银白色金属,硬度大,熔点高 D.Na可以在空气中稳定存在
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期第二次月考化学试卷(解析版) 题型:选择题
下列仪器中没有零刻度的是( )
A.温度计 B.量筒 C.滴定管 D.托盘天平游码标尺
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期12月月考化学试卷(解析版) 题型:简答题
(2011·浙江,27)某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 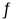 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓 度/mol·L-1 | 2.4×10-3 | 3.4×10-3 | 4.8×10-3 | 6.8×10-3 | 9.4×10-3 |
①可以判断该分解反应已经达到平衡的是_______________ 。
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
②根据表中数据,列式计算25.0 ℃时的分解平衡常数:________。
③取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0 ℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量_________________ (填“增加”,“减少”或“不变”)。
④氨基甲酸铵分解反应的焓变ΔH_______________0(填“>”、“=”或“<”),熵变ΔS________________0(填“>”、“=”或“<”)。
(2)已知:NH2COONH4+2H2O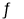 NH4HCO3+NH3·H2O
NH4HCO3+NH3·H2O
该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO-)随时间的变化趋势如下图所示。

⑤计算25.0 ℃时,0~6 min氨基甲酸铵水解反应的平均速率:________。
⑥根据图中信息,如何说明该水解反应速率随温度升高而增大:______________ _______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com