
【题目】A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,能进行如图所示的多种反应。

(1)A的官能团名称是_______________________,B的结构简式是________。
(2)反应②的反应类型为______________。
(3)写出反应③的化学方程式:_____________________。
(4)写出反应④的化学方程式:_____________________。
【答案】羟基 CH2CH2 加成反应 C2H5OH+CH3COOH![]() CH3COOC2H5+H2O 2CH3CH2OH+O2
CH3COOC2H5+H2O 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
【解析】
A是化学实验室中最常见的有机物,它易溶于水并有特殊香味,A为乙醇,乙烯和水加成反应生成乙醇,因此B为乙烯,乙醇和乙酸发生酯化反应生成乙酸乙酯,因此C为乙酸乙酯,乙醇催化氧化生成乙醛,因此D为乙醛,乙醇和钠反应生成乙醇钠,因此E为乙醇钠。
(1)乙醇中含有的官能团为羟基;乙烯的结构简式为CH2CH2;故答案为:羟基;CH2CH2。
(2)乙烯与水发生加成反应生成乙醇;故答案为:加成反应。
(3)乙醇和乙酸反应生成乙酸乙酯,化学方程式为CH3CH2OH+ CH3COOH ![]() CH3COOC2H5+H2O;故答案为:CH3CH2OH+CH3COOH
CH3COOC2H5+H2O;故答案为:CH3CH2OH+CH3COOH![]() CH3COOC2H5+H2O。
CH3COOC2H5+H2O。
(4)乙醇在铜的催化作用下与氧气发生氧化反应生成乙醛,化学方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O;故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O;故答案为:2CH3CH2OH+O2![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】某密闭容器中发生反应:N2(g)+3H2(g)![]() 2NH3(g)ΔH<0,达到化学平衡状态,下列说法正确的是( )
2NH3(g)ΔH<0,达到化学平衡状态,下列说法正确的是( )
A.其他条件不变时,增大c(N2),H2的平衡转化率增大
B.其他条件不变时,降低温度,n(NH3)减小
C.其他条件不变时,增大压强,该反应的平衡常数增大
D.其他条件不变时,升高温度,该反应的化学反应速率加快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要用480mL0.1molL-1的硫酸铜溶液,以下配制方法正确的是( )
A. 称取![]() 胆矾(CuSO4·5H2O),配成500mL溶液
胆矾(CuSO4·5H2O),配成500mL溶液
B. 称取![]() 胆矾(CuSO4·5H2O),加入500mL水配成溶液
胆矾(CuSO4·5H2O),加入500mL水配成溶液
C. 称取![]() 无水硫酸铜粉末,加入480mL水配成溶液
无水硫酸铜粉末,加入480mL水配成溶液
D. 称取![]() 无水硫酸铜粉末,加入500mL水配成溶液
无水硫酸铜粉末,加入500mL水配成溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水硫酸铜在加热条件下能发生分解反应,生成氧化铜、二氧化硫、三氧化硫和氧气。某学生试图用如图所示装置来确定该化学反应中各物质的计量关系。
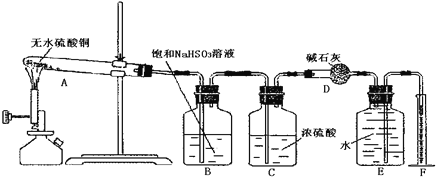
试回答:
(1)加热过程中,试管A中发生的实验现象可能有___。
(2)装置E和F的作用是___;
(3)该学生使用装置B的本意是除去混合气体中的三氧化硫以提纯氧气,他的做法正确吗?为什么?___。
(4)另一学生将9.6g无水硫酸铜充分加热使其完全分解后,用正确的实验方法除去了生成物中的二氧化硫和三氧化硫,最后测出氧气的体积为448mL(标准状况)。据此可计算出二氧化硫为___mol,三氧化硫为___mol。
(5)由上述实验数据可知无水硫酸铜受热分解的化学方程式:___。
(6)上述装置可以简化而不影响实验效果。请你提出一个简化方案,达到使装置最简单而不影响实验效果的目的:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1乙氧基萘常用作香料,也可合成其他香料。实验室制备1乙氧基萘的过程如下:
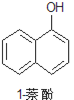 +CH3CH2OH
+CH3CH2OH![]()
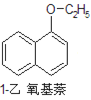 +H2O
+H2O
已知:1萘酚的性质与苯酚相似,有难闻的苯酚气味。相关物质的物理常数:
物质 | 相对分子质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度 | |
水 | 乙醇 | |||||
1萘酚 | 144 | 无色或黄色菱形结晶或粉末 | 96℃ | 278℃ | 微溶于水 | 易溶于乙醇 |
1乙氧基萘 | 172 | 无色液体 | 5.5℃ | 267℃ | 不溶于水 | 易溶于乙醇 |
乙醇 | 46 | 无色液体 | 114.1℃ | 78.5℃ | 任意比混溶 | |
(1)将一定量1萘酚溶于无水乙醇中,并加入少量浓硫酸混合。将混合液置于如图所示的容器中加热充分反应。实验中使用过量乙醇的原因是__________。
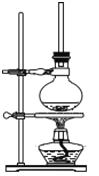
(2)装置中长玻璃管的作用是:______。
(3)该反应不能用实验室制备乙酸乙酯的装置,简述理由____________;
(4)反应结束,需要提纯产物,在下面的横线上填上相应操作的名称:倒入冷水,碱洗并_______ → 水洗并_______ →加入CaCl2干燥并______→___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬是一种氧气吸收剂, 通常以二水盐[Cr(CH3COO)2]2 ·2H2O(式量:376)的形式存在,难溶于冷水,易溶于盐酸。其制备原理和实验装置:
制备原理:![]()
实验装置:(如图所示)

(1)仪器 A 的名称是__________。
(2)装好试剂后按上述装置进行实验,完成下表内容。
操作步骤 | 实验现象 | 发生反应的离子方程式 |
关闭①___________________,打开②_______________,(用K1、K2、K3填写,下同)使盐酸缓慢加入至抽滤瓶中 | 抽滤瓶中锌粒溶解,溶液由橙色逐渐变成蓝色,有少量气泡 | ③________,Zn+2H+=Zn2++H2↑ |
抽滤瓶中产生大量气体时快速加入适量盐酸,关闭K2和④__________________,打开⑤_________ | 抽滤瓶中⑥____________ | Zn+2H+=Zn2++H2↑ |
当溶液完全转移后,迅速塞紧锥形瓶,用冷水冷却 | 锥形瓶中有深红色晶体析出 | ⑦_____________ |
(3)洗涤产品后干燥、称量,得到 1.0g 固体。列式表示产率:____(不必计算出结果,K2Cr2O7 式量:294)。在实验中如果盐酸过量,会导致产率偏________。(填“高”或“低”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前,从海水提取的溴占世界溴年产量的三分之一左右,空气吹出法是工业规模海水提溴的常用方法。其中一种工艺流程为:①海水浓缩,酸化;②通入Cl2,使Br— 转化为Br2;③通入空气、水蒸气,将Br2吹入吸收塔,与吸收剂SO2反应转化为HBr;④通入Cl2,再经过一系列处理得到产品Br2。请回答下列问题:
(1)步骤②、③操作的目的是_____(填“富集溴”或“萃取溴”);
(2)在步骤③中,生成HBr的化学方程式是___________;
(3)在步骤②中,若通入22.4LCl2(标准状况),理论上可得Br2__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型漂白剂结构如图所示,其中W.Y.Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列说法正确的是
![]()
A.非金属性:X>W>Y
B.Y的最高价氧化为对应的水化物为三元酸
C.可利用W与X、Y形成的化合物热还原制备单质Y
D.该漂白剂中仅有X均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维生素C的结构简式是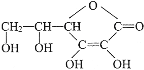 ,它的分子式是______________。由于它能防治坏血病,又称为_______。在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有__________性;在维生素C溶液中滴入少量蓝色的含有淀粉的碘水,可观察到的现象是___________,说明维生素C具有____________性。
,它的分子式是______________。由于它能防治坏血病,又称为_______。在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有__________性;在维生素C溶液中滴入少量蓝色的含有淀粉的碘水,可观察到的现象是___________,说明维生素C具有____________性。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com