
某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理正确的是
50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
m(混合物) | 9.2g | 15.7g | 27.6g |
| 2.24L | 3.36L | 3.36L |
A.盐酸的物质的量浓度为5.0mol·L-1
B.根据表中数据计算出混合物中NaHCO3的物质的量分数为50%
C.9.2g混合物中NaHCO3和KHCO3分别为5.0g和4.2g
D.15.7g混合物恰好与盐酸完全反应
科目:高中化学 来源:2017届江苏省徐州、宿迁、连云港、淮安四市高三11月模拟化学卷(解析版) 题型:实验题
[实验化学]对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺磺化得到。

已知:100 mL水在20℃时可溶解对氨基苯磺酸1.08 g,在100℃时可溶解6.67 g。
实验室可用苯胺、浓硫酸为原料,利用右图所示实验装置合成对氨基苯磺酸。实验步骤如下:步骤1:在一个250 mL三颈烧瓶中加入10 mL苯胺及几粒沸石,将三颈烧瓶放在冰水中冷却,小心地加入18 mL浓硫酸。在三颈烧瓶的两个瓶口上分别装冷凝管、温度计,另一个没有使用的瓶口用塞子塞紧。将三颈烧瓶置于油浴中缓慢加热至170~180℃,维持此温度2~2.5小时。
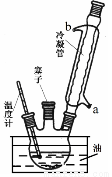
步骤2:将反应产物冷却至约50℃后,倒入盛有100 mL冷水的烧杯中,用玻璃棒不断搅拌,促使对氨基苯磺酸晶体析出。用该烧杯中的少量冷水将烧瓶内残留的产物冲洗到烧杯中,抽滤,用少量冷水洗涤,得到对氨基苯磺酸粗产品。
步骤3:将粗产品用沸水溶解,冷却结晶,抽滤,收集产品,晾干可得纯净的对氨基苯磺酸。
(1)实验装置中冷凝管由 处(填“a”或“b”)通入冷凝水。
(2)步骤1油浴加热的优点有 。
(3)步骤2中用玻璃棒不断搅拌可促使对氨基苯磺酸晶体析出的理由是 ,用少量冷水洗涤的目的是 。
(4)步骤2和3均进行抽滤操作,在抽滤完毕停止抽滤时,应注意先拆下连接泵和吸滤瓶的橡皮管,然后关闭水龙头,其目的是 。
(5)步骤3中若溶液颜色过深,可用 进行脱色处理。
查看答案和解析>>
科目:高中化学 来源:2017届云南曲靖市高三上学期第三次月考化学试卷(解析版) 题型:推断题
有机物A-G之间的转化关系下图所示,按要求回答下列问题:

(1)A的名称为______;C分子在核磁共振氢谱中有______个吸收峰.D的结构简式为______;F含有的官能团名称是______.
(2)指出下列反应④类型_____________________。
(3)反应⑤的化学方程式为____________________________。
(4)反应⑥的化学方程式为____________________________。
(5)F有多种同分异构体,其中满足以下条件的同分异构体有___________种。
①与FeC13溶液发生显色反应
②苯环上最多有三个取代基。且苯环上的一卤代物只有两种
③能发生银镜反应
④1mol该有机物与足量的钠反应,生成标准状况下22.4L的气体
查看答案和解析>>
科目:高中化学 来源:2017届云南曲靖市高三上学期第三次月考化学试卷(解析版) 题型:选择题
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A是组成有机物的必要元素,元素B的原子最外层电子数是其电子层数的3倍,元素D与A为同族元素,元素C与E形成的化合物CE是氯碱工业的主要原料。下列说法正确的是
A. 原子半径:C>D>B>A
B. C和E的单质常温下不能相互反应
C. C与B形成的两种化合物均属于离子化合物,且化学键类型完全相同
D. A、D、E的最高价氧化物对应水化物均为弱酸
查看答案和解析>>
科目:高中化学 来源:2017届陕西西安市高三上第二次质量检测化学试卷(解析版) 题型:实验题
某化工厂冶炼金属、回收硫的工艺流程如下:
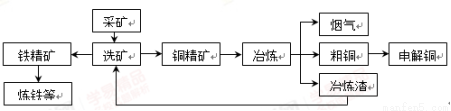
I.回收硫
(1)工业上,采用饱和亚硫酸钠溶液吸收烟气中二氧化硫,写出离子方程式:。
然后,加热吸收液收集SO2。将二氧化硫、空气在稀硫酸中构成原电池,负极反应式为。
II.冶炼铜
(2)工业上,火法冶炼铜分两步:第一步,含铜矿(主要成分是Cu2S)在空气中煅烧生成氧化亚铜和刺激性气味气体;第二步,氧化亚铜和铜矿在高温下反应生成铜和刺激性气体。写出冶炼铜的总反应方程式:。
(3)用电解法精炼粗铜(含银、金、铁、锌杂质),装置如图所示。下列说法不正确的是。
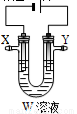
A.Y极为粗铜、X极为纯铜
B.X极净增质量等于Y极净减质量
C.铜盐溶液都可以作精炼铜的电解质溶液
D.若电路有1mol电子转移,则X极净增32g
(4)几种金属离子的沉淀pH:
金属氢氧化物 | 开始沉淀pH | 完全沉淀的pH |
Fe(OH)3 | 2.7 | 3.7 |
Fe(OH)2 | 7.6 | 9.7 |
Cu(OH)2 | 4.6 | 6.4 |
Zn(OH)2 | 5.9 | 8.9 |
铜盐溶液中Fe2,Zn2+对精炼铜可能会产生影响。工业上,除去Fe2+方法是,在酸性混合溶液中加入(选填:双氧水、次氯酸钠、氯水或高锰酸钾溶液)将Fe2+氧化成Fe3+,离子方程式为。加入碱调节溶液pH范围为。
III.冶炼铁
(5)化工厂利用菱铁矿(主要成分是碳酸亚铁)冶炼铁的原理是(用化学方程式表示):。生铁炼钢的主要原理是。
(6)生铁在湿润空气中发生电化学腐蚀最终生成红色铁锈,金属电化腐蚀类型为。
查看答案和解析>>
科目:高中化学 来源:2017届陕西西安市高三上第二次质量检测化学试卷(解析版) 题型:选择题
下列各组物质中,不是按 (“→”表示一步完成)关系相互转化的是
(“→”表示一步完成)关系相互转化的是
选项 | A | B | C | D |
a | HNO3 | CH2=CH2 | NaOH | Fe |
b | NO2 | CH3CH2Br | NaHCO3 | FeCl3 |
c | NO | CH3CH2OH | Na2CO3 | FeCl2 |
查看答案和解析>>
科目:高中化学 来源:2017届陕西西安市高三上第二次质量检测化学试卷(解析版) 题型:选择题
常温下,在溶液中可以发生反应:X+2Y3+=2Y2++X2+,则下列叙述①X被氧化;②X是氧化剂;③Y2+既具有氧化性也具有还原性;④Y2+是氧化产物;⑤Y3+的氧化性比X2+的氧化性强。以下叙述中正确的是
A.①②⑤
B.①③⑤
C.②④⑤
D.③④⑤
查看答案和解析>>
科目:高中化学 来源:2017届山东师范大学附属中学高三上第二次模拟考试化学试卷(解析版) 题型:选择题
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,其中R元素的氢化物的水溶液能腐蚀玻璃,则下列判断正确的是

A. 非金属性:Z<T<X
B. R与Q的电子数相差26
C. 气态氢化物稳定性:R<T<Q
D. 简单阴离子的还原性:T>Q
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省瓦房店市高一上10月月考化学试卷(解析版) 题型:选择题
某溶液中大量存在以下五种离子:NO3-、SO42-、Fe3+、H+、M。其物质的量浓度之比为c(NO3-)∶c(SO42-)∶c(Fe3+)∶c(H+)∶c(M)=2∶3∶1∶3∶1,则M可能是:
A.Al3+ B.Cl- C.Mg2+ D.Ba2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com