
下列叙述正确的是( )
A甲苯既可使溴的四氯化碳溶液褪色,也可使酸性高锰酸钾溶液褪色
B.有机物 的消去产物有两种
的消去产物有两种
C.有机物A(C4H6O2)能发生加聚反应,可推知A的结构一定是
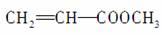
D.可用溴水鉴别甲苯、苯酚、1己烯三种无色液体
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
A、B两种烃,它们含碳质量分数相同,下列关于A和B的叙述正确的是( )
A. A和B一定是同分异构体 B. A和B不可能是同系物
C. A和B最简式一定相同 D. A和B的化学性质相似
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液仅含下列离子中的几种,且所含各种离子的物质的量浓度均为0.lmol/L(忽略水的电离及离子的水解).K+ Ag+ Mg2+ Al3+ NH4+ Cl﹣ CO32﹣ NO3﹣ SO42﹣ I﹣
用如下各步实验分析该溶液组成:
①取5mL溶液,滴少量稀氨水,发现溶液中有沉淀生成,且离子种类增加.
②用铂丝蘸取溶液,在火焰上灼烧,透过蓝色钻玻璃观察,火焰不显紫色.
③另取溶液加入过量盐酸,有无色气体生成,该无色气体遇空气变成红棕色.
④向步骤③实验所得的溶液中加入BaCl2溶液,有白色沉淀生成.
请回答下列问题:
(1)由步骤②判断,溶液中一定不含有的阳离子是 ;步骤③中生成无色气体的化学式是
最终确定溶液中所含阴离子有 ﹣
(3)另取100mL原溶液,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧沉淀至恒重,得到的固体化学式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
以化学平衡与化学反应速率的关 系可知()
系可知()
A. 化学反应速率变化时,化学平衡一定发生移动
B. 化学平衡发生移动时、化学反应速率一定变化
C. 正反应进行的程度大、正反应速率一定大
D. 只有使用催化剂才会发生化学反应速率变化,而化学平衡不移动的情况.
查看答案和解析>>
科目:高中化学 来源: 题型:
氨是一种重要的化工原料,氨的合成和应用是当前的重要研究内容之一.
(1)传统哈伯法合成氨工艺中,
①升高温度,正反应速率(V正) (填“增大”、“减小”或“不变”).
②若增大压强,N2的转化率 ;若已达平衡后再加入N2,N2的转化率减小(填“增大”、“减小”或“不变”).
③若加压到10×101.3KPa时,其它条件不变,发现平衡逆向移动,原因应该是
A.由于体积变大了,反应朝着体积增大方向移动
B.由于N2状态发生了变化
C.由于体积变小了,反应朝着体积增大方向移动
D.由于N2和H2的状态都发生了变化
E.由于H2状态发生了变化,N2状态可能发生变化也可能没有变化
④如图表示上述反应在某一时间段中反应速率与反应过程的关系图.由图判断,NH3的百分含量最高的一段时间是 .
⑤据图判断反应在t2~t3这段时间内,曲线变化的原因是D,t5~t6时间内曲线变化的原因可能是B(以上均填编号).
A.加了催化剂 B.扩大容器的体积 C.降低温度 D.增大压强
⑥不同温度、压强下,合成氨平衡体系中NH3的物质的量分数见表(N2和H2的起始物质的量之比为1:3 ).分析表中数据,200℃100MPa时H2转化率最高.
实际工业生产不选用该条件的主要原因是 .
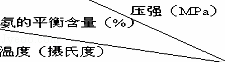 0.1 10 20 30 60 100
0.1 10 20 30 60 100
200 15.3 81.5 86.4 89.9 95.4 98.8
300 2.2 52.0 64.2 71.0 84.2 92.6
400 0.4 25.1 38.2 47.0 65.2 79.8
500 0.1 10.6 19.1 26.4 42.2 57.5
600 0.05 4.5 9.1 13.8 23.1 31.4
(2)最近美国Simons等科学家发明了不必使氨先裂化为氢就可直接用于燃料电池的方法.它既有液氢燃料电池的优点,又克服了液氢不易保存的不足.其装置为用铂黑作为电极,加入电解质溶液中,一个电极通入空气,另一电极通入氨气.其电池反应为4NH3+3O2═2N2+6H2O.写出负极电极反应式 ,你认为电解质溶液应显 (填“酸性”、“中性”、“碱性”),其原因是 .

查看答案和解析>>
科目:高中化学 来源: 题型:
300多年前,著名化学家波义耳发现了铁盐与没食子酸的显色反应,并由此发明了蓝黑墨水。没食子酸的结构式为
(1)用没食子酸制造墨水主要利用了________类化合物的性质(填代号)。
A.醇 B.酚 C.油脂 D.羧酸
(2)没食子酸丙酯具有抗氧化作用,是目前广泛应用的食品添加剂,其结构简式为______________。
(3)尼泊金酯是对羟基苯甲酸与醇形成的酯类化合物,是国家允许使用的食品防腐剂。尼泊金丁酯的分子式为__________,其苯环只与-OH和-COOR两类取代基直接相连的同分异构体有________种。
(4)写出尼泊金乙酯与氢氧化钠溶液加热反应的化学方程式:
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
1791年,法国医生路布兰首先获得制碱专利,以食盐、浓硫酸、石灰石、煤为原料制碱,该方法分三步:
①用NaCl与H2SO4反应制Na2SO4:2NaCl+H2SO4═Na2SO4+2HCl↑
②用焦炭还原Na2SO4制Na2S:Na2SO4+4C═Na2S+4CO↑
③用硫化钠与石灰石反应制Na2CO3:Na2S+CaCO3═Na2CO3+CaS
下列说法正确的是( )
|
| A. | ②③两步都是氧化还原反应 |
|
| B. | 只有第②步是氧化还原反应 |
|
| C. | 该方法对生产设备基本没有腐蚀 |
|
| D. | 该方法对环境污染较小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是( )
|
| A. | NaHCO3溶液与盐酸:CO32﹣+2 H+=H2O+CO2↑ |
|
| B. | 硝酸银溶液与铜:Cu+Ag+=Cu2++Ag |
|
| C. | 金属钾与水反应:K+H2O═K++OH﹣+H2↑ |
|
| D. | 用醋酸除水垢:2CH3COOH+CaCO3=Ca2++2CH3COO﹣+H2O+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com