
��1����0.2mol/L HA ��Һ�� 0.1mol/L NaOH��Һ�������ϣ���û����Һ��c��Na+��>c��A?�������á�>������<����=����д���пհף���
�ٻ����Һ��c��A?��_________c��HA����
�ڻ����Һ��c��HA�� + c��A?�� 0.1mol/L��
��2������ʱ��ȡ0.1mol•L-1 HX��Һ��0.1mol•L-1 NaOH��Һ�������ϣ���Ϻ���Һ����ı仯���ƣ���û����Һ��pH=8���Իش��������⣺
�ٻ����Һ����ˮ�������c��OH-����0.1mol•L-1 NaOH��Һ����ˮ�������c��OH-��֮��Ϊ ��
����֪NH4X��Һ�����ԣ���֪��HX��Һ���뵽Na2CO3��Һ��������ų������ƶϣ�NH4��2CO3��Һ��pH__________7��ѡ���������������������
 ѧ���쳵�����ּ��ں�����ҵϵ�д�
ѧ���쳵�����ּ��ں�����ҵϵ�д� ��˼ά������ҵϵ�д�
��˼ά������ҵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡۣ��һ�ߡ�Ҷ�ض��ߵ���У�߶������л�ѧ���������棩 ���ͣ�ѡ����
����H+����Cl������Al3������K������S2������OH������NO3������NH4���ֱ����H2O�У������ϲ�Ӱ��ˮ�ĵ���ƽ����ǣ� ��
A���٢ۢݢߢ� B���ڢܢ� C���٢� D���ڢܢޢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ��һ��ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������Ӧ���У������ý���֪ʶ���͵���
A���峿����ï�ܵ����֣��������Կ�����֦Ҷ������һ��������
B��һ֧�ֱ�ʹ�����ֲ�ͬ�ƺŵ�����īˮ���׳��ֶ���
C���ڱ���FeCl3��Һ����μ���NaOH��Һ���������ɫ����
D���ں�ˮ�뺣ˮ���紦���������γ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
һ���¶��£�ij�ݻ��ɱ�������У���Ӧ2A��g��+B��g�� 2C��g���ﵽƽ��ʱ��A��B��C�����ʵ����ֱ�Ϊ4moL��2moL��4moL�������¶Ⱥ�ѹǿ���䣬��ƽ�����������ߵ��������µ�������ʹƽ�����Ƶ��ǣ� ��
2C��g���ﵽƽ��ʱ��A��B��C�����ʵ����ֱ�Ϊ4moL��2moL��4moL�������¶Ⱥ�ѹǿ���䣬��ƽ�����������ߵ��������µ�������ʹƽ�����Ƶ��ǣ� ��
A�����ӱ� B������ �� C��������1moL D��������1moL
�� C��������1moL D��������1moL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ���ǣ� ��
A�����ȷ�Ӧ�ڳ����¶���������
B�����ȷ�Ӧ�����ȾͲ��ᷢ��
C����Ҫ���Ȳ��ܷ����ķ�Ӧ�������ȷ�Ӧ
D�����ݷ�Ӧ����������������������Դ�С��ȷ����Ӧ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ���й����ʵ�Ũ�ȹ�ϵ��ȷ���ǣ� ��
A��c��NH4+����ȵ�NH4HCO3��NH4HSO4��NH4Cl��Һ�У�C��NH4HSO4����C��NH4HCO3����C��NH4Cl��
B�����������Һ�м����������ᣬ�õ������Ի����Һ��:c��Na+��>c��CH3COO-��>c��H+��>c��OH-��
C��1��0mol/LNa2CO3��Һ�У�c��OH-��=c��HCO3-��+2c��HCO3��+c��H+��
D��ij��Ԫ�������ʽ��NaHA��Һ�У�c��Na+��+c��H+��=c��HA-��+c��OH-��+c��A2-��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�������ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ܴٽ�ˮ�ĵ��룬��ʹ��Һ��c��H+����c��OH-���IJ�����
�ٽ�ˮ������� ����ˮ��Ͷ��һС������� ����ˮ��ͨCO2
����ˮ�м����������� ����ˮ�м�NaHCO3���� ����ˮ�м�NaHSO4����
A���� B���٢ܢ� C���ۢܢ� D���٢ڢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ӱ�ʡ��һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
200 mL Fe2(SO4)3��Һ�к�Fe3�� 56 g����Һ��SO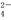 �����ʵ���Ũ���� ( )
�����ʵ���Ũ���� ( )
A��7.5 mol/L B��5 mol/L C��10 mol/L D��2.5 mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ɽ��ʡ�߶������л�ѧ�Ծ��������棩 ���ͣ������
��.���¡���ѹ�£���һ���ɱ��ݻ��������з������·�Ӧ��A������+B������ C������
C������
��1������ʼʱ����1molA��1molB������ƽ�������a molC������ʼʱ����3mol A��3mol B������ƽ�������C�����ʵ���Ϊ__________mol��
��2������ʼʱ����x molA��2molB��1molC������ƽ���A��C�����ʵ����ֱ���ymol��3a mol����x=__________mol��y=__________mol��ƽ��ʱ��B�����ʵ���__________��ѡ��һ����ţ�
���ף�����2mol ���ң�����2mol ������С��2mol ���������ܴ��ڡ����ڻ�С��2mol
��3�����ڣ�2����ƽ���������ټ���3molC�����ٴε���ƽ���C�����ʵ���������__________��
��.��ά���¶Ȳ��䣬��һ���루1����Ӧǰ��ʼ�����ͬ�����ݻ��̶��������з���������Ӧ��
��4����ʼʱ����1molA��1molB����ƽ�������b molC����b�루1��С���е�a���бȽ���ȷ����__________��ѡ��һ����ţ���
���ף�a��b ���ң�a��b ������a=b ���������ܱȽ�a��b�Ĵ�С
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com